Clear Sky Science · zh
通过对三取代烯烃进行氢氨化实现具有邻位立体中心的手性胺的立体可分歧合成
分子形状为何重要
当今许多药物的效力源于三维形状上的微小差异。由相同原子构成的两个分子可能像左右手一样:几乎相同,但一个可能有治疗作用,另一个却有害。该研究提出了一种在一类称为胺的重要分子中雕塑此类形状的新方法,这类胺广泛存在于药物、天然产物和农用化学品中。通过将简单、平面的构件引导为精确的三维排列,这项工作为更可靠地获得既更有效又更安全的药物开辟了途径。
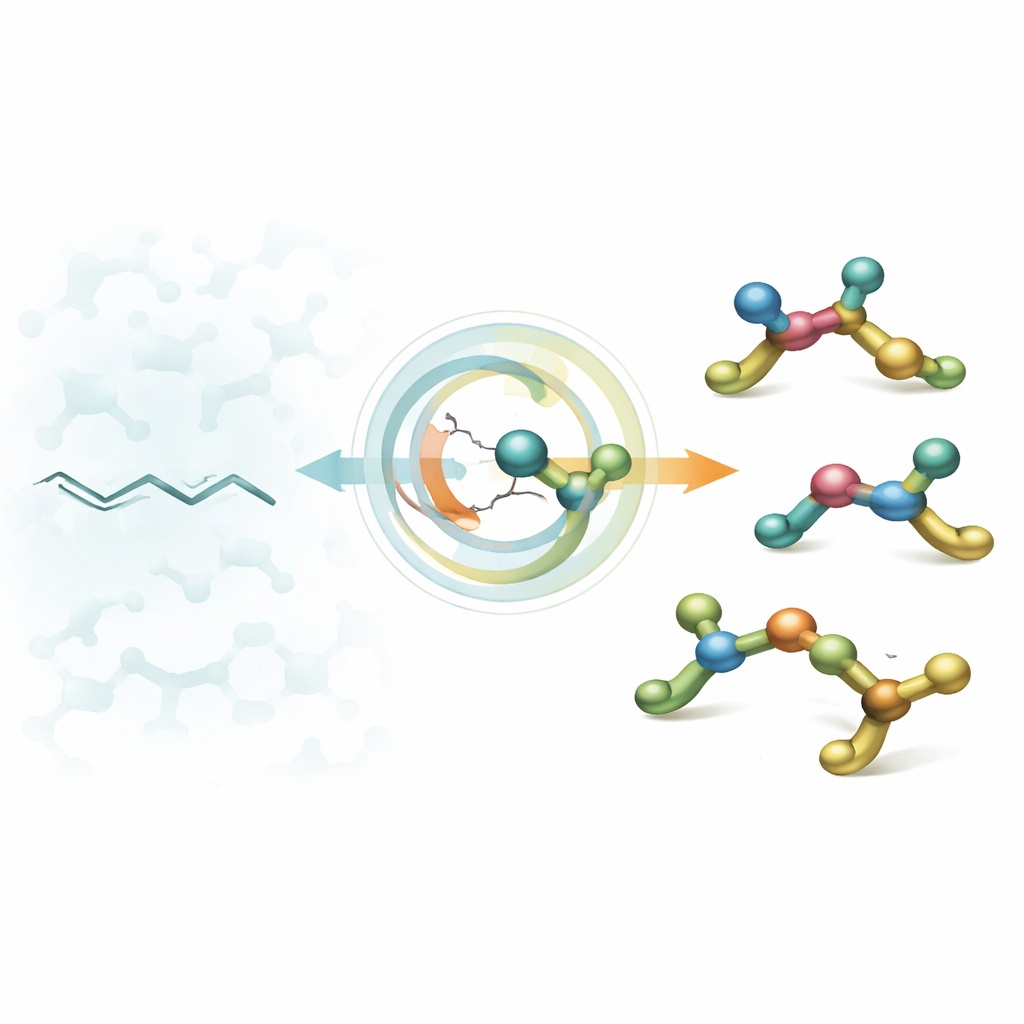
从平面链到三维构件
药物设计者常以脂肪胺为起点——这些含氮小片段可以与生物靶点结合。几十年来,化学家已能熟练构建具有单个“扭转点”(一个立体中心)的胺,但真实药物常包含几个紧邻的此类点。这些密集排列的手性中心能显著改善分子与酶或受体的配合度,但它们以可控方式构建极为困难。现有方法通常只偏向生成一种构型,使化学家缺乏简单而灵活的策略来获得他们可能想测试的所有形状。
一套反应能够指向四种结果
作者通过将易得的三取代烯烃——本质上带拥挤双键的平面碳链——转化为具有两个相邻立体中心的三维胺来解决这一问题。他们的关键步骤是镍催化的氢氨化:镍氢物种首先加到双键上,然后引入胺片段,整个过程经过精心编排。巧妙之处在于产物可通过两个可预测开关控制:起始双键为E或Z构型,以及镍催化配体为R或S构型。翻转这两个设置,就能用相同的反应条件按需获得四种可能的立体异构体中的任意一种。
为真实分子设计
除了概念上的突破之外,该化学反应被证明具有鲁棒性和实用性。该反应兼容范围广泛的胺反应物,从简单的二级胺到携带酯、氨甲酰基、砜甚至常用于后期药物修饰的硼酸酯的更复杂变体。同样,许多不同的三取代烯烃能顺利参与,包括来源于天然产物和现有药物分子的底物。在大多数情况下,该方法以高产率并对镜像体和两个相邻立体中心的相对构型实现优良控制地提供期望的胺产物。
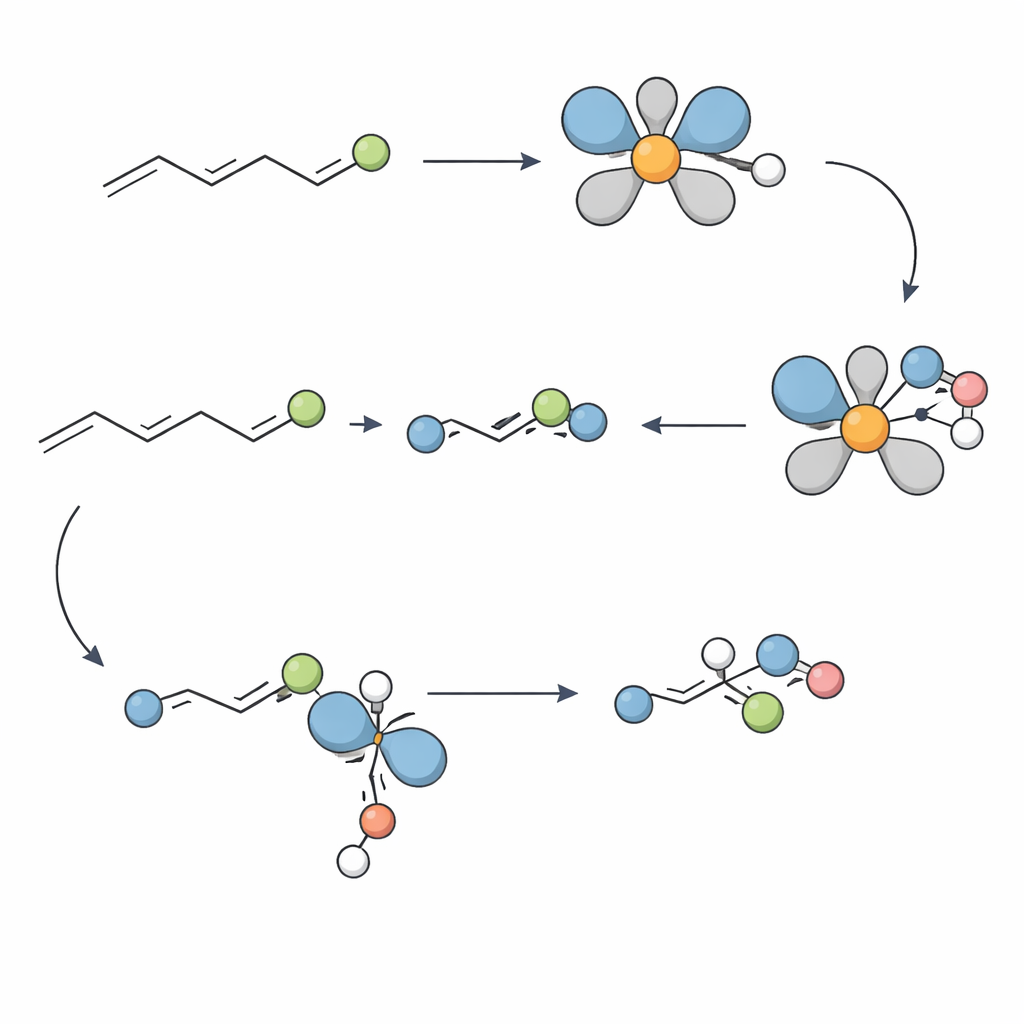
探明催化剂的工作方式
为了理解该方法为何效果良好,团队进行了机理学实验。标记研究表明,镍配合物中的氢化物以单一步骤、不可逆地加到烯烃的特定位点,从而以精确几何构建出两个相邻的立体中心。与可能的自由基捕获剂的测试表明,自由基途径不太可能。相反,高分辨质谱学证据和经晶体学表征的镍配合物提示一个在镍(II)与镍(I)物种之间穿梭的循环。一个关键步骤似乎是在这两种氧化态之间的交接(转金属化),最终导致形成定义胺产物的C–N键。
为未来药物打开新可能性
在实际示范中,作者将该策略用于改造复杂的类药分子,并构建含有N-(2-乙氨基)酰胺基元的立体定义的已知药物类似物。他们还展示了该反应可放大规模进行,产物在后续转化中可保持已设定的立体化学不变。对非专业读者来说,关键信息是化学家现在拥有一种可编程的方法,不仅能调出一种,而是能调出在两个相邻手性中心周围的四种可能三维排列中的任意一种。这一能力应大幅扩展药物发现候选分子的目录,使形状-活性关系的系统探索成为可能,从而最终促成更佳设计的疗法。}
引用: Bai, H., Li, M., Wang, X. et al. Stereodivergent synthesis of chiral amines bearing vicinal stereocenters via hydroamination of trisubstituted alkenes. Nat Commun 17, 3431 (2026). https://doi.org/10.1038/s41467-026-70294-6
关键词: 手性胺, 镍催化, 氢氨化, 立体可分歧合成, 药物发现