Clear Sky Science · sv
Stereodivergent syntes av chirala aminer med intilliggande stereocenter via hydroaminering av trisubstituerade alkener
Varför molekylens form spelar roll
Många av dagens läkemedel får sin verkan från små skillnader i tredimensionell form. Två molekyler byggda av samma atomer kan uppföra sig som vänster och höger hand: nästan identiska, men den ena kan bota medan den andra skadar. Denna studie presenterar ett nytt sätt att forma sådana strukturer i en viktig familj av molekyler kallade aminer, som förekommer i läkemedel, naturprodukter och växtskyddskemikalier. Genom att lära enkla, platta byggstenar att vika sig till precisa 3D-arrangemang öppnar arbetet en mer pålitlig väg till läkemedel som både är mer effektiva och säkrare.
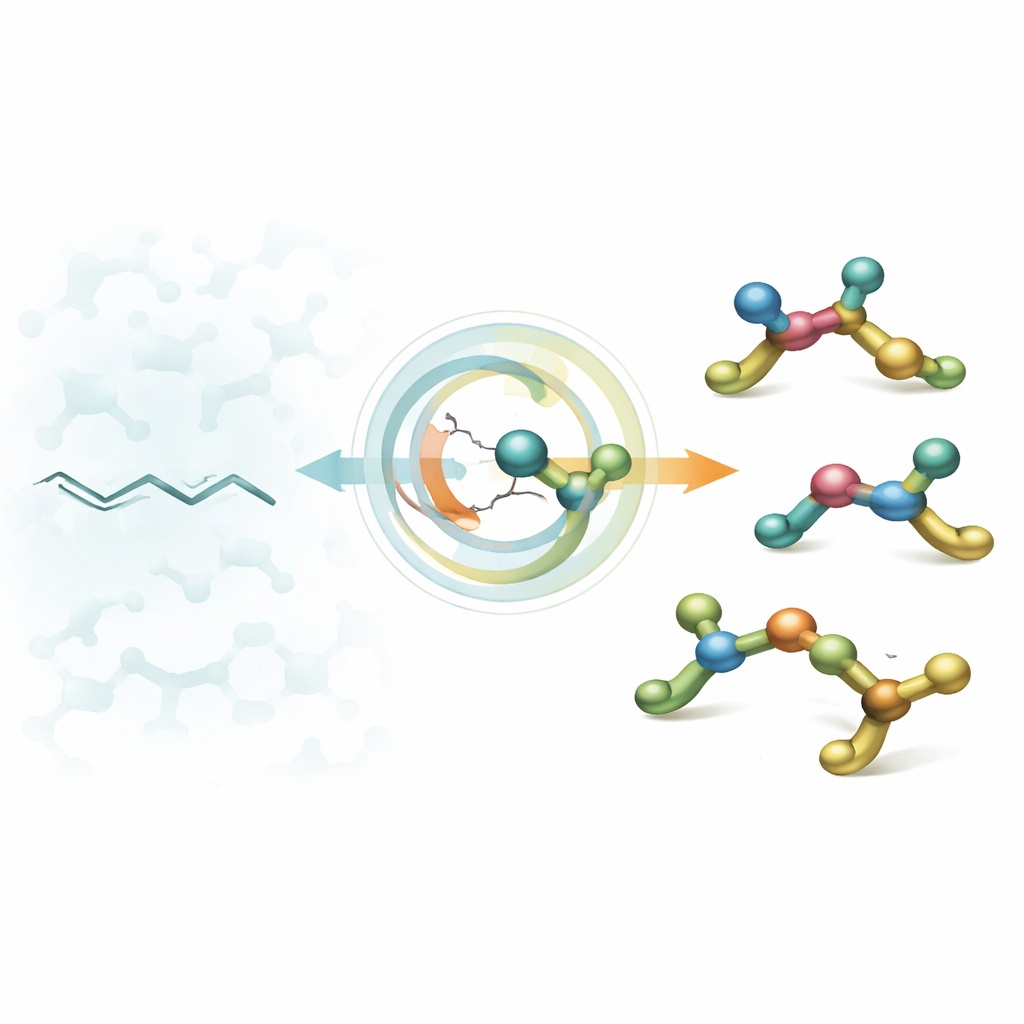
Från platta kedjor till 3D‑byggstenar
Läkemedelsdesigners utgår ofta från alifatiska aminer – små kvävehaltiga fragment som passar in i biologiska mål. Under årtionden har kemister blivit skickliga på att göra aminer med en enda "vridpunkt" (ett stereocenter), men verkliga läkemedel innehåller ofta flera sådana punkter tätt intill varandra. Dessa tätt packade chirala center kan dramatiskt förbättra hur en molekyl passar in i ett enzym eller en receptor, men de är ökända för att vara svåra att bygga kontrollerat. Befintliga metoder gynnar vanligtvis bara en konfiguration, vilket lämnar kemister utan en enkel, flexibel strategi för att nå alla former de vill undersöka.
En enda reaktion som kan sikta i fyra riktningar
Författarna tar sig an detta problem genom att omvandla lättillgängliga trisubstituerade alkener – i praktiken platta kolkedjor med en trång dubbelbindning – till 3D‑aminer med två intilliggande stereocenter. Deras nyckelsteg är en nickel‑katalyserad hydroaminering: en nickelhyridart först adderas över dubbelbindningen, och sedan kopplas ett aminfragment på i en noggrant koreograferad sekvens. Den smarta vändningen är att utfallet beror på ett förutsägbart sätt på bara två brytare: om startdubbelbindningen är i E‑ eller Z‑arrangemang, och om nickels chirala ligand är R‑ eller S‑versionen. Genom att växla dessa två inställningar kan samma reaktionsuppställning ge någon av de fyra möjliga stereoisomererna på begäran.
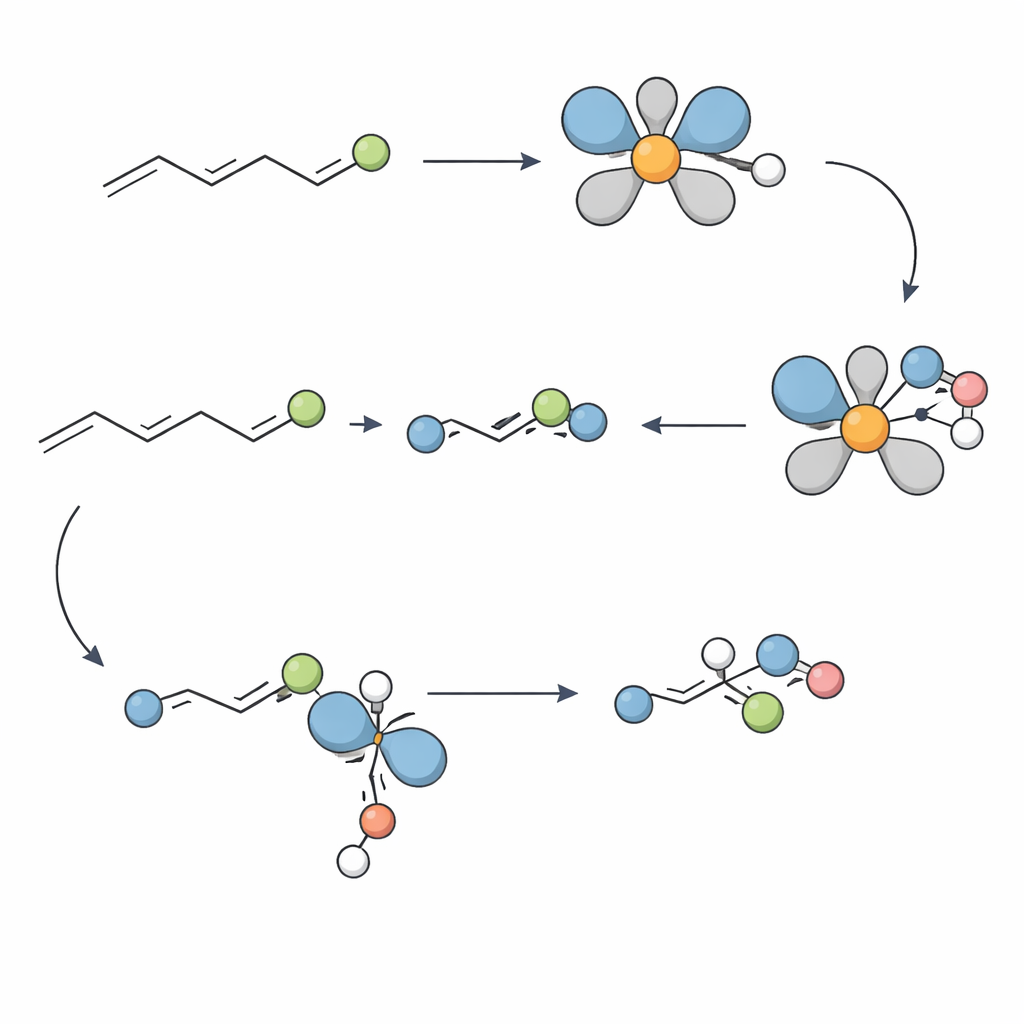
Utformat för verkliga molekyler
Bortom det konceptuella framsteget visar sig kemin vara robust och praktisk. Reaktionen tolererar ett brett spektrum av aminpartners, från enkla sekundära aminer till mer utsmyckade varianter som bär estrar, karbamater, sulfoner och till och med boronater som ofta används senare i läkemedelsmodifiering. Likaså deltar många olika trisubstituerade alkener smidigt, inklusive sådana härledda från naturprodukter och befintliga läkemedel. I de flesta fall levererar processen de önskade aminerna i höga utbyten och med utmärkt kontroll över både vilken spegelbild som bildas och hur de två intilliggande stereocenterna är arrangerade.
Undersöka hur katalysatorn gör sitt arbete
För att förstå varför metoden fungerar så väl genomförde teamet mekanistiska experiment. Märkningsstudier visade att hydriden i nickelkomplexet adderar till en specifik position på alkenerna i ett enda, icke‑reversibelt steg, vilket etablerar de två intilliggande stereocenterna med precis geometri. Tester med potentiella radikalfällor antydde att friradikalvägar är osannolika. Istället pekar bevis från högupplöst massespektrometri och ett kristallografiskt karaktäriserat nickelkomplex mot en cykel som växlar mellan nickel(II)- och nickel(I)-arter. Ett nyckelsteg tycks vara en överlämning (transmetallering) mellan dessa två oxidationsstater, vilket slutligen leder till bildandet av C–N‑bindningen som definierar aminprodukten.
Nya möjligheter för framtida läkemedel
I praktiska demonstrationer applicerade författarna sin strategi för att modifiera avancerade läkemedelslika molekyler och för att bygga stereo‑definierade analoger av befintliga läkemedel som innehåller ett N‑(2‑etylamino)amidmotiv. De visade också att reaktionen kan skalas upp och att de framställda produkterna kan omvandlas vidare utan att förlora sin noggrant inställda stereokemi. För icke‑specialister är huvudbudskapet att kemister nu har ett programmerbart sätt att ställa in inte bara en, utan alla fyra möjliga 3D‑arrangemang kring två intilliggande chirala center i värdefulla aminstrukturer. Denna förmåga bör avsevärt utöka menyn av kandidatmolekyler för läkemedelsupptäckt, möjliggöra mer systematisk utforskning av form–aktivitetssamband och i slutändan bättre utformade behandlingar.
Citering: Bai, H., Li, M., Wang, X. et al. Stereodivergent synthesis of chiral amines bearing vicinal stereocenters via hydroamination of trisubstituted alkenes. Nat Commun 17, 3431 (2026). https://doi.org/10.1038/s41467-026-70294-6
Nyckelord: chirala aminer, nickelkatalys, hydroaminering, stereodivergent syntes, läkemedelsupptäckt