Clear Sky Science · de
Stereodivergente Synthese chiraler Amine mit benachbarten Stereozentren durch Hydroaminierung trisubstituierter Alkene
Warum die Form eines Moleküls zählt
Viele moderne Medikamente verdanken ihre Wirksamkeit sehr kleinen Unterschieden in der dreidimensionalen Gestalt. Zwei aus den gleichen Atomen aufgebaute Moleküle können wie linke und rechte Hand wirken: fast identisch, doch das eine heilt, während das andere schaden kann. Diese Studie stellt eine neue Methode vor, mit der sich solche Gestalten in einer wichtigen Molekülklasse, den Aminen, gezielt formen lassen. Amine kommen in Arzneistoffen, Naturstoffen und Agrochemikalien häufig vor. Indem einfache, flache Bausteine zu präzisen 3D‑Anordnungen geführt werden, eröffnet die Arbeit einen verlässlicheren Weg zu Wirkstoffen, die wirksamer und sicherer sind.
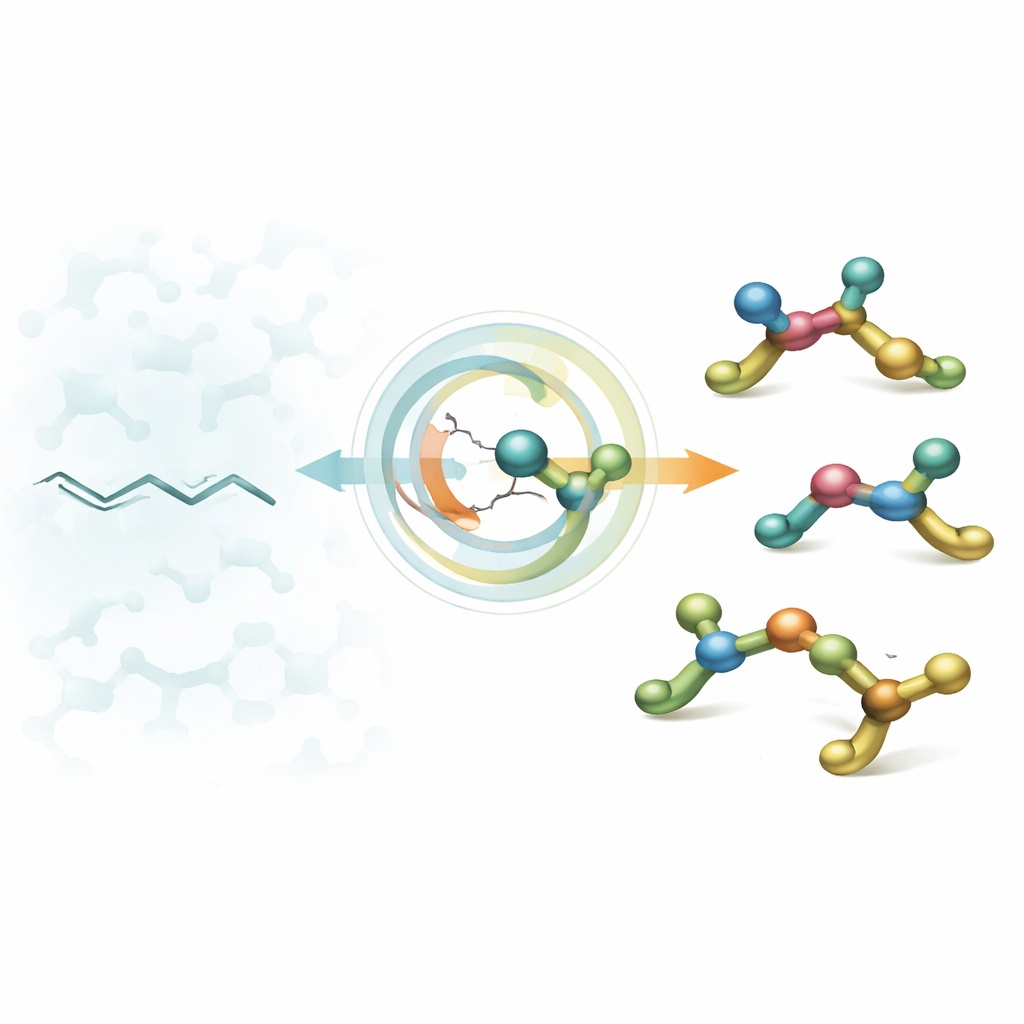
Von flachen Ketten zu 3D‑Bausteinen
Arzneimitteldesigner beginnen häufig mit aliphatischen Aminen – kleinen, stickstoffhaltigen Fragmenten, die an biologische Ziele andocken. Chemiker sind seit Jahrzehnten routiniert darin, Amine mit einem einzelnen „Drehpunkt“ (einem Stereozentrum) herzustellen, doch echte Wirkstoffe enthalten oft mehrere solcher Zentren direkt nebeneinander. Diese eng beieinanderliegenden chiralen Zentren können die Passform eines Moleküls in ein Enzym oder einen Rezeptor drastisch verbessern, sind aber berüchtigt schwer kontrolliert zu erzeugen. Bestehende Methoden bevorzugen in der Regel nur eine Konfiguration und lassen Chemiker ohne einfache, flexible Strategie zurück, um alle gewünschten Gestalten zu erreichen.
Eine einzige Reaktion mit vier Zielen
Die Autoren lösen dieses Problem, indem sie leicht verfügbare trisubstituierte Alkene – im Grunde flache Kohlenstoffketten mit einer überfüllten Doppelbindung – in 3D‑Amine mit zwei benachbarten Stereozentren umwandeln. Ihr Schlüsselzug ist eine nikkel‑katalysierte Hydroaminierung: Ein Nickelhydrid‑Spezies addiert zunächst über die Doppelbindung, danach wird ein Aminfragment eingeführt, alles in einer sorgfältig abgestimmten Abfolge. Der clevere Kniff besteht darin, dass das Ergebnis auf vorhersehbare Weise von nur zwei Stellschrauben abhängt: davon, ob die Anfangsdoppelbindung in E‑ oder Z‑Anordnung vorliegt, und davon, ob das chirale Ligand des Nickels die R‑ oder S‑Form hat. Durch Umlegen dieser beiden Einstellungen kann die gleiche Reaktionsanordnung auf Abruf eines der vier möglichen Stereoisomere liefern.
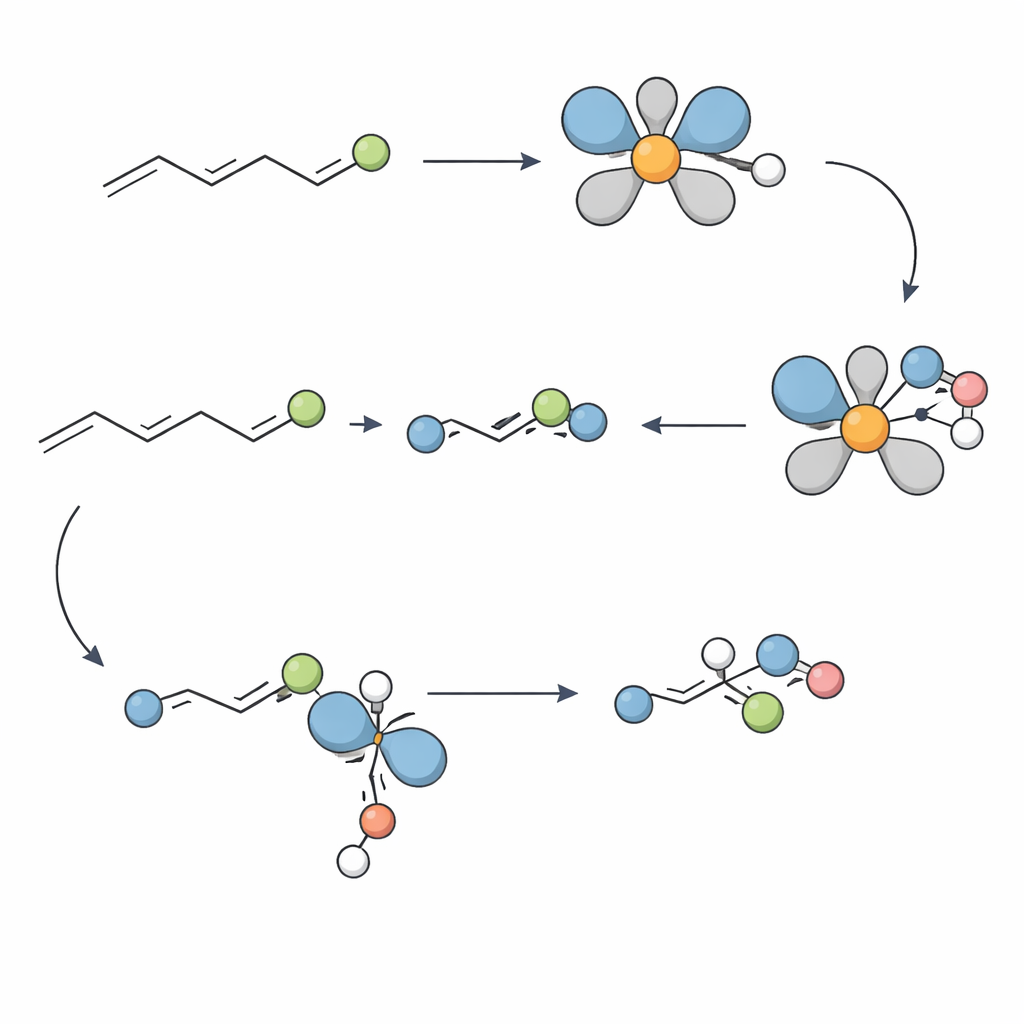
Für reale Moleküle entworfen
Über den konzeptionellen Fortschritt hinaus erweist sich die Chemie als robust und praktisch. Die Reaktion toleriert eine breite Palette von Aminpartnern, von einfachen sekundären Aminen bis hin zu stärker funktionalisierten Varianten mit Estern, Carbamaten, Sulfonen und sogar Boronsäureestern, die häufig später bei der Wirkstoffmodifikation verwendet werden. Ebenso reagieren viele verschiedene trisubstituierte Alkene problemlos, einschließlich solcher, die aus Naturstoffen und bestehenden Arzneimitteln abgeleitet sind. In den meisten Fällen liefert der Prozess die gewünschten Amine in hohen Ausbeuten und mit exzellenter Kontrolle sowohl darüber, welches Spiegelbild gebildet wird, als auch darüber, wie die beiden benachbarten Stereozentren angeordnet sind.
Aufklärung, wie der Katalysator arbeitet
Um zu verstehen, warum die Methode so gut funktioniert, führten die Autoren mechanistische Experimente durch. Markierungsstudien zeigten, dass das Hydrid im Nickelkomplex an einer spezifischen Position der Doppelbindung in einem einzelnen, irreversiblen Schritt addiert und so die beiden benachbarten Stereozentren mit präziser Geometrie festlegt. Tests mit möglichen Radikalfängern deuteten darauf hin, dass freie Radikalwege unwahrscheinlich sind. Stattdessen deuten Befunde aus hochauflösender Massenspektrometrie und ein kristallografisch charakterisierter Nickelkomplex auf einen Zyklus hin, der zwischen Nickel(II)- und Nickel(I)-Spezies pendelt. Ein wichtiger Schritt scheint eine Übergabe (Transmetallierung) zwischen diesen beiden Oxidationsstufen zu sein, die letztlich zur Ausbildung der C–N‑Bindung führt, die das Aminprodukt definiert.
Neue Möglichkeiten für künftige Arzneimittel
In praxisnahen Demonstrationen wendeten die Autoren ihre Strategie an, um fortgeschrittene wirkstoffähnliche Moleküle zu modifizieren und stereo-definierte Analoga bestehender Arzneistoffe zu synthetisieren, die ein N‑(2‑ethylamino)amid‑Motiv enthalten. Sie zeigten auch, dass die Reaktion skaliert werden kann und die resultierenden Produkte weiter umgewandelt werden können, ohne die sorgfältig eingestellte Stereochemie zu verlieren. Für Nichtfachleute lautet die Kernbotschaft: Chemiker haben nun eine programmierbare Methode, um nicht nur eine, sondern alle vier möglichen 3D‑Anordnungen um zwei benachbarte chirale Zentren in wertvollen Aminstrukturen festzulegen. Diese Fähigkeit sollte die Auswahl an Kandidatenmolekülen für die Wirkstoffforschung deutlich erweitern, eine systematischere Erforschung von Form‑Aktivitäts‑Beziehungen ermöglichen und letztlich besser designte Therapien begünstigen.
Zitation: Bai, H., Li, M., Wang, X. et al. Stereodivergent synthesis of chiral amines bearing vicinal stereocenters via hydroamination of trisubstituted alkenes. Nat Commun 17, 3431 (2026). https://doi.org/10.1038/s41467-026-70294-6
Schlüsselwörter: chiral amine, Nikkel-Katalyse, Hydroaminierung, stereodivergente Synthese, Wirkstoffforschung