Clear Sky Science · ru
Стереорасходящая синтез хиральных аминов с соседними стереоцентрами через гидроаминацию триозамещённых алкенов
Почему форма молекулы имеет значение
Многие современные лекарства обязаны своим действием крошечным различиям в трёхмерной форме. Две молекулы, состоящие из одинаковых атомов, могут вести себя как левая и правая рука: почти идентичны, но одна может лечить, а другая навредить. В этом исследовании представлен новый способ придать такие формы важному классу соединений — аминам, которые широко встречаются в лекарствах, природных продуктах и агрохимии. Научившись превращать простые плоские строительные блоки в точные трёхмерные структуры, работа открывает более надёжный путь к созданию лекарств, которые одновременно эффективнее и безопаснее.
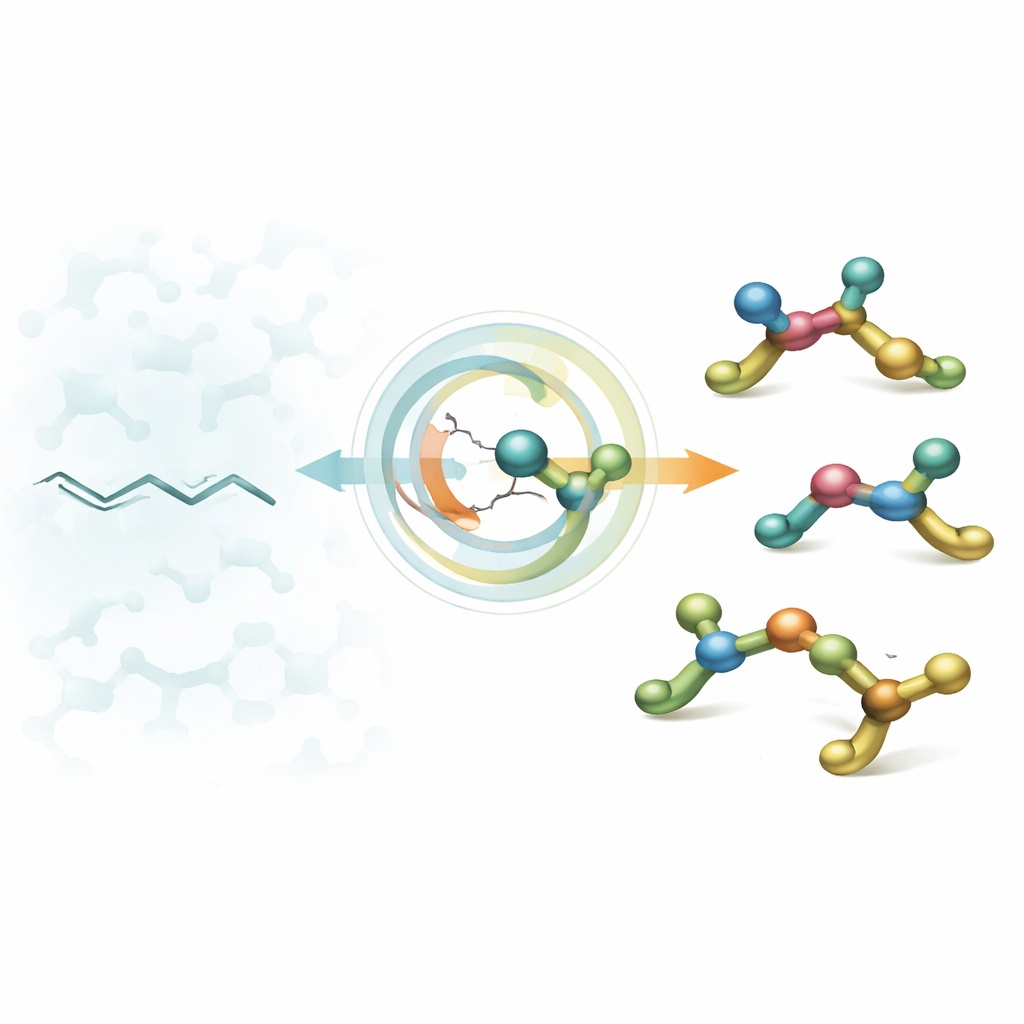
От плоских цепочек к 3D‑блокам
Дизайнеры лекарств часто начинают с алифатических аминов — небольших фрагментов, содержащих азот, которые встраиваются в биологические мишени. Десятилетиями химики научились создавать амины с одной «точкой поворота» (стереоцентром), однако реальные препараты часто содержат несколько таких точек, расположенных рядом друг с другом. Эти плотно расположенные хиральные центры могут существенно улучшить сродство молекулы к ферменту или рецептору, но они чрезвычайно трудно собираются контролируемо. Существующие методы обычно дают преимущество лишь одной конфигурации, оставляя химиков без простой гибкой стратегии для доступа ко всем желаемым формам.
Одна реакция, нацеленная в четыре стороны
Авторы решают эту проблему, превращая доступные триозамещённые алкены — по сути плоские углеродные цепочки с загруженной двойной связью — в трёхмерные амины с двумя соседними стереоцентрами. Ключевой ход — никелевый катализ гидроаминацией: никелевый гидрид сначала добавляется по двойной связи, затем присоединяется аминный фрагмент, всё это выполняется в тщательно скоординированной последовательности. Хитрость в том, что исходный результат предсказуемо зависит всего от двух переключателей: находится ли исходная двойная связь в варианте E или Z и какая из энантиоморфных лигандов никеля — R или S. Переключая эти два параметра, одна и та же схема реакции может дать любой из четырёх возможных стереоизомеров по требованию.
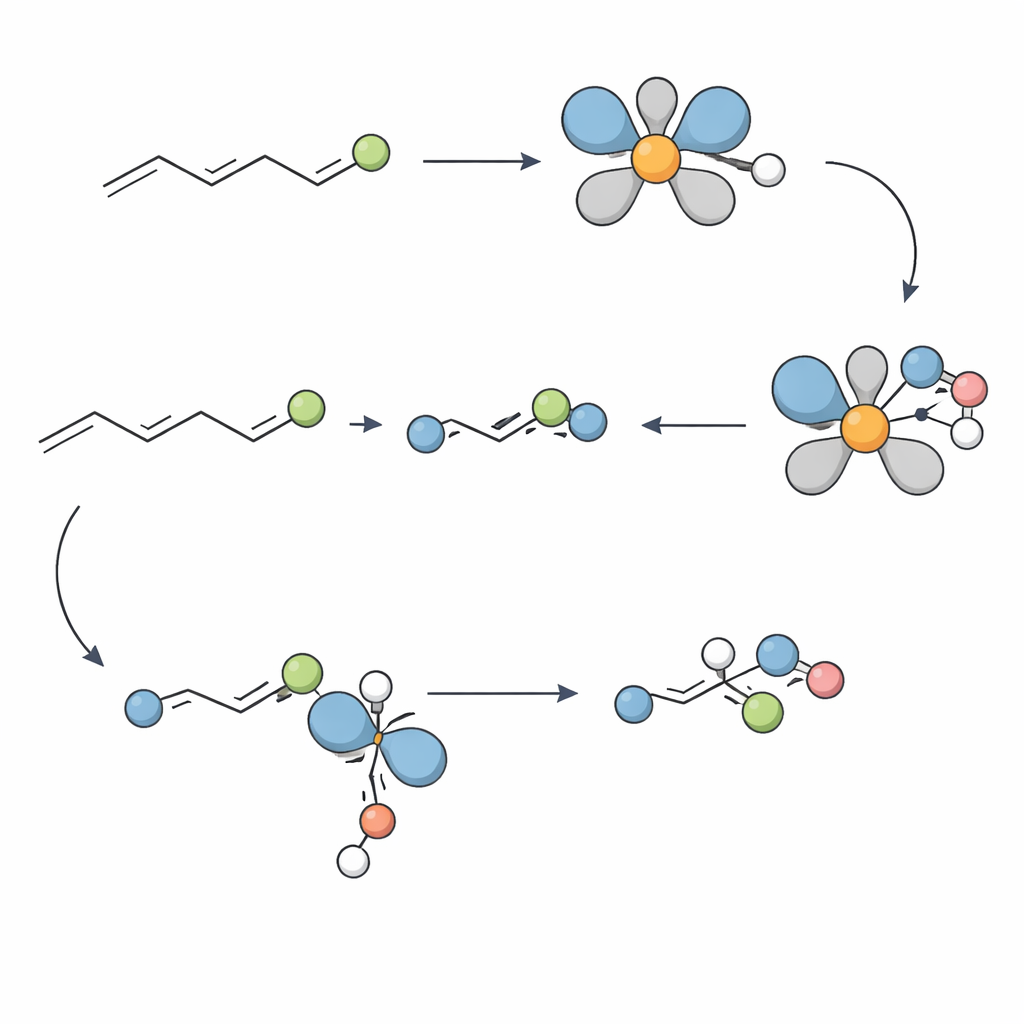
Сконструировано для молекул реального мира
Помимо концептуального прогресса, химия оказалась устойчивой и практичной. Реакция терпима к широкому кругу аминных партнёров — от простых вторичных аминов до более функционализированных вариантов, несущих эфиры, карбаматы, сульфоны и даже бороновые эфиры, часто используемые на поздних стадиях модификации препаратов. Аналогично, многие разные триозамещённые алкены реагируют плавно, включая производные природных продуктов и уже существующих лекарств. В большинстве случаев процесс даёт желаемые амины в высоких выходах и с отличным контролем как над образующимся энантиомером, так и над взаимным расположением двух соседних стереоцентров.
Изучая, как катализатор выполняет свою работу
Чтобы понять, почему метод работает так хорошо, команда провела механистические эксперименты. Исследования с метками показали, что гидрид в никелевом комплексе добавляется в конкретную позицию алкена в одностадийном необратимом шаге, задавая двум соседним стереоцентрам точную геометрию. Испытания с потенциальными ловушками радикалов показали, что свободнорадикальные пути маловероятны. Вместо этого данные высокоразрешающей масс‑спектрометрии и кристаллографически охарактеризованный никелевый комплекс указывают на цикл, который переключается между состояниями никель(II) и никель(I). Ключевым шагом, по-видимому, является перенос между этими степенями окисления (трансметаллизация), что в итоге ведёт к образованию C–N‑связи, определяющей продукт — амин.
Новые возможности для будущих лекарств
В практических примерах авторы применили свою стратегию для модификации сложных лекарственно‑подобных молекул и для синтеза стереоопределённых аналогов существующих препаратов, содержащих мотив N‑(2‑этилaмино)амид. Они также показали, что реакцию можно увеличить в масштабе и что полученные продукты могут быть дальше трансформированы без утраты установленной стереохимии. Для неспециалистов ключевое сообщение таково: у химиков теперь есть программируемый способ устанавливать не одну, а все четыре возможные трёхмерные конфигурации вокруг двух соседних хиральных центров в ценных аминовых структурах. Эта возможность значительно расширит набор кандидатов для поиска лекарств, позволив более системно исследовать взаимосвязь формы и активности и, в итоге, проектировать более совершенные терапии.
Цитирование: Bai, H., Li, M., Wang, X. et al. Stereodivergent synthesis of chiral amines bearing vicinal stereocenters via hydroamination of trisubstituted alkenes. Nat Commun 17, 3431 (2026). https://doi.org/10.1038/s41467-026-70294-6
Ключевые слова: хиральные амины, никелевый катализ, гидроаминация, стереорасходящий синтез, поиск лекарств