Clear Sky Science · nl
Stereodivergente synthese van chirale amines met aangrenzende stereocentra via hydroaminering van trisubstitueerde alkenen
Waarom de vorm van een molecuul ertoe doet
Veel van de actuele geneesmiddelen danken hun werking aan kleine verschillen in driedimensionale vorm. Twee moleculen met dezelfde atomen kunnen zich gedragen als linker- en rechterhand: bijna identiek, maar de ene kan genezen terwijl de ander schadelijk is. Deze studie introduceert een nieuwe manier om zulke vormen te vormen in een belangrijke klasse moleculen, amines, die veel voorkomen in geneesmiddelen, natuurlijke producten en gewasbeschermingsmiddelen. Door eenvoudige, vlakke bouwstenen te laten vouwen naar precieze 3D-arrangementen, opent het werk een betrouwbaardere route naar geneesmiddelen die zowel effectiever als veiliger zijn.
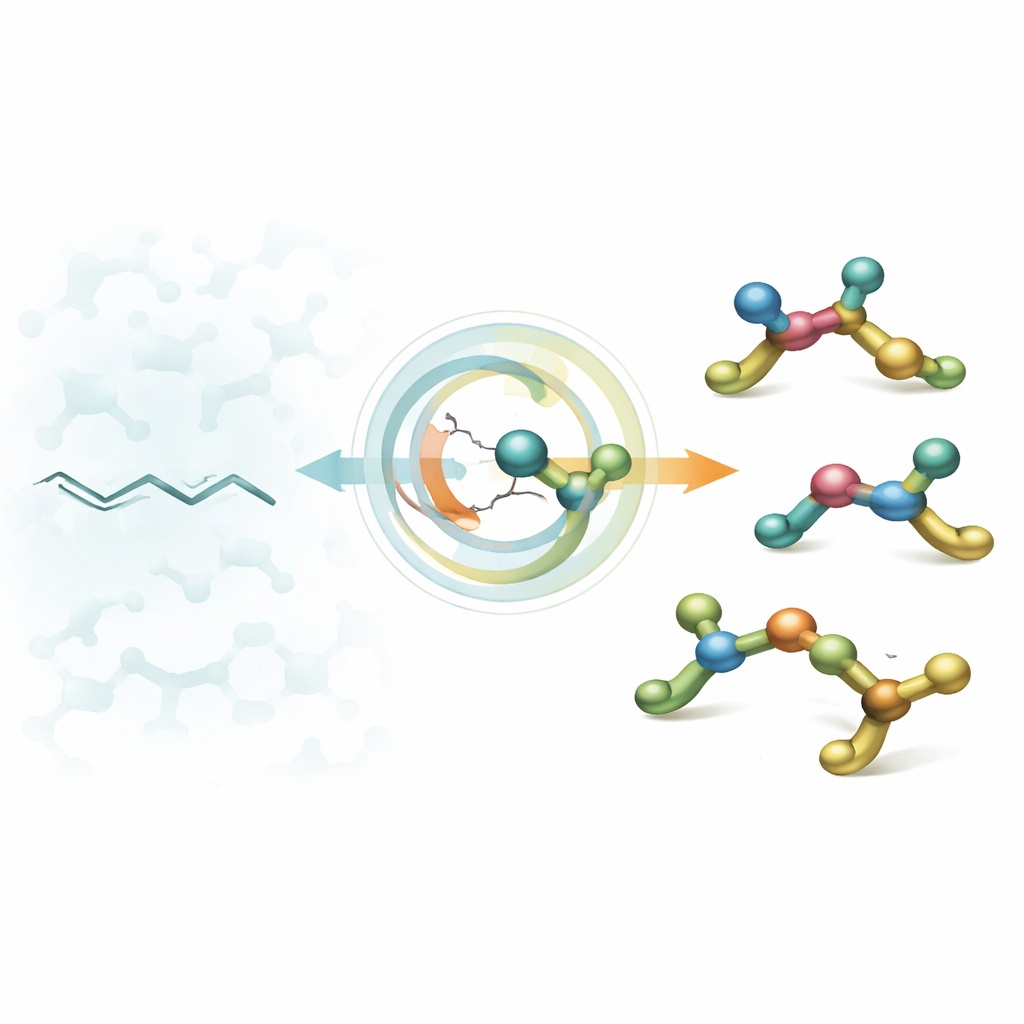
Van vlakke ketens naar 3D‑bouwstenen
Geneesmiddelontwerpers beginnen vaak met alifatische amines — kleine stikstofbevattende fragmenten die in biologische doelen passen. Jarenlang zijn chemici vaardig geworden in het maken van amines met één enkel "draai‑punt" (een stereocentrum), maar echte geneesmiddelen bevatten vaak meerdere zulke punten vlak naast elkaar. Deze dicht opeengepakte chirale centra kunnen sterk verbeteren hoe een molecuul in een enzym of receptor past, maar ze zijn berucht moeilijk gecontroleerd te bouwen. Bestaande methoden geven meestal de voorkeur aan slechts één configuratie, waardoor chemici geen eenvoudige, flexibele strategie hebben om alle gewenste vormen te bereiken.
Een enkele reactie die vier richtingen kan opgaan
De auteurs pakken dit probleem aan door gemakkelijk beschikbare trisubstitueerde alkenen — feitelijk vlakke koolstofketens met een drukbezette dubbele binding — om te zetten in 3D‑amines met twee aangrenzende stereocentra. Hun sleutelzet is een nikkelgekatalyseerde hydroaminering: een nikkel‑hydride‑soort voegt zich eerst over de dubbele binding, waarna een aminefragment wordt aangehecht, alles in een zorgvuldig gechoreografeerde volgorde. De slimme wending is dat het resultaat op een voorspelbare manier afhangt van slechts twee schakelaars: of de beginnende dubbele binding een E‑ of Z‑arrangement heeft en of het chirale ligand van het nikkel de R‑ of S‑versie is. Door deze twee instellingen om te keren, kan dezelfde reactiesetup op verzoek elk van de vier mogelijke stereoisomeren opleveren.
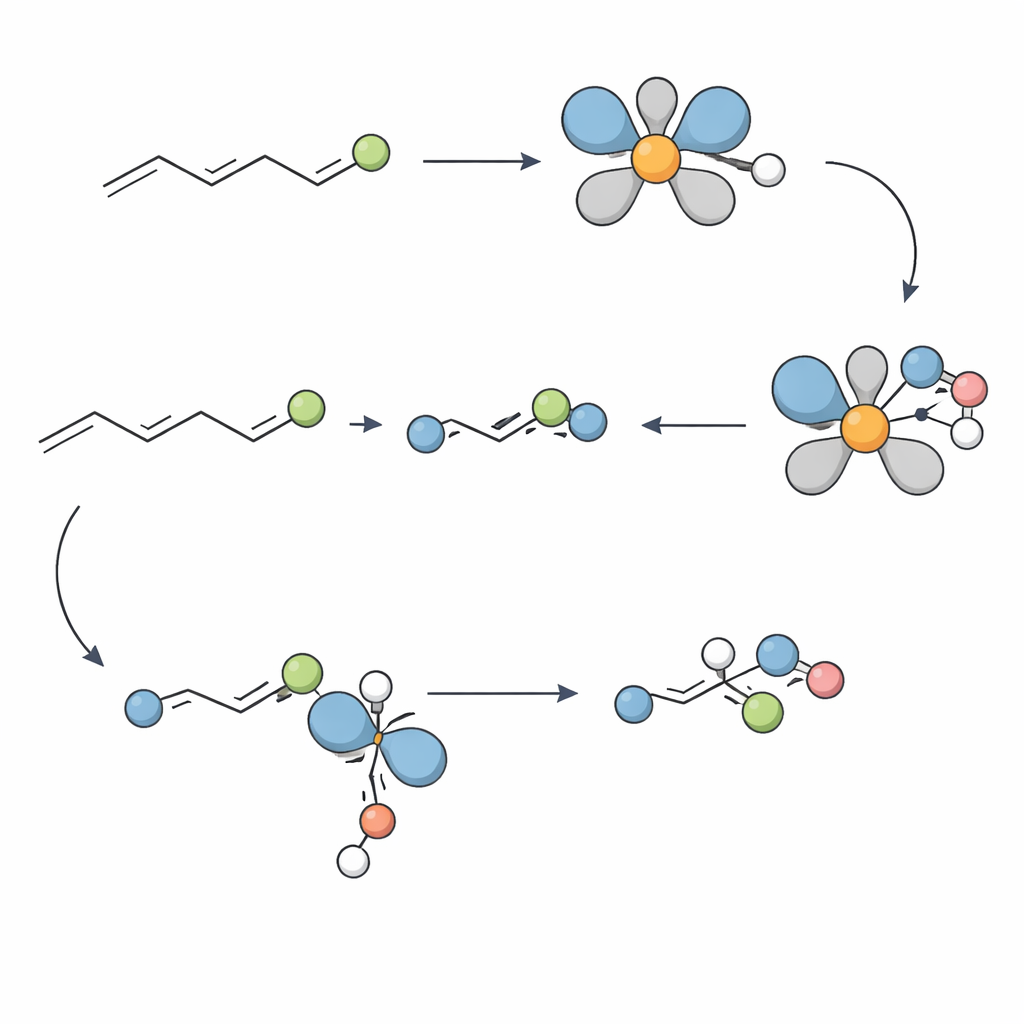
Ontworpen voor moleculen uit de praktijk
Buiten de conceptuele vooruitgang blijkt de chemie robuust en praktisch. De reactie tolereert een breed scala aan aminepartners, van eenvoudige secundaire amines tot meer gesubstitueerde varianten die esters, carbamaten, sulfonen en zelfs boorzuuresters dragen die vaak later in geneesmiddelmodificatie worden gebruikt. Evenzo reageren veel verschillende trisubstitueerde alkenen soepel mee, waaronder derivaten uit natuurlijke producten en bestaande geneesmiddelen. In de meeste gevallen levert het proces de gewenste amines in hoge opbrengsten en met uitstekende controle over zowel welke spiegelbeeldvorm wordt gevormd als over de rangschikking van de twee aangrenzende stereocentra.
Onderzoeken hoe de katalysator zijn werk doet
Om te begrijpen waarom de methode zo goed werkt, voerde het team mechanistische experimenten uit. Labelingstudies toonden aan dat het hydride in het nikkelcomplex zich op één specifieke positie van het alkeen voegt in een enkele, niet‑omkeerbare stap, waarmee de twee aangrenzende stereocentra met precieze geometrie worden vastgezet. Proeven met mogelijke radicalenvangers suggereerden dat vrije‑radicaalroutes onwaarschijnlijk zijn. In plaats daarvan wijzen gegevens van hoogresolutie‑massaspectrometrie en een door kristallografie gekarakteriseerd nikkelcomplex op een cyclus die tussen nikkel(II)- en nikkel(I)-soorten schakeld. Een sleutelstap lijkt een overdracht (transmetalatie) tussen deze twee oxidatietoestanden te zijn, die uiteindelijk leidt tot de vorming van de C–N‑binding die het amineproduct definieert.
Nieuwe mogelijkheden voor toekomstige geneesmiddelen
In praktische demonstraties pasten de auteurs hun strategie toe om geavanceerde geneesmiddelachtige moleculen te modificeren en stereodefiniëerde analogen van bestaande geneesmiddelen te bouwen die een N‑(2‑ethylamino)amide‑motief bevatten. Ze toonden ook aan dat de reactie opgeschaald kan worden en dat de resulterende producten verder getransformeerd kunnen worden zonder hun zorgvuldig ingestelde stereochemie te verliezen. Voor niet‑specialisten is de kernboodschap dat chemici nu een programmeerbare manier hebben om niet slechts één, maar alle vier mogelijke 3D‑rangschikkingen rond twee aangrenzende chirale centra in waardevolle amines in te stellen. Deze mogelijkheid zal het scala aan kandidaatmoleculen voor geneesmiddelenonderzoek sterk uitbreiden, waardoor systematischer onderzoek naar vorm‑activiteitsrelaties mogelijk wordt en uiteindelijk beter ontworpen therapieën.
Bronvermelding: Bai, H., Li, M., Wang, X. et al. Stereodivergent synthesis of chiral amines bearing vicinal stereocenters via hydroamination of trisubstituted alkenes. Nat Commun 17, 3431 (2026). https://doi.org/10.1038/s41467-026-70294-6
Trefwoorden: chirale amines, nikkelkatalyse, hydroaminering, stereodivergente synthese, geneesmiddelenonderzoek