Clear Sky Science · it
Sintesi stereodivergente di ammine chirali con centri stereogenici vicinali tramite idroaminazione di alcheni trisostituiti
Perché la forma di una molecola conta
Molti dei farmaci odierni devono la loro efficacia a piccole differenze nella forma tridimensionale. Due molecole composte dagli stessi atomi possono comportarsi come mano destra e sinistra: quasi identiche, eppure una può curare mentre l’altra nuocere. Questo studio introduce un nuovo modo di scolpire tali forme in una famiglia chiave di molecole chiamate ammine, presenti diffusamente in farmaci, prodotti naturali e agrochimici. Insegnando a semplici blocchi costitutivi piatti a ripiegarsi in disposizioni 3D precise, il lavoro apre una via più affidabile verso farmaci più efficaci e sicuri.
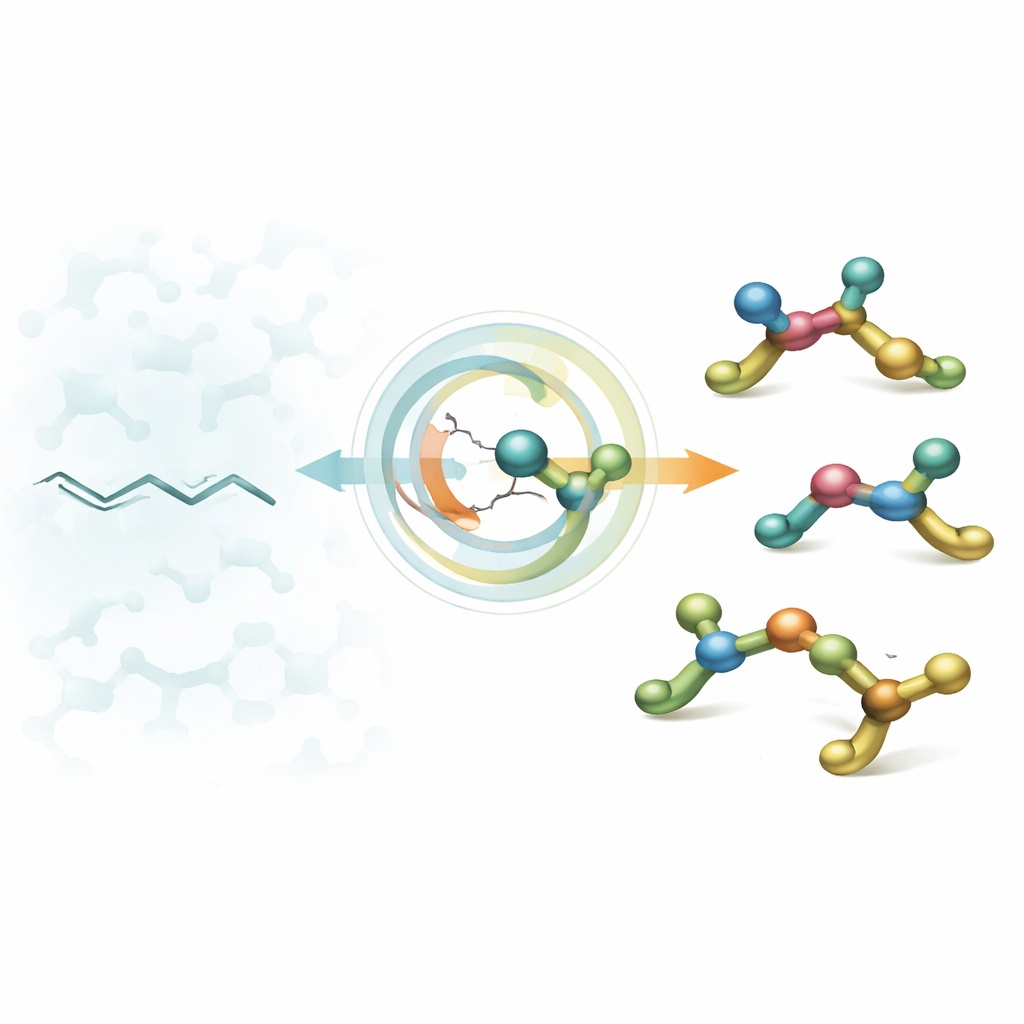
Dalle catene piatte ai mattoni 3D
I progettisti di farmaci spesso partono da ammine alifatiche – piccoli frammenti contenenti azoto che si inseriscono nei bersagli biologici. Per decenni, i chimici sono diventati abili nel preparare ammine con un singolo «punto di torsione» (uno stereocentro), ma i farmaci reali contengono frequentemente diversi di questi punti uno accanto all’altro. Questi centri chirali affollati possono migliorare drasticamente l’adattamento di una molecola a un enzima o a un recettore, ma sono notoriamente difficili da costruire in modo controllato. I metodi esistenti di solito favoriscono un’unica configurazione, lasciando i chimici senza una strategia semplice e flessibile per accedere a tutte le forme che vorrebbero testare.
Un’unica reazione che può mirare in quattro direzioni
Gli autori affrontano questo problema convertendo alcheni trisostituiti prontamente disponibili – essenzialmente catene di carbonio piatte con un doppio legame affollato – in ammine 3D che presentano due centri stereogenici vicinali. La loro mossa chiave è un’idroaminazione catalizzata dal nichel: una specie idruro del nichel si addiziona prima al doppio legame, quindi viene collegato un frammento amminico, il tutto in una sequenza attentamente coreografata. La scelta geniale è che l’esito dipende in modo prevedibile da sole due variabili: se il doppio legame di partenza è nella disposizione E o Z e se il ligando chirale del nichel è la sua versione R o S. Modificando queste due impostazioni, la stessa configurazione di reazione può fornire su richiesta una qualsiasi delle quattro possibili stereoisomeri.
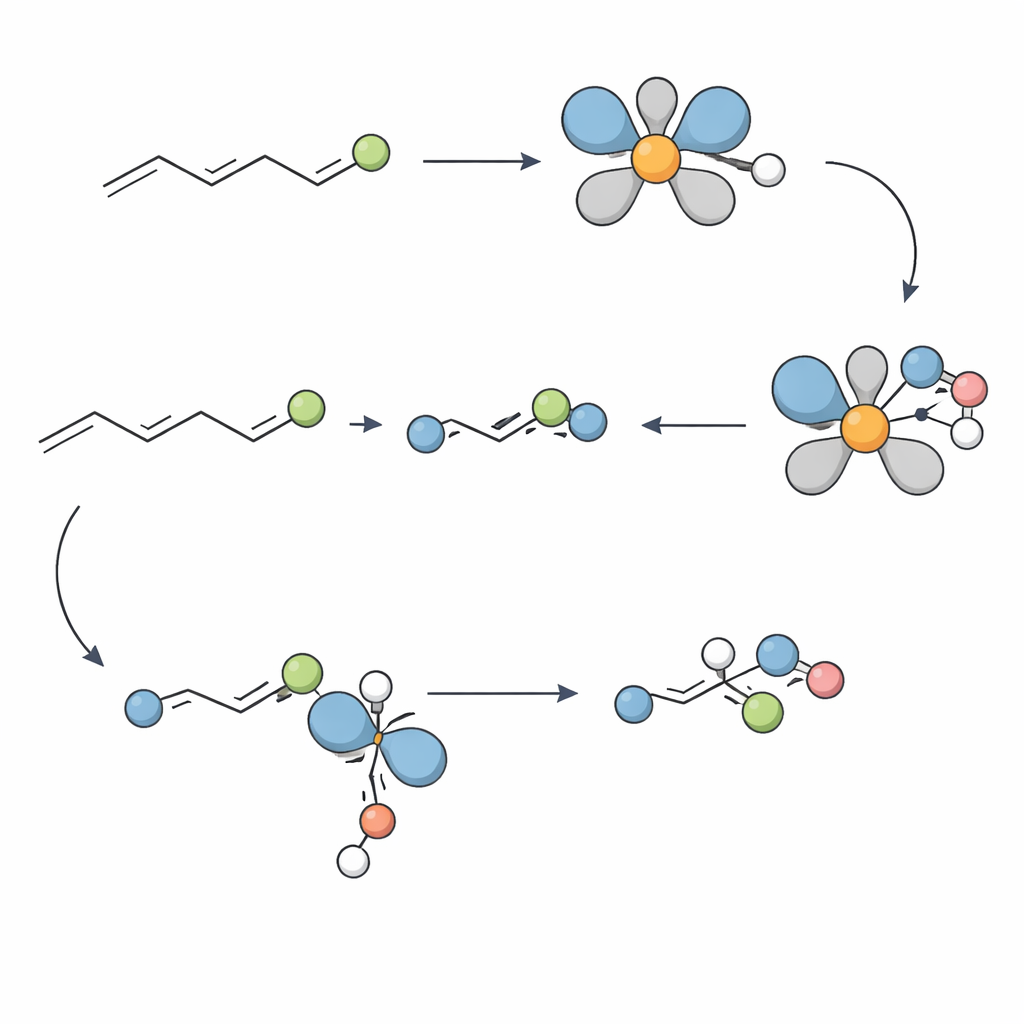
Progettata per molecole del mondo reale
Oltre al progresso concettuale, la chimica si dimostra robusta e pratica. La reazione tollera un’ampia gamma di partner amminici, da semplici ammine secondarie a varianti più funzionalizzate che portano esteri, carbammati, solfoni e persino esteri boronici spesso impiegati in successivi passaggi di modifica dei farmaci. Allo stesso modo, molti diversi alcheni trisostituiti partecipano senza problemi, inclusi quelli derivati da prodotti naturali e da molecole farmacologiche esistenti. Nella maggior parte dei casi, il processo fornisce le ammine desiderate con alte rese e con eccellente controllo sia dell’impronta speculare sia della disposizione relativa dei due centri stereogenici vicinali.
Indagare come il catalizzatore compie il suo lavoro
Per capire perché il metodo funzioni così bene, il gruppo ha svolto esperimenti meccanicistici. Studi di marcatura hanno mostrato che l’idruro nel complesso di nichel si addiziona in una posizione specifica sull’alchene in un singolo passaggio non reversibile, predisponendo i due centri stereogenici vicinali con geometria precisa. Test con potenziali trappole per radicali hanno suggerito che percorsi a radicali liberi sono improbabili. Al contrario, prove da spettrometria di massa ad alta risoluzione e un complesso di nichel caratterizzato cristallograficamente indicano un ciclo che transita tra specie nichel(II) e nichel(I). Un passaggio chiave sembra essere un trasferimento tra questi due stati di ossidazione (transmetalazione), che porta infine alla formazione del legame C–N che definisce il prodotto ammico.
Nuove possibilità per i farmaci futuri
In dimostrazioni pratiche, gli autori hanno applicato la loro strategia per modificare molecole avanzate di tipo farmaceutico e per costruire analoghi stereo‑definiti di medicinali esistenti che contengono il motivo N‑(2‑etilamino)ammide. Hanno inoltre mostrato che la reazione può essere scalata e che i prodotti risultanti possono essere ulteriormente trasformati senza perdere la stereochimica accuratamente impostata. Per i non specialisti, il messaggio chiave è che i chimici hanno ora un modo programmabile per impostare non solo una, ma tutte e quattro le possibili disposizioni 3D attorno a due centri chirali vicinali in strutture amminiche di valore. Questa capacità dovrebbe ampliare notevolmente il menu di molecole candidate per la scoperta di farmaci, permettendo un’esplorazione più sistematica delle relazioni forma‑attività e, in ultima analisi, terapie progettate meglio.
Citazione: Bai, H., Li, M., Wang, X. et al. Stereodivergent synthesis of chiral amines bearing vicinal stereocenters via hydroamination of trisubstituted alkenes. Nat Commun 17, 3431 (2026). https://doi.org/10.1038/s41467-026-70294-6
Parole chiave: ammine chirali, catalisi al nichel, idroaminazione, sintesi stereodivergente, scoperta di farmaci