Clear Sky Science · pl
Stereodivergentna synteza chiralnych aminów z sąsiednimi centrami stereogenicznymi przez hydroaminację alkenów trisubstytucyjnych
Dlaczego kształt cząsteczki ma znaczenie
Wiele współczesnych leków zawdzięcza swoje działanie drobnym różnicom w trójwymiarowym kształcie. Dwie cząsteczki zbudowane z tych samych atomów mogą zachowywać się jak lewa i prawa ręka: niemal identyczne, lecz jedna może leczyć, a druga szkodzić. W tym badaniu przedstawiono nowy sposób formowania takich kształtów w ważnej rodzinie związków — aminach, które występują powszechnie w lekach, produktach naturalnych i agrochemikaliach. Umożliwiając prostym, płaskim fragmentom przybieranie precyzyjnych układów 3D, praca otwiera bardziej niezawodną drogę do leków skuteczniejszych i bezpieczniejszych.
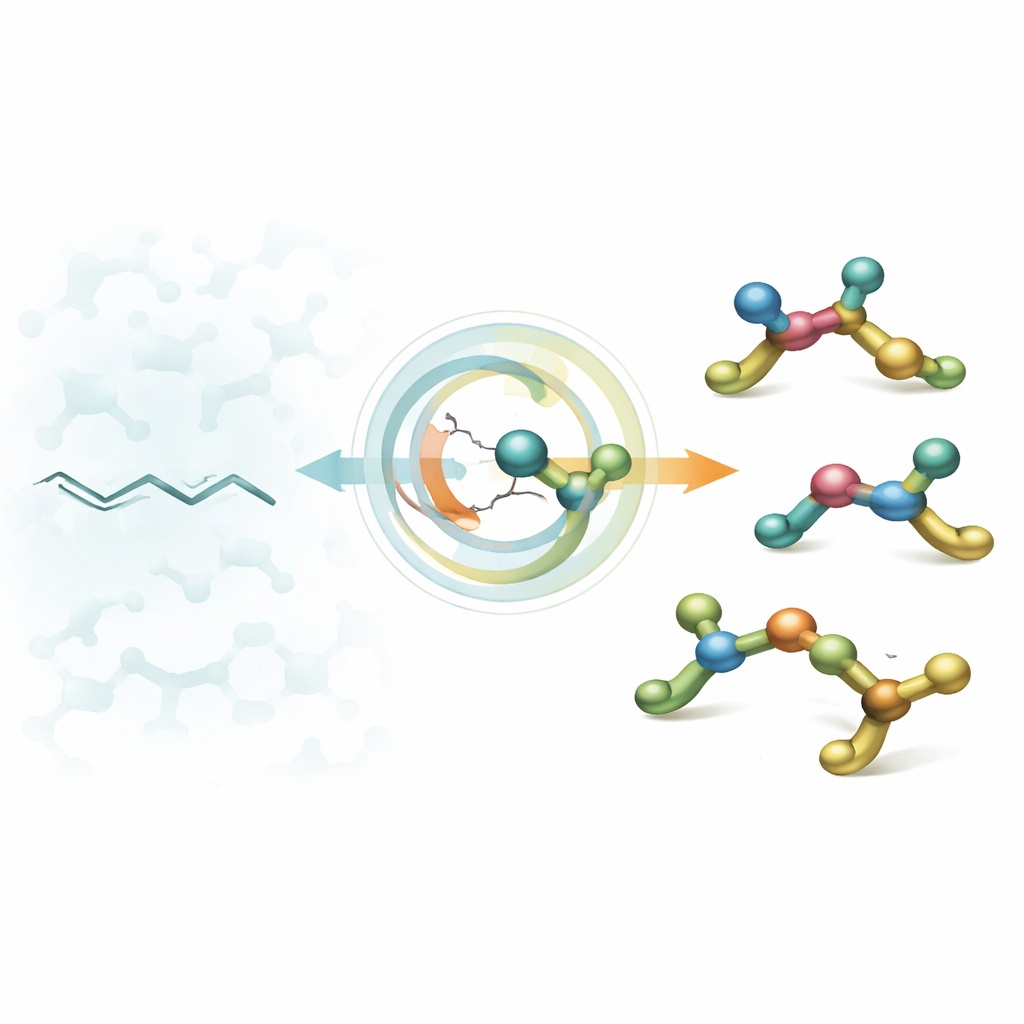
Od płaskich łańcuchów do bloków 3D
Projektanci leków często zaczynają od amin alifatycznych — małych fragmentów zawierających azot, które wpasowują się w biologiczne cele. Przez dziesięciolecia chemicy nauczyli się wytwarzać aminy z jednym „punktem skrętu” (centrum stereogenicznym), jednak prawdziwe leki często zawierają kilka takich punktów obok siebie. Te ciasno upakowane centra chiralne mogą znacząco poprawić dopasowanie cząsteczki do enzymu lub receptora, ale są wyjątkowo trudne do zbudowania w kontrolowany sposób. Istniejące metody zwykle faworyzują tylko jeden układ, pozbawiając chemików prostej i elastycznej strategii dostępu do wszystkich kształtów, które chcieliby przetestować.
Pojedyncza reakcja, która może iść w cztery strony
Autorzy rozwiązują ten problem, przekształcając łatwo dostępne alkeny trisubstytucyjne — w praktyce płaskie łańcuchy węgla z zatłoczonym wiązaniem podwójnym — w aminy 3D z dwoma sąsiednimi centrami stereogenicznymi. Kluczowy ruch to hydroaminacja katalizowana niklem: rodzaj niklowego hydridu najpierw addycjonuje do wiązania podwójnego, a następnie przyłącza się fragment aminowy, wszystko w starannie zaplanowanej sekwencji. Spryt polega na tym, że wynik zależy w przewidywalny sposób od zaledwie dwóch przełączników: czy wyjściowe wiązanie podwójne ma konfigurację E czy Z oraz czy chiralny ligand niklu jest w wersji R czy S. Przełączając te dwa ustawienia, ta sama konfiguracja reakcji może dostarczyć dowolny z czterech możliwych stereozomerów na żądanie.
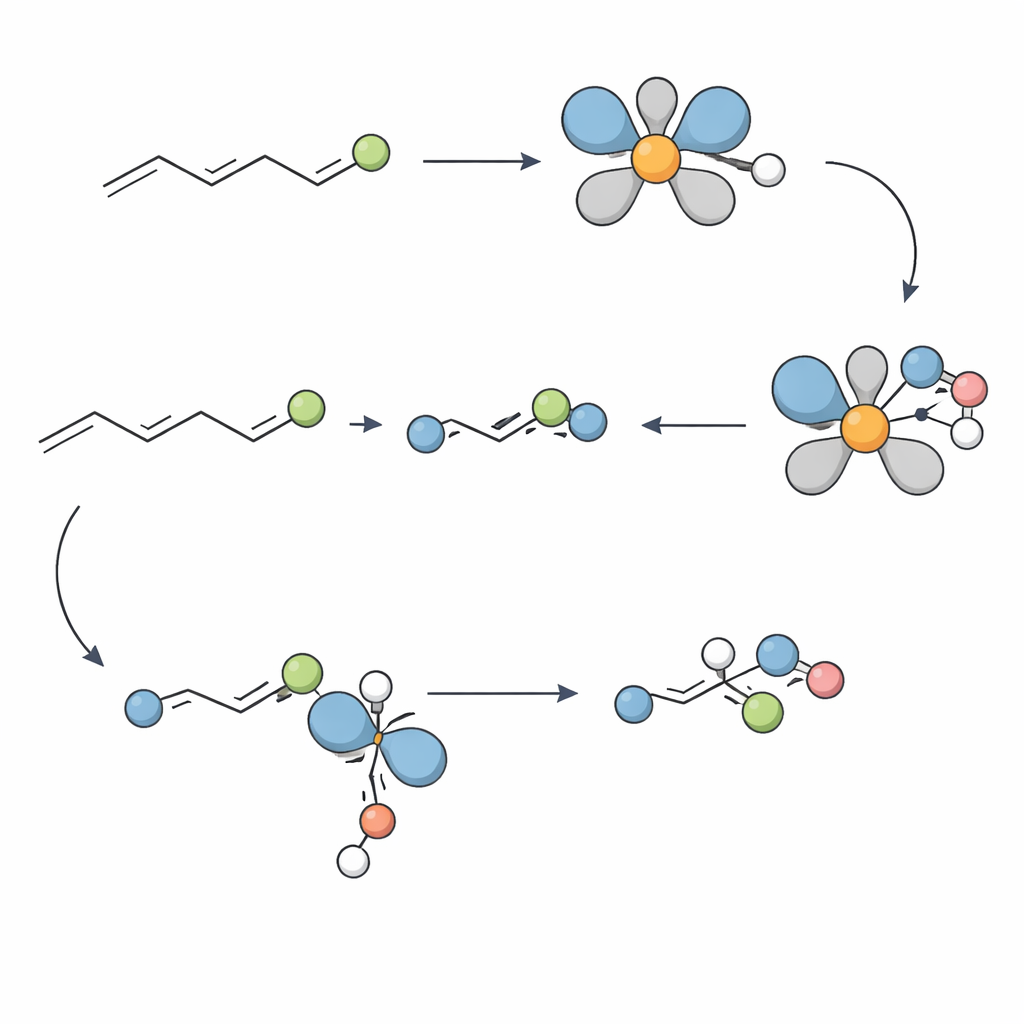
Zaplanowane dla rzeczywistych cząsteczek
Ponad konceptualnym postępem, chemia okazuje się odporna i praktyczna. Reakcja toleruje szerokie spektrum partnerów aminowych, od prostych amin wtórnych po bardziej podstawione warianty niosące estry, karbaminiany, sulfony, a nawet estry boranowe często wykorzystywane później w modyfikacjach leków. Podobnie wiele różnych alkenów trisubstytucyjnych reaguje gładko, w tym te pochodzące z produktów naturalnych i istniejących leków. W większości przypadków proces dostarcza pożądane aminy w wysokich wydajnościach i z doskonałą kontrolą zarówno nad tym, które lustrzane odbicie powstaje, jak i nad konfiguracją dwóch sąsiednich centrów stereogenicznych.
Badanie, jak katalizator wykonuje swoją pracę
Aby zrozumieć, dlaczego metoda działa tak dobrze, zespół przeprowadził eksperymenty mechanistyczne. Badania z użyciem znakowania wykazały, że hydrid w kompleksie niklu addycjonuje do określonej pozycji na alkenie w pojedynczym, nieodwracalnym kroku, ustanawiając dwa sąsiednie centra stereo z precyzyjną geometrią. Testy z potencjalnymi pułapkami rodnikowymi sugerowały, że ścieżki z wolnymi rodnikami są mało prawdopodobne. Zamiast tego dane z wysokorozdzielczej spektrometrii mas oraz skryształizowanego kompleksu niklowego wskazują na cykl przełączający się między gatunkami niklu(II) i niklu(I). Kluczowym etapem wydaje się przekazanie (transmetalcja) między tymi dwoma stanami utlenienia, które ostatecznie prowadzi do powstania wiązania C–N definiującego produkt aminowy.
Nowe możliwości dla przyszłych leków
W demonstracjach praktycznych autorzy zastosowali swoją strategię do modyfikacji zaawansowanych cząsteczek przypominających leki i do budowy stereo‑określonych analogów istniejących leków zawierających motyw N‑(2‑etylamino)amidu. Pokaźny został także potencjał skalowania reakcji oraz możliwość dalszych przekształceń produktów bez utraty starannie ustalonej stereochemii. Dla osób niebędących specjalistami kluczowy wniosek jest taki, że chemicy dysponują teraz programowalnym sposobem na ustawienie nie tylko jednego, lecz wszystkich czterech możliwych układów 3D wokół dwóch sąsiednich centrów chiralnych w wartościowych strukturach aminowych. Ta zdolność powinna znacznie rozszerzyć pulę kandydatów do odkrywania leków, umożliwiając bardziej systematyczne badanie zależności kształt–aktywność i w efekcie lepiej zaprojektowane terapie.
Cytowanie: Bai, H., Li, M., Wang, X. et al. Stereodivergent synthesis of chiral amines bearing vicinal stereocenters via hydroamination of trisubstituted alkenes. Nat Commun 17, 3431 (2026). https://doi.org/10.1038/s41467-026-70294-6
Słowa kluczowe: aminy chiralne, kataliza niklowa, hydroaminacja, synteza stereodivergentna, odkrywanie leków