Clear Sky Science · fr
Synthèse stéréodivergente d’amines chirales portant des stéréocentres vicinaux via hydroamination d’alcènes trisubstitués
Pourquoi la forme d’une molécule compte
De nombreux médicaments actuels tirent leur efficacité de minuscules différences de forme tridimensionnelle. Deux molécules composées des mêmes atomes peuvent se comporter comme une main gauche et une main droite : presque identiques, mais l’une peut soigner tandis que l’autre nuit. Cette étude présente une nouvelle façon de sculpter ces formes dans une famille clé de composés — les amines — présentes dans les médicaments, les produits naturels et les agrochimiques. En apprenant à des blocs de construction simples et plats à se replier en arrangements 3D précis, ce travail ouvre une voie plus fiable vers des médicaments à la fois plus efficaces et plus sûrs.
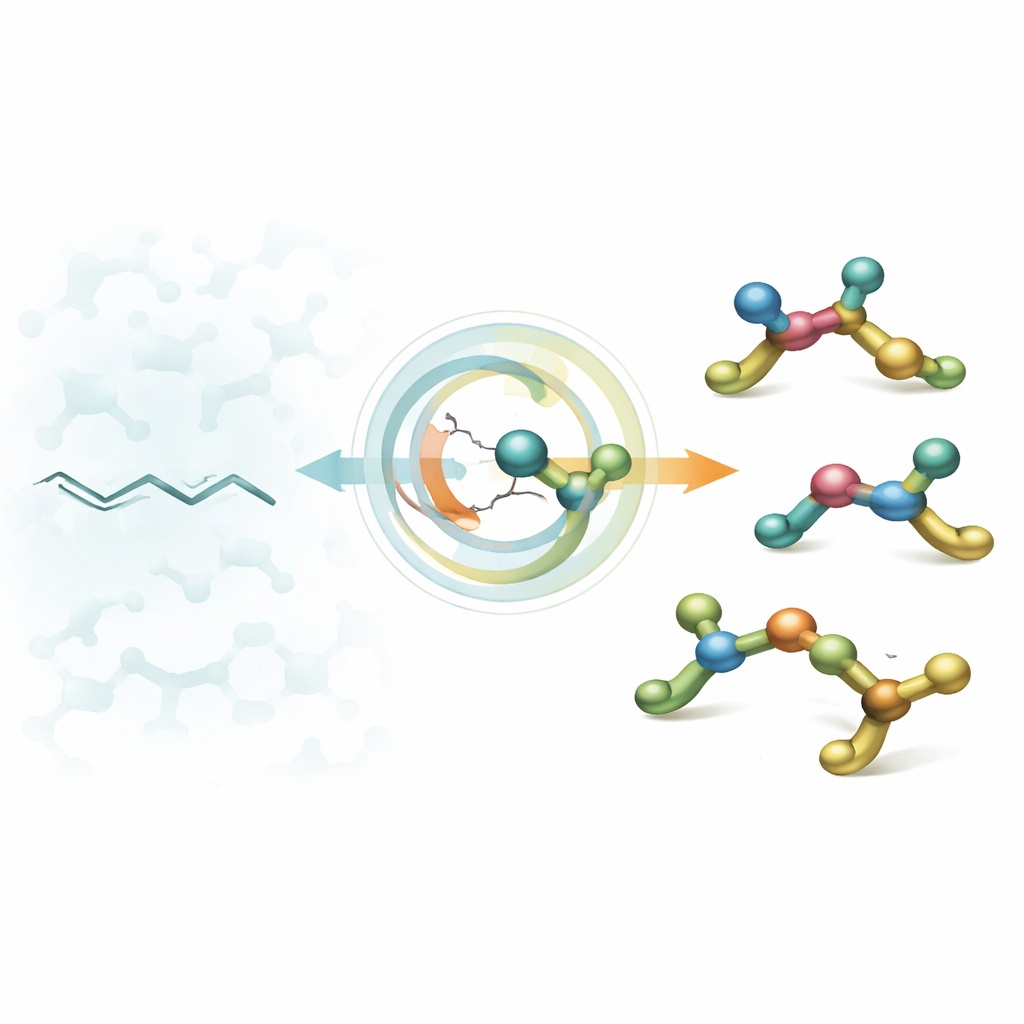
Des chaînes plates aux briques 3D
Les concepteurs de médicaments partent souvent d’amines aliphatiques — de petits fragments contenant de l’azote qui se lient aux cibles biologiques. Depuis des décennies, les chimistes maîtrisent la préparation d’amines portant un seul « point de torsion » (un centre stéréogénique), alors que les médicaments réels contiennent souvent plusieurs de ces centres côte à côte. Ces centres chiraux étroitement groupés peuvent améliorer fortement l’ajustement d’une molécule à une enzyme ou à un récepteur, mais ils sont notoirement difficiles à construire de manière contrôlée. Les méthodes existantes favorisent généralement un seul agencement, privant les chimistes d’une stratégie simple et flexible pour accéder à toutes les formes qu’ils souhaiteraient tester.
Une seule réaction qui peut viser quatre directions
Les auteurs s’attaquent à ce problème en convertissant des alcènes trisubstitués facilement accessibles — essentiellement des chaînes de carbone plates avec une double liaison encombrée — en amines 3D portant deux stéréocentres voisins. Leur étape clé est une hydroamination catalysée par le nickel : une espèce hydrure de nickel s’additionne d’abord sur la double liaison, puis un fragment amine est fixé, le tout dans une séquence soigneusement chorégraphiée. L’astuce consiste à ce que le résultat dépende de manière prévisible de seulement deux commutateurs : si la double liaison de départ est en configuration E ou Z, et si le ligand chiral du nickel est de configuration R ou S. En faisant varier ces deux paramètres, le même dispositif réactionnel peut fournir à la demande l’un des quatre stéréoisomères possibles.
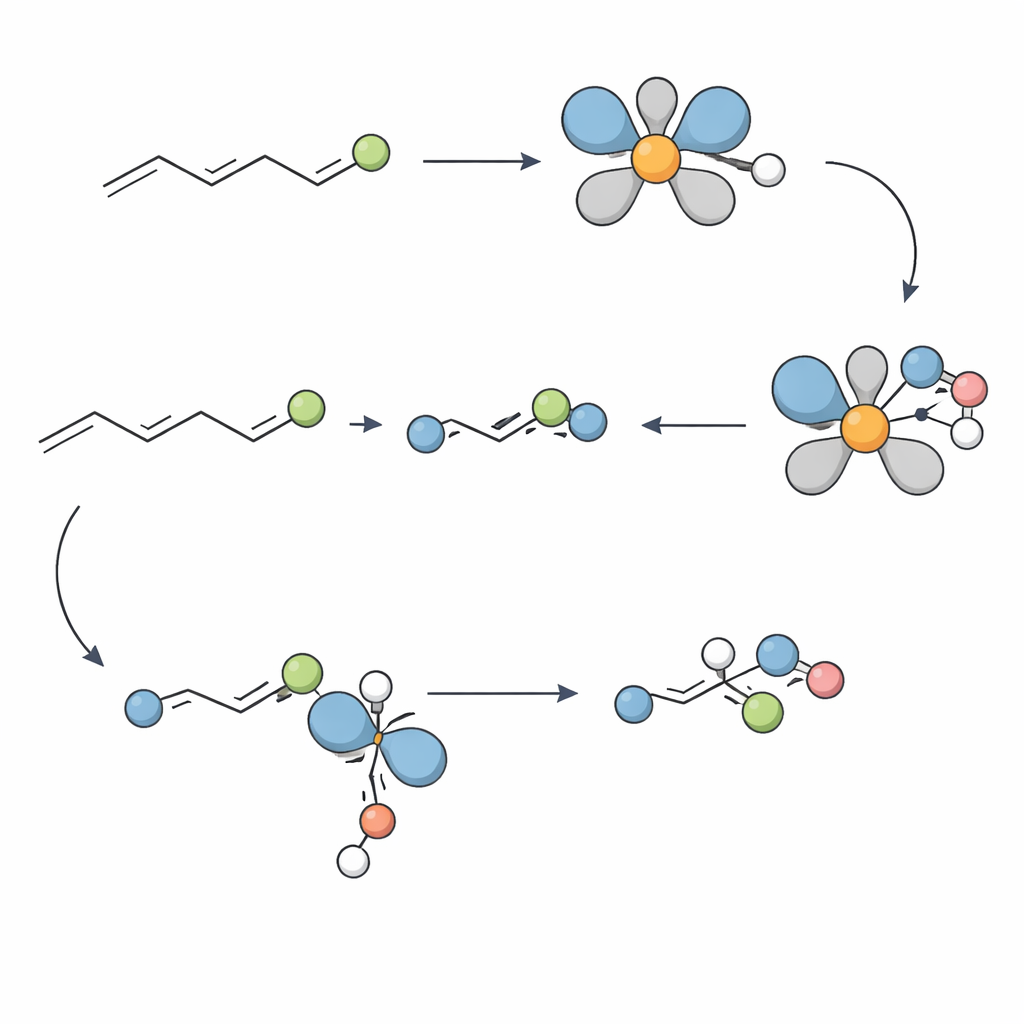
Conçu pour des molécules du monde réel
Au‑delà de l’avancée conceptuelle, la chimie s’avère robuste et pratique. La réaction tolère une large gamme de partenaires amines, depuis des amines secondaires simples jusqu’à des variantes plus substituées portant des esters, des carbamates, des sulfones et même des esters boroniques souvent utilisés ultérieurement dans la modification de médicaments. De même, de nombreux alcènes trisubstitués différents réagissent facilement, y compris ceux dérivés de produits naturels et de molécules médicamenteuses existantes. Dans la plupart des cas, le procédé fournit les amines souhaitées en bons rendements et avec un excellent contrôle à la fois de l’image miroir formée et de l’arrangement des deux stéréocentres voisins.
Explorer le fonctionnement du catalyseur
Pour comprendre pourquoi la méthode fonctionne si bien, l’équipe a réalisé des expériences mécanistiques. Des études de marquage ont montré que l’hydrure du complexe de nickel s’additionne en un point spécifique de l’alcène dans une étape unique et non réversible, installant les deux stéréocentres voisins avec une géométrie précise. Des tests avec des pièges à radicaux potentiels suggèrent que des voies radicalaires libres sont peu probables. À la place, des preuves issues de spectrométrie de masse haute résolution et d’un complexe de nickel caractérisé par cristallographie indiquent un cycle oscillant entre des espèces nickel(II) et nickel(I). Une étape clé semble être un transfert (transmétallation) entre ces deux états d’oxydation, qui conduit finalement à la formation de la liaison C–N définissant le produit amine.
Nouvelles possibilités pour les médicaments futurs
Dans des démonstrations pratiques, les auteurs ont appliqué leur stratégie pour modifier des molécules avancées de type médicament et pour construire des analogues stéréo‑définis de médicaments existants contenant un motif N‑(2‑éthylamino)amide. Ils ont également montré que la réaction peut être montée à l’échelle et que les produits obtenus peuvent être transformés davantage sans perdre leur stéréochimie soigneusement établie. Pour les non‑spécialistes, le message clé est que les chimistes disposent désormais d’un moyen programmable pour contrôler non pas une, mais les quatre dispositions 3D possibles autour de deux centres chiraux voisins dans des structures d’amines utiles. Cette capacité devrait largement élargir le catalogue de molécules candidates pour la découverte de médicaments, permettant une exploration plus systématique des relations forme‑activité et, finalement, la conception de thérapies mieux pensées.
Citation: Bai, H., Li, M., Wang, X. et al. Stereodivergent synthesis of chiral amines bearing vicinal stereocenters via hydroamination of trisubstituted alkenes. Nat Commun 17, 3431 (2026). https://doi.org/10.1038/s41467-026-70294-6
Mots-clés: amines chirales, catalyse au nickel, hydroamination, synthèse stéréodivergente, découverte de médicaments