Clear Sky Science · pt
Síntese estereodivergente de aminas quirais com centros estereogênicos vicinais via hidroaminação de alcenos trisubstituídos
Por que a forma de uma molécula importa
Muitos dos medicamentos atuais devem sua eficácia a pequenas diferenças na forma tridimensional. Duas moléculas feitas dos mesmos átomos podem comportar‑se como a mão esquerda e a mão direita: quase idênticas, mas uma pode curar enquanto a outra prejudica. Este estudo apresenta uma nova forma de esculpir essas formas em uma família chave de moléculas chamadas aminas, que aparecem em medicamentos, produtos naturais e agroquímicos. Ao ensinar blocos de construção simples e planos a se dobrarem em arranjos 3D precisos, o trabalho abre uma rota mais confiável para fármacos mais eficazes e seguros.
De cadeias planas a blocos de construção 3D
Projetistas de fármacos frequentemente partem de aminas alifáticas – pequenos fragmentos contendo nitrogênio que se encaixam em alvos biológicos. Por décadas, químicos se tornaram hábeis em produzir aminas com um único “ponto de torção” (um centro estereogênico), mas fármacos reais frequentemente contêm vários desses pontos lado a lado. Esses centros quirais compactos podem melhorar dramaticamente como uma molécula se ajusta a uma enzima ou receptor, mas são notoriamente difíceis de construir de forma controlada. Métodos existentes normalmente favorecem apenas um arranjo, deixando os químicos sem uma estratégia simples e flexível para acessar todas as formas que gostariam de testar.
Uma única reação que pode mirar em quatro direções
Os autores enfrentam esse problema convertendo alcenos trisubstituídos prontamente disponíveis – essencialmente cadeias de carbono planas com uma dupla ligação congestionada – em aminas 3D com dois centros estereogênicos vizinhos. A jogada-chave é uma hidroaminação catalisada por níquel: uma espécie hidreto de níquel adiciona primeiro através da dupla ligação, depois um fragmento amina é ligado, tudo em uma sequência cuidadosamente coreografada. A sacada é que o resultado depende de forma previsível de apenas dois controles: se a dupla ligação inicial está na configuração E ou Z, e se o ligante quiral do níquel está na versão R ou S. Ao alternar essas duas configurações, o mesmo conjunto reacional pode fornecer qualquer um dos quatro estereoisômeros possíveis sob demanda.
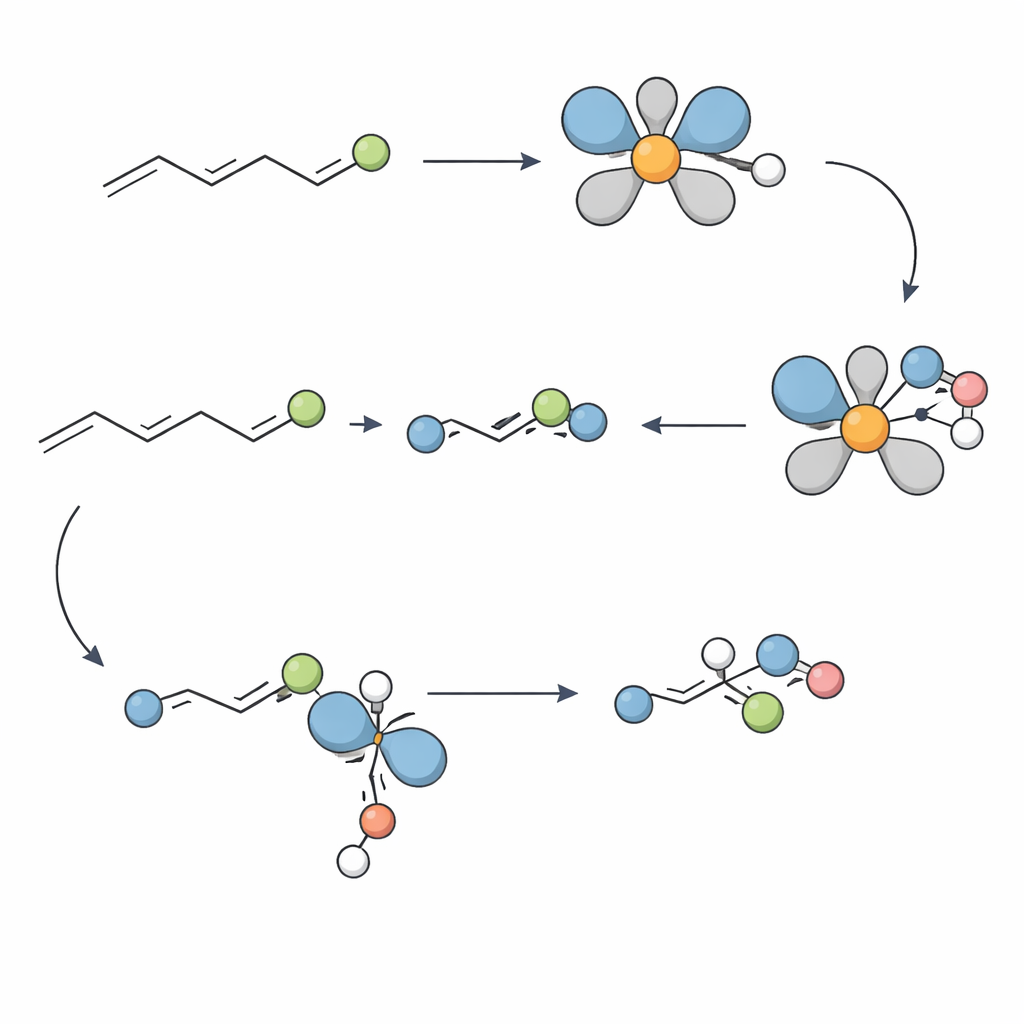
Projetado para moléculas do mundo real
Além do avanço conceitual, a química mostra‑se robusta e prática. A reação tolera uma ampla gama de parceiros amina, desde aminas secundárias simples até variantes mais substituídas que carregam ésteres, carbamatos, sulfones e até ésteres de boro frequentemente usados em modificações posteriores de fármacos. Do mesmo modo, muitos alcenos trisubstituídos diferentes participam de forma suave, incluindo aqueles derivados de produtos naturais e moléculas farmacêuticas existentes. Na maioria dos casos, o processo fornece as aminas desejadas em altos rendimentos e com excelente controle tanto de qual imagem especular é formada quanto de como os dois centros estereogênicos vizinhos estão arranjados.
Investigando como o catalisador faz seu trabalho
Para entender por que o método funciona tão bem, a equipe realizou experimentos mecanísticos. Estudos de marcação mostraram que o hidreto no complexo de níquel adiciona‑se a uma posição específica do alceno em um único passo não reversível, estabelecendo os dois centros estereogênicos vizinhos com geometria precisa. Testes com possíveis armadilhas de radicais sugeriram que vias por radicais livres são improváveis. Em vez disso, evidências de espectrometria de massa de alta resolução e de um complexo de níquel caracterizado por cristalografia apontam para um ciclo que alterna entre espécies níquel(II) e níquel(I). Um passo-chave parece ser uma transferência (transmetalação) entre esses dois estados de oxidação, que finalmente leva à formação da ligação C–N que define o produto amina.
Novas possibilidades para futuros medicamentos
Em demonstrações práticas, os autores aplicaram sua estratégia para modificar moléculas avançadas do tipo fármaco e para construir análogos estereodefinidos de medicamentos existentes que contêm o motivo N‑(2‑etilamino)amida. Eles também mostraram que a reação pode ser ampliada e que os produtos resultantes podem ser transformados adicionalmente sem perder a estereoquímica cuidadosamente definida. Para não especialistas, a mensagem principal é que os químicos agora dispõem de uma forma programável de ajustar não apenas uma, mas todas as quatro disposições 3D possíveis em torno de dois centros quirais vizinhos em estruturas valiosas de aminas. Essa capacidade deve ampliar muito o cardápio de moléculas candidatas para descoberta de fármacos, permitindo uma exploração mais sistemática das relações forma–atividade e, em última instância, terapias melhor projetadas.
Citação: Bai, H., Li, M., Wang, X. et al. Stereodivergent synthesis of chiral amines bearing vicinal stereocenters via hydroamination of trisubstituted alkenes. Nat Commun 17, 3431 (2026). https://doi.org/10.1038/s41467-026-70294-6
Palavras-chave: aminas quirais, catálise com níquel, hidroaminação, síntese estereodivergente, descoberta de fármacos