Clear Sky Science · es
Síntesis estereodivergente de aminas quirales con centros estereogénicos vecinales mediante hidroaminación de alquenos trisustituidos
Por qué importa la forma de una molécula
Muchos de los medicamentos actuales deben su potencia a pequeñas diferencias en la forma tridimensional. Dos moléculas compuestas por los mismos átomos pueden comportarse como la mano izquierda y la derecha: casi idénticas, pero una puede curar mientras que la otra perjudica. Este estudio presenta una nueva manera de esculpir esas formas en una familia clave de compuestos, las aminas, que abundan en fármacos, productos naturales y agroquímicos. Al enseñar a bloques de construcción simples y planos a plegarse en disposiciones 3D precisas, el trabajo abre una vía más fiable para obtener medicamentos más efectivos y seguros.
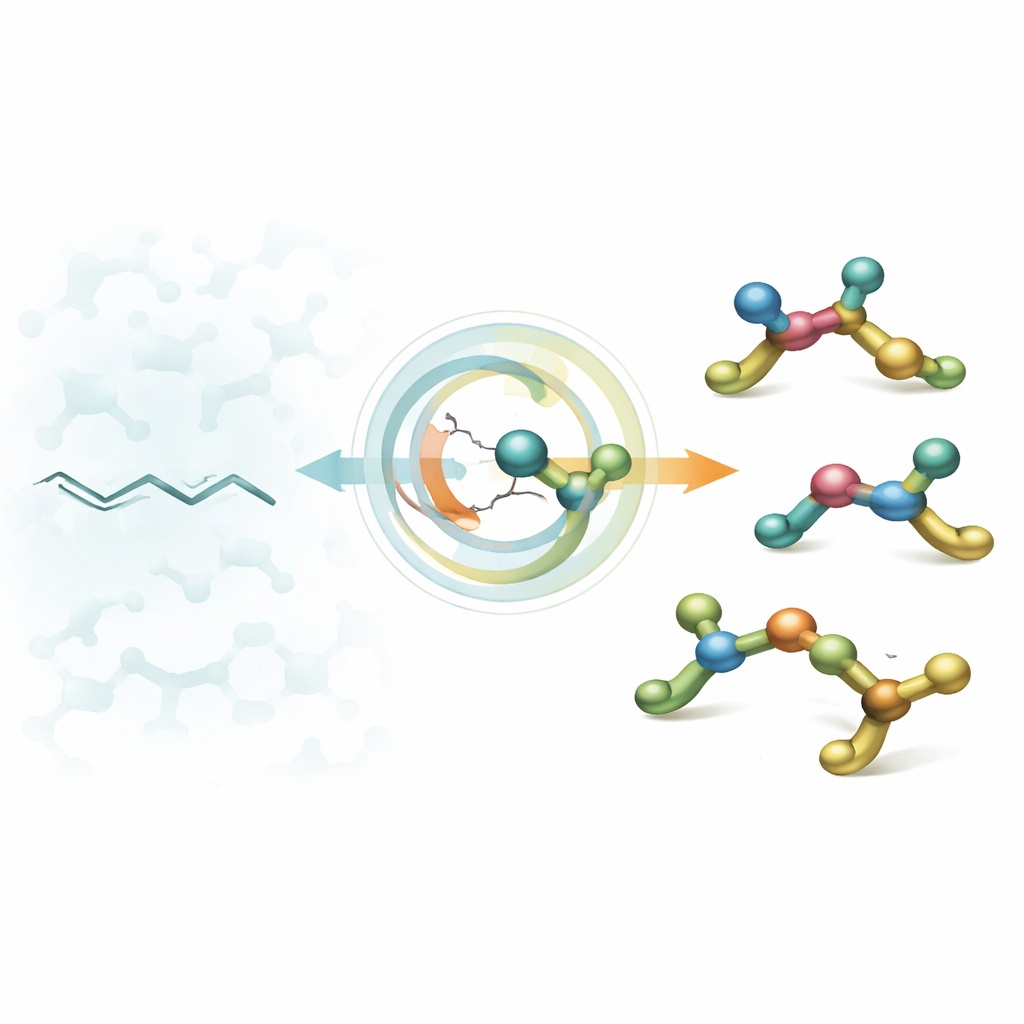
De cadenas planas a bloques de construcción 3D
Los diseñadores de fármacos suelen partir de aminas alifáticas: pequeños fragmentos que contienen nitrógeno que encajan en dianas biológicas. Durante décadas, los químicos han perfeccionado la síntesis de aminas con un único «punto de torsión» (un centro estereogénico), pero los fármacos reales con frecuencia contienen varios de estos puntos adyacentes. Estos centros quirales compactos pueden mejorar drásticamente cómo encaja una molécula en una enzima o receptor, pero son notoriamente difíciles de construir de forma controlada. Los métodos existentes suelen favorecer una sola disposición, dejando a los químicos sin una estrategia sencilla y flexible para acceder a todas las formas que podrían querer probar.
Una sola reacción que puede apuntar en cuatro direcciones
Los autores abordan este problema convirtiendo alquenos trisustituidos de fácil acceso —esencialmente cadenas de carbono planas con un doble enlace congestionado— en aminas 3D que poseen dos centros estereogénicos vecinos. Su movimiento clave es una hidroaminación catalizada por níquel: una especie hidruro de níquel primero se añade al doble enlace y luego se incorpora el fragmento amina, todo en una secuencia cuidadosamente coreografiada. El giro ingenioso es que el resultado depende de forma predecible de solo dos conmutadores: si el doble enlace inicial está en la disposición E o Z, y si el ligando quiral del níquel es la versión R o S. Al invertir estas dos opciones, la misma configuración de reacción puede entregar cualquiera de los cuatro estereoisómeros posibles a la carta.
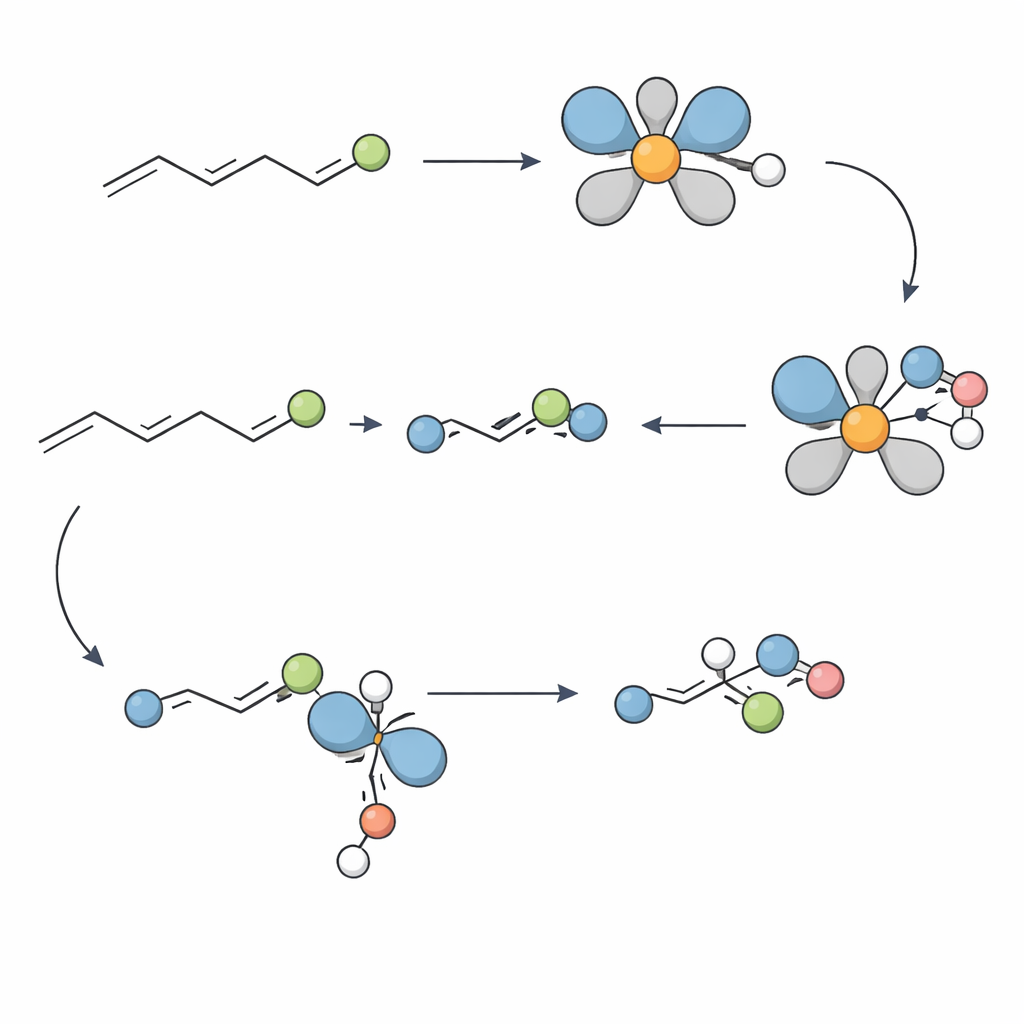
Diseñado para moléculas reales
Más allá del avance conceptual, la química demuestra ser robusta y práctica. La reacción tolera una amplia gama de socios amínicos, desde aminas secundarias simples hasta variantes más sustituidas que llevan ésteres, carbamatos, sulfona y hasta ésteres borónicos usados frecuentemente en modificaciones posteriores de fármacos. Del mismo modo, muchos alquenos trisustituidos diferentes participan con fluidez, incluidos aquellos derivados de productos naturales y moléculas farmacológicas ya existentes. En la mayoría de los casos, el proceso entrega las aminas deseadas en altos rendimientos y con un excelente control tanto sobre qué imagen especular se forma como sobre la disposición de los dos centros estereogénicos vecinos.
Investigando cómo actúa el catalizador
Para entender por qué el método funciona tan bien, el equipo realizó experimentos mecanísticos. Estudios de etiquetado mostraron que el hidruro en el complejo de níquel se añade a una posición específica del alqueno en un único paso no reversible, estableciendo los dos centros estereógenos vecinos con geometría precisa. Ensayos con posibles trampas de radicales sugirieron que las vías por radicales libres son improbables. En su lugar, la evidencia procedente de espectrometría de masas de alta resolución y de un complejo de níquel caracterizado cristalográficamente apunta a un ciclo que oscila entre especies de níquel(II) y níquel(I). Un paso clave parece ser una transferencia (transmetalación) entre estos dos estados de oxidación, que finalmente conduce a la formación del enlace C–N que define el producto amínico.
Nuevas posibilidades para futuros medicamentos
En demostraciones prácticas, los autores aplicaron su estrategia para modificar moléculas avanzadas con afinidad farmacológica y para construir análogos estereodefinidos de medicamentos existentes que contienen el motivo N‑(2‑etilamino)amida. También mostraron que la reacción puede escalarse y que los productos obtenidos pueden transformarse adicionalmente sin perder la estereoquímica cuidadosamente establecida. Para los no especialistas, el mensaje clave es que los químicos disponen ahora de una forma programable de sintonizar no solo una, sino las cuatro disposiciones 3D posibles alrededor de dos centros quirales adyacentes en valiosas estructuras amínicas. Esta capacidad debería ampliar considerablemente el menú de moléculas candidatas para el descubrimiento de fármacos, permitiendo una exploración más sistemática de las relaciones forma–actividad y, en última instancia, terapias mejor diseñadas.
Cita: Bai, H., Li, M., Wang, X. et al. Stereodivergent synthesis of chiral amines bearing vicinal stereocenters via hydroamination of trisubstituted alkenes. Nat Commun 17, 3431 (2026). https://doi.org/10.1038/s41467-026-70294-6
Palabras clave: aminas quirales, catálisis con níquel, hidroaminación, síntesis estereodivergente, descubrimiento de fármacos