Clear Sky Science · zh
有丝分裂微同源介导的断裂诱导复制促进染色体合成异常
当染色体失控时
癌症和某些先天缺陷常常在我们的染色体以极端方式混乱时出现:DNA 段被复制、翻转并拼接成古怪的拼贴。本文提出了一个具有重大医学意义的基本问题:这种混乱如何在一次性跃变中发生,而不是经过多年逐步累积?通过细致观察受损的染色体末端,作者发现了一种高度易错的修复过程,能够在一次事件中重写长片段基因组。
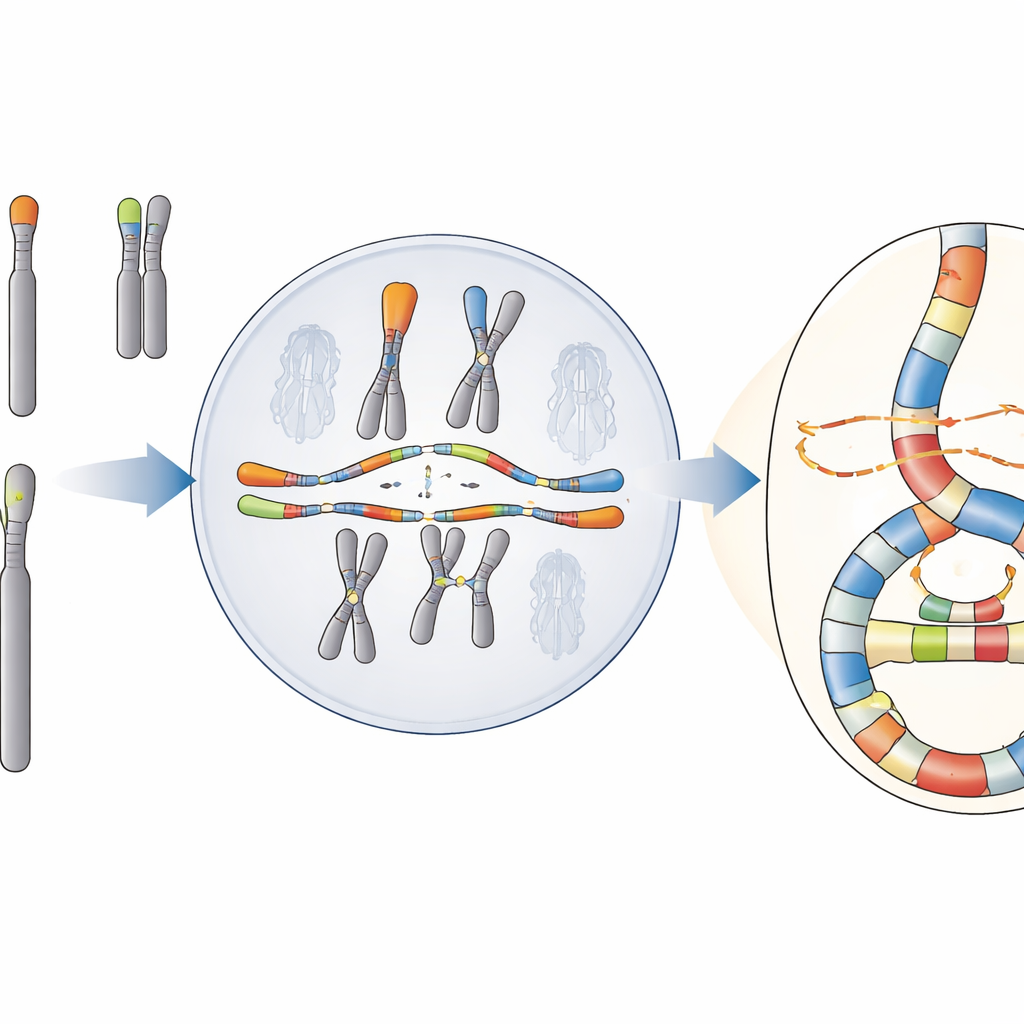
表面混乱下的隐含模式
研究团队聚焦于一种称为染色体合成异常(chromoanasynthesis)的现象,其中 DNA 片段被复制并多次重新插入,形成密集的重排簇和基因的额外拷贝。与另一种著名灾变——染色体碎裂(chromothripsis,表面像随机重粘碎裂的 DNA)不同,染色体合成异常带有反复复制 DNA 并在模板间切换的指纹。这些事件在癌症及某些罕见发育障碍中常见,但在人体细胞中其起源难以确定,因为标准测序常常无法捕捉重排区域的全部复杂性。
读取超长 DNA 分子
为了解决这一问题,作者构建了一种针对融合染色体末端(端粒)专门设计的单分子长读长测序方法,称为 Fusion-seq Long-Read(FSLR)。他们研究了被推入“端粒危机”的人类成纤维细胞——一种染色体末端变得危险性缩短的状态——并在癌细胞系中使用工程化分子剪刀在端粒内侧切割 DNA。长读长测序使他们能够从头到尾追踪每条融合的 DNA 分子,不仅揭示了两个端粒相遇的位置,还显示了夹在中间的每一个额外片段以及这些片段来自基因组的何处。
一种诱变性的复制粘贴修复通路
他们发现的融合分子令人惊讶地复杂。有些包含数十甚至上百个来自多个染色体的插入片段,并且存在频繁被重复复制的“热点”。片段之间的连接处常常共享少数匹配的碱基,这是“微同源”配对而非干净教科书式修复的特征。模式强烈指向一种称为微同源介导断裂诱导复制(microhomology-mediated break-induced replication,MM-BIR)的复制粘贴机制。在这一过程中,断裂的 DNA 末端短暂与另一条 DNA 分子上的短匹配序列配对,开始复制,然后脱离并附着到另一个模板上,留下重复和重排的片段序列。遗传学和药物学实验表明,这一路径依赖于通常与小片段末端连接相关的酶与能够复制长片段 DNA 的更强复制机器的协作。
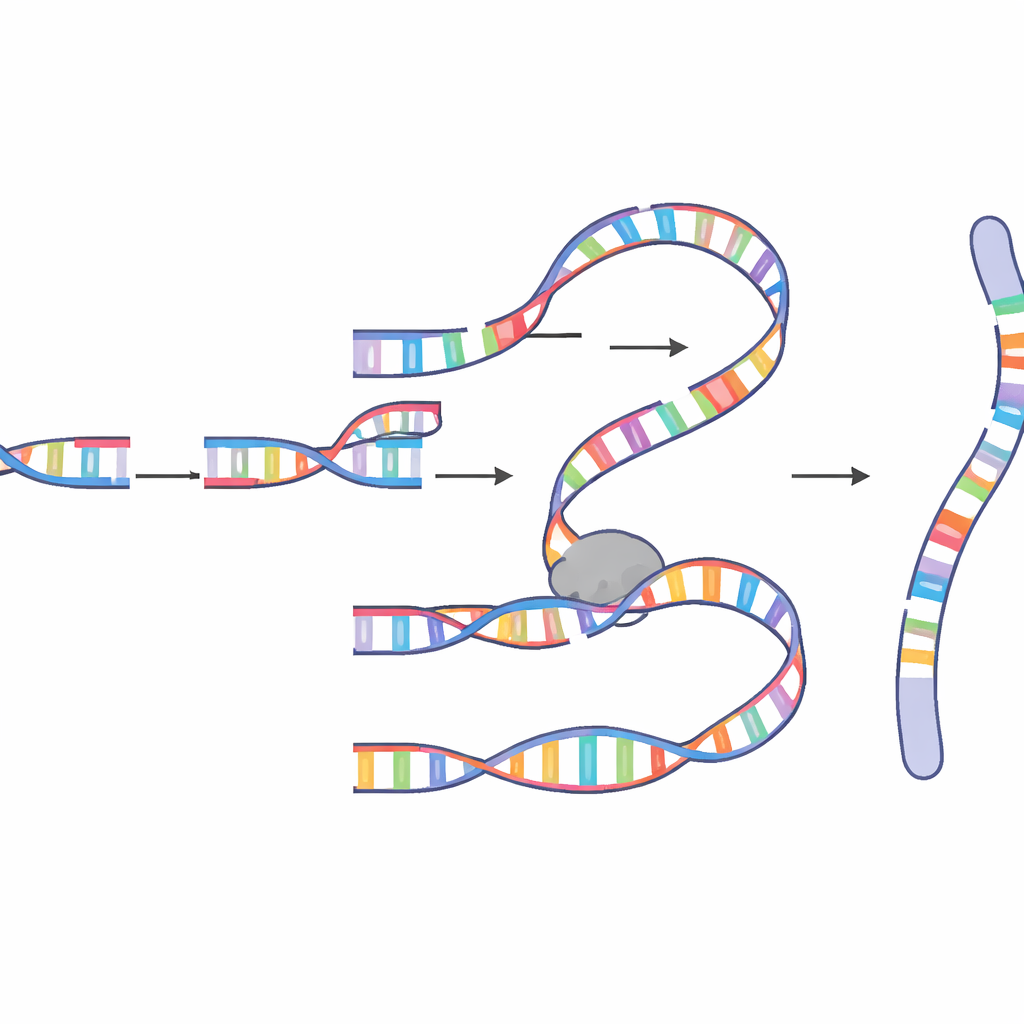
为何有丝分裂是危险时刻
一个关键的令人惊讶的发现是时间性。该系统中的染色体合成异常特异地发生在有丝分裂期间——细胞分裂且染色体高度凝缩的短暂窗口。作者表明,当细胞的 G2/M 损伤检查点——阻止带有断裂 DNA 进入有丝分裂的主要防护机制——被削弱时,复杂事件的发生频率大幅增加。他们还证明了一种称为 θ 型聚合酶(polymerase theta)的酶,作为“最后防线”式的修复因子,发挥了核心作用,帮助断裂末端找到微小的匹配序列并启动合成。随后更具过程性的酶如 δ 型聚合酶延伸新合成的 DNA,并由 PIF1、POLD3 和 PCNA 等因子帮助维持复制机器的运行。当这些辅助因子被改变时,插入 DNA 的长度和模式发生变化,证实染色体合成异常是由有丝分裂特异性的 MM-BIR 驱动,而非简单的断裂片段连接。
对癌症和先天缺陷的新线索
总体而言,这项工作揭示了一条在断裂染色体末端遇到有丝分裂时启动的高度诱变的“应急修复”通路。与其温和地恢复原始序列,有丝分裂 MM-BIR 能在一次事件中快速扩增并重混基因组区域,包括基因富集区和潜在的致癌基因。对健康细胞来说,这是一种有风险但有时不可避免的完成复制和分裂的方式。但是对于癌前细胞而言,它可能正提供了驱动侵袭性肿瘤生长或导致先天疾病中观察到的复杂染色体变化所需的那种基因组动荡。通过在分子水平上描绘该过程,这项研究为理解 — 也许将来针对 — 导致某些严重人类疾病的灾难性基因组重组提供了新途径。
引用: Ngo, G.H.P., Cleal, K., Seifan, S. et al. Mitotic microhomology-mediated break-induced replication promotes chromoanasynthesis. Nat Commun 17, 3375 (2026). https://doi.org/10.1038/s41467-026-70086-y
关键词: 染色体重排, 端粒危机, DNA 修复, 基因组不稳定性, 癌症遗传学