Clear Sky Science · fr
La réplication induite par cassure médiée par microhomologie en mitose favorise la chromoanasynthèse
Quand les chromosomes partent en vrille
Le cancer et certains troubles congénitaux surviennent souvent lorsque nos chromosomes sont chamboulés de manière extrême : des segments d'ADN sont dupliqués, inversés et recousus en patchworks étranges. Cet article pose une question fondamentale aux lourdes implications médicales : comment un tel chaos peut‑il se produire en une seule étape, plutôt qu'au fil des années ? En observant de près les extrémités chromosomiques endommagées, les auteurs mettent au jour un mécanisme de réparation très sujet aux erreurs capable de réécrire de larges portions du génome d'un seul coup.
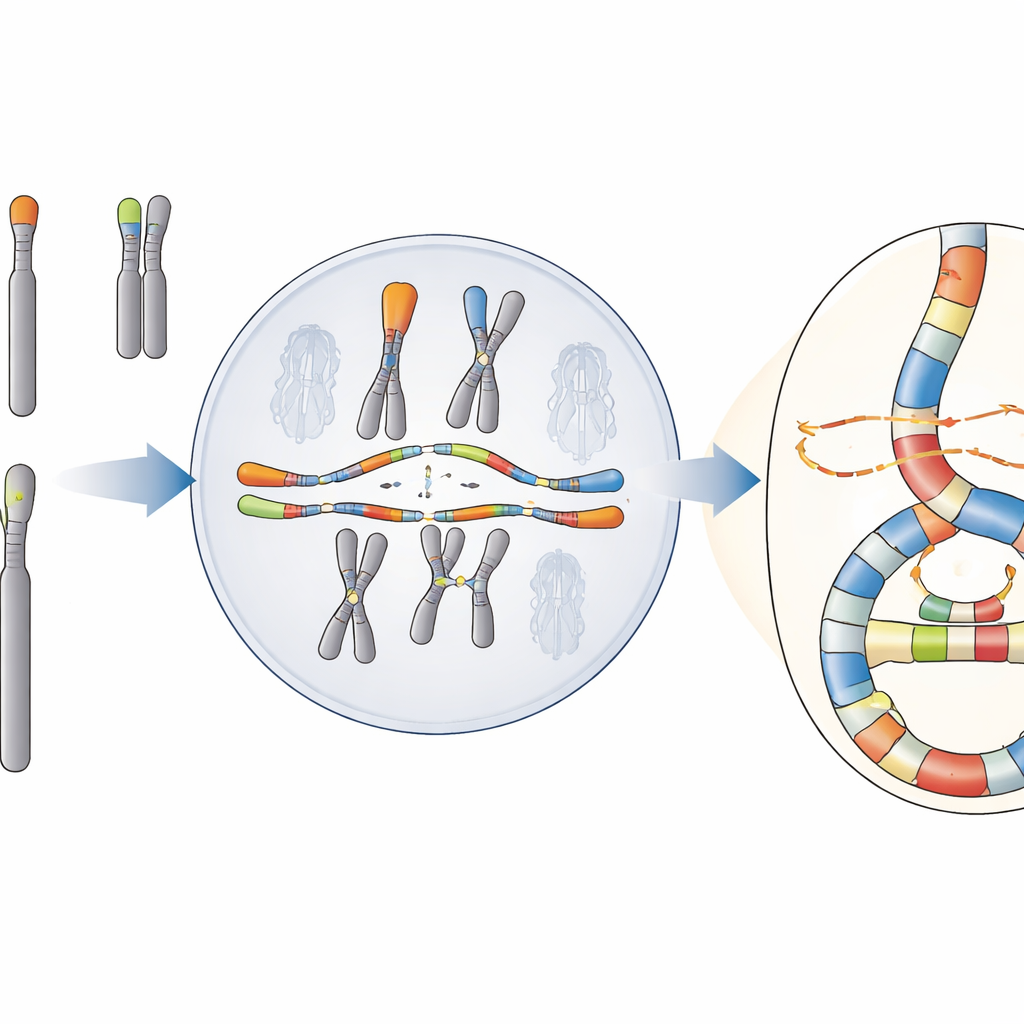
Une catastrophe avec un motif caché
L'équipe se concentre sur un phénomène appelé chromoanasynthèse, au cours duquel des morceaux d'ADN sont copiés et réinsérés plusieurs fois, créant des grappes denses de réarrangements et des copies supplémentaires de gènes. Contrairement à une autre catastrophe bien connue, la chromothripsis, qui ressemble à un recollage aléatoire d'ADN brisé, la chromoanasynthèse porte l'empreinte de copies répétées et de commutations entre modèles. Ces événements sont courants dans les cancers et dans certains troubles développementaux rares, mais leurs origines dans les cellules humaines ont été difficiles à établir parce que le séquençage standard manque souvent la pleine complexité des régions réassemblées.
Lire des molécules d'ADN ultra‑longues
Pour aborder ce problème, les auteurs ont développé une méthode de séquençage longue lecture sur molécule unique, Fusion‑seq Long‑Read (FSLR), spécifiquement destinée aux extrémités chromosomiques, ou télomères, qui se sont fusionnées. Ils ont étudié des fibroblastes humains poussés en « crise des télomères », un état où les bouts des chromosomes deviennent dangereusement courts, et ont aussi utilisé des ciseaux moléculaires conçus pour couper l'ADN juste à l'intérieur des télomères dans des lignées cellulaires cancéreuses. Le séquençage longue lecture leur a permis de suivre chaque molécule d'ADN fusionnée de bout en bout, révélant non seulement où se rejoignaient les deux télomères, mais aussi chaque fragment supplémentaire coincé entre eux et l'origine génomique de ces fragments.
Une voie de réparation mutagène de type copier‑coller
Les molécules fusionnées qu'ils ont mises au jour étaient étonnamment complexes. Certaines contenaient des dizaines, voire plus d'une centaine, de fragments insérés provenant de nombreux chromosomes, avec des « points chauds » fréquents qui avaient été copiés à plusieurs reprises. Les jonctions entre fragments partageaient souvent quelques bases identiques, signature d'un appariement basé sur la « microhomologie » plutôt que d'une réparation propre et classique. Les schémas pointaient fortement vers un mécanisme de copie‑collage connu sous le nom de réplication induite par cassure médiée par microhomologie (MM‑BIR). Dans ce processus, une extrémité d'ADN rompue s'apparie brièvement avec une courte séquence correspondante sur une autre molécule d'ADN, commence à copier, puis se détache pour s'accrocher à un autre modèle, laissant derrière elle une traînée de segments dupliqués et réarrangés. Des expériences génétiques et pharmacologiques ont montré que cette voie dépend d'une collaboration entre des enzymes habituellement associées à une jonction de petites tailles et une machinerie de réplication plus puissante capable de copier de longs segments d'ADN.
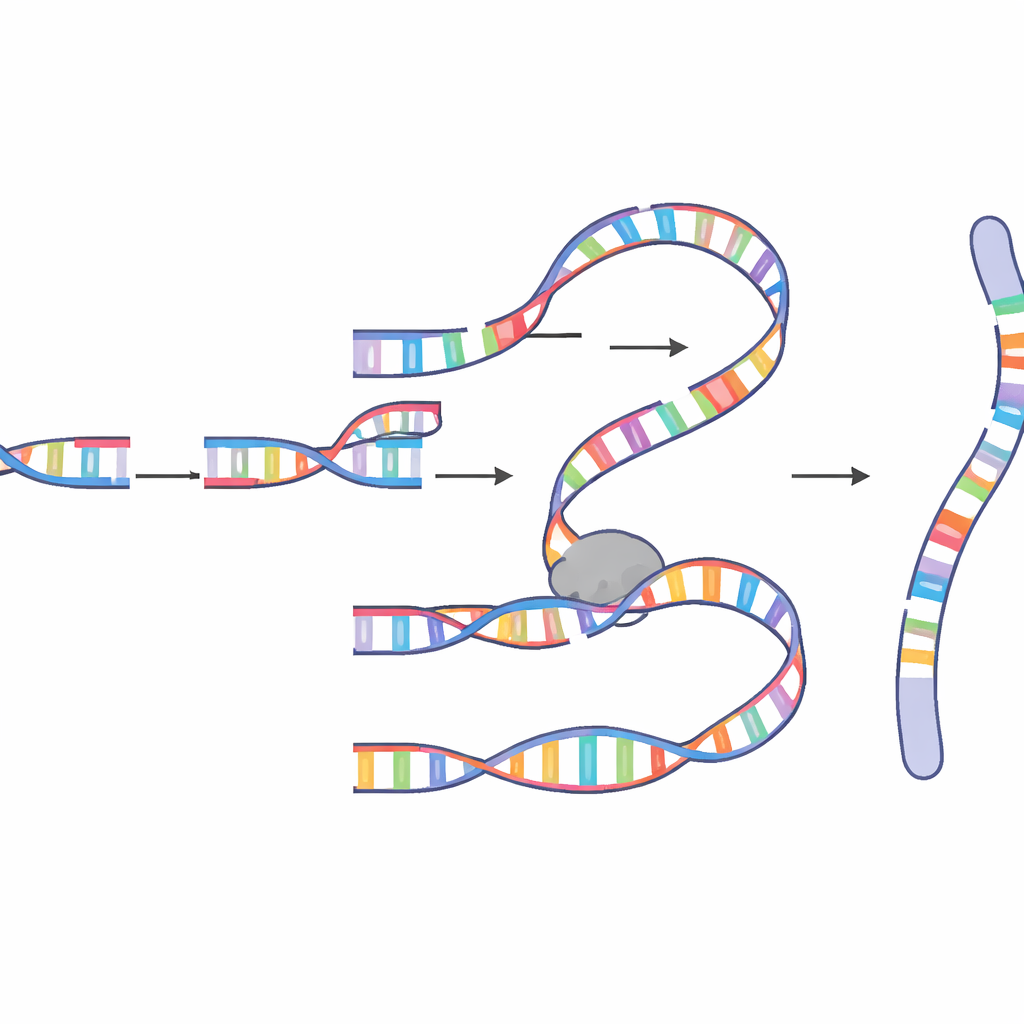
Pourquoi la mitose est un moment dangereux
Une surprise clé fut le moment où cela se produit. La chromoanasynthèse dans ce système survenait spécifiquement pendant la mitose, la brève période où les cellules se divisent et les chromosomes sont fortement condensés. Les auteurs ont montré que lorsque le point de contrôle des dommages G2/M — la principale garde‑fou qui empêche l'entrée en mitose en présence d'ADN cassé — était affaibli, les événements complexes devenaient beaucoup plus fréquents. Ils ont également démontré qu'une enzyme appelée polymérase theta, connue comme un facteur de réparation « du dernier recours », joue un rôle central en aidant les extrémités rompues à trouver de petites séquences appariées et à initier la synthèse. Des polymérases plus processives, comme la polymérase delta, étendent ensuite le nouvel ADN, aidées par des facteurs tels que PIF1, POLD3 et PCNA qui maintiennent la machinerie de réplication en mouvement. Lorsque ces auxiliaires étaient altérés, la longueur et le schéma de l'ADN inséré changeaient, confirmant que la chromoanasynthèse est entraînée par une version mitotique spécialisée de la MM‑BIR plutôt que par une simple ligature de fragments cassés.
Nouveaux indices sur le cancer et les malformations congénitales
Dans l'ensemble, le travail révèle une voie de « réparation d'urgence » hautement mutagène qui se déclenche lorsque des extrémités chromosomiques cassées rencontrent la mitose. Plutôt que de restaurer doucement la séquence d'origine, la MM‑BIR mitotique peut amplifier et remixer rapidement des régions du génome, y compris des zones riches en gènes et des oncogènes potentiels, en un seul événement. Pour une cellule saine, c'est une stratégie risquée mais parfois inévitable pour achever la réplication et la division. Pour une cellule précancéreuse, en revanche, cela peut fournir exactement le type de bouleversement génomique qui favorise la croissance tumorale agressive ou contribue aux changements chromosomiques complexes observés dans les troubles congénitaux. En cartographiant ce processus au niveau moléculaire, l'étude ouvre la voie à de nouvelles façons de comprendre — et peut‑être un jour de cibler — le remaniement catastrophique du génome qui sous‑tend certaines des maladies humaines les plus difficiles.
Citation: Ngo, G.H.P., Cleal, K., Seifan, S. et al. Mitotic microhomology-mediated break-induced replication promotes chromoanasynthesis. Nat Commun 17, 3375 (2026). https://doi.org/10.1038/s41467-026-70086-y
Mots-clés: réarrangements chromosomiques, crise des télomères, réparation de l'ADN, instabilité génomique, génétique du cancer