Clear Sky Science · nl
Mitotische microhomologie-gemedieerde break-induced replication bevordert chromoanasynthese
Als chromosomen ontsporen
Kanker en sommige aangeboren afwijkingen ontstaan vaak wanneer onze chromosomen op extreme wijze worden dooreen gehaald: stukken DNA worden gekopieerd, omgedraaid en aan elkaar genaaid tot bizarre lapwerken. Deze studie stelt een fundamentele vraag met grote medische gevolgen: hoe ontstaat dergelijke chaos in één enkele sprong, in plaats van stukje bij beetje over vele jaren? Door nauwkeurig te kijken naar beschadigde chromosomeinden onthullen de auteurs een zeer foutgevoelig herstelproces dat lange stukken van het genoom in één keer kan herschrijven.
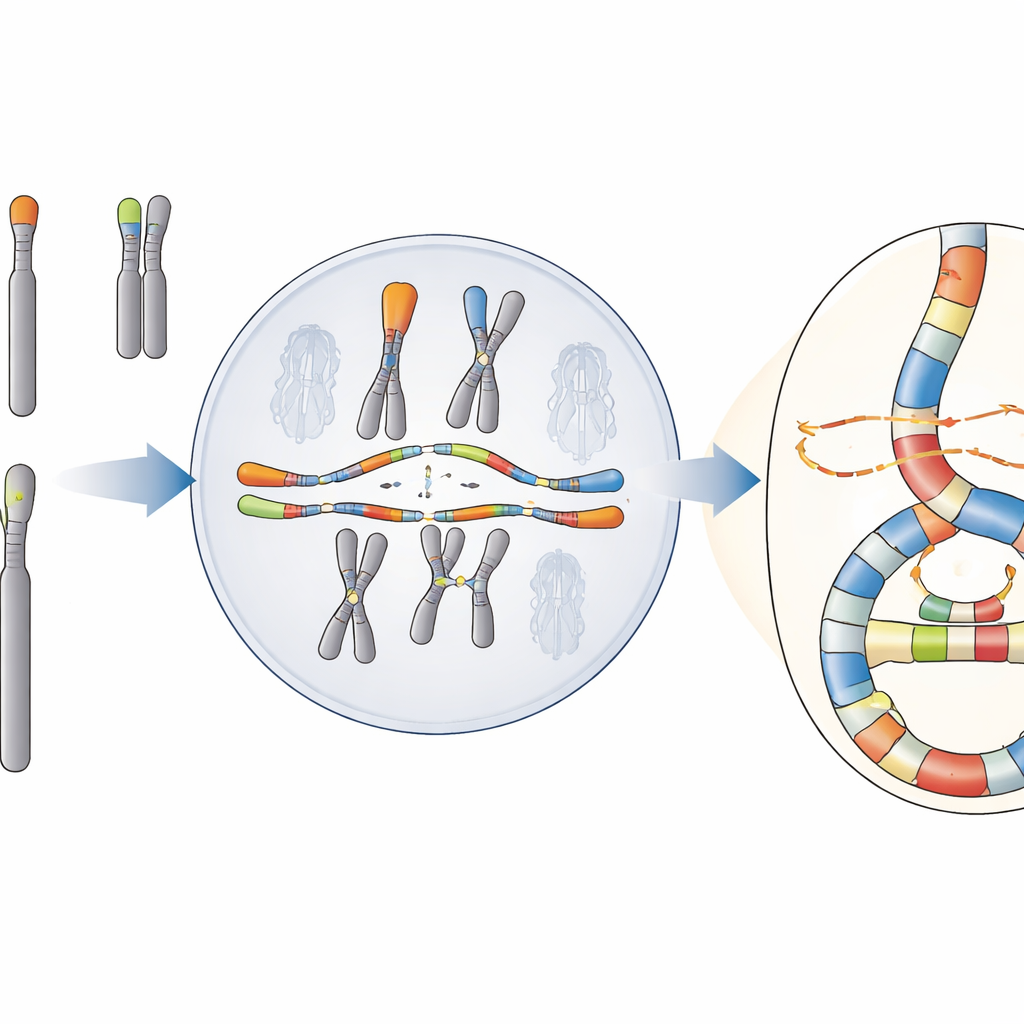
Een catastrofe met een verborgen patroon
Het team concentreert zich op een verschijnsel dat chromoanasynthese wordt genoemd, waarbij DNA-fragmenten worden gekopieerd en meerdere keren opnieuw ingebracht, waardoor dicht opeengepakte herschikkingen en extra kopieën van genen ontstaan. In tegenstelling tot een andere bekende catastrofe, chromothripsis, die lijkt op het willekeurig opnieuw lijmen van verbrijzeld DNA, draagt chromoanasynthese het keurmerk van herhaalde DNA-kopieën en wisselingen tussen templates. Deze gebeurtenissen komen vaak voor in tumoren en in sommige zeldzame ontwikkelingsstoornissen, maar hun oorsprong in menselijke cellen is moeilijk te achterhalen omdat standaardsequencing vaak niet de volledige complexiteit van de herschikte regio’s vangt.
Ultra-lange DNA-moleculen lezen
Om dit aan te pakken ontwikkelden de auteurs een single-molecule long-read sequencingsmethode, Fusion-seq Long-Read (FSLR), specifiek gericht op chromosomeinden, of telomeren, die aan elkaar zijn gefuseerd. Ze bestudeerden menselijke fibroblasten die in een “telomeercrisis” werden geduwd, een toestand waarin chromosomeinden gevaarlijk kort worden, en gebruikten ook aangebrachte moleculaire scharen om DNA net binnen de telomeren door te knippen in kankercellijnen. Long-read sequencing stelde hen in staat elk gefuseerd DNA-molecuul van het ene uiteinde tot het andere te volgen, waardoor niet alleen duidelijk werd waar de twee telomeren elkaar raakten maar ook elk extra fragment dat ertussen was geklemd en waar in het genoom die fragmenten vandaan kwamen.
Een mutageen copy-and-paste-herstelpad
De gefuseerde moleculen die ze ontdekten waren verbazingwekkend complex. Sommige bevatten tientallen of zelfs meer dan honderd ingevoegde fragmenten afkomstig van vele chromosomen, met frequente “hotspots” die herhaaldelijk waren gekopieerd. De verbanden tussen fragmenten deelden vaak een paar overeenkomende basen, een kenmerk van op microhomologie gebaseerde koppeling in plaats van netjes, tekstboekachtig herstel. De patronen wezen sterk op een copy-and-paste-mechanisme bekend als microhomology-mediated break-induced replication (MM-BIR). In dit proces paart een gebroken DNA-einde kort met een korte overeenkomende sequentie op een ander DNA-molecuul, begint te kopiëren, laat vervolgens los en haakt zich vast aan weer een ander template, waarbij een spoor van gedupliceerde en herschikte segmenten achterblijft. Genetische en medicamenteuze experimenten toonden aan dat dit pad afhankelijk is van een samenwerking tussen enzymen die normaal geassocieerd worden met klein-patch end joining en een krachtiger replicatiemechanisme dat lange DNA-stukken kan kopiëren.
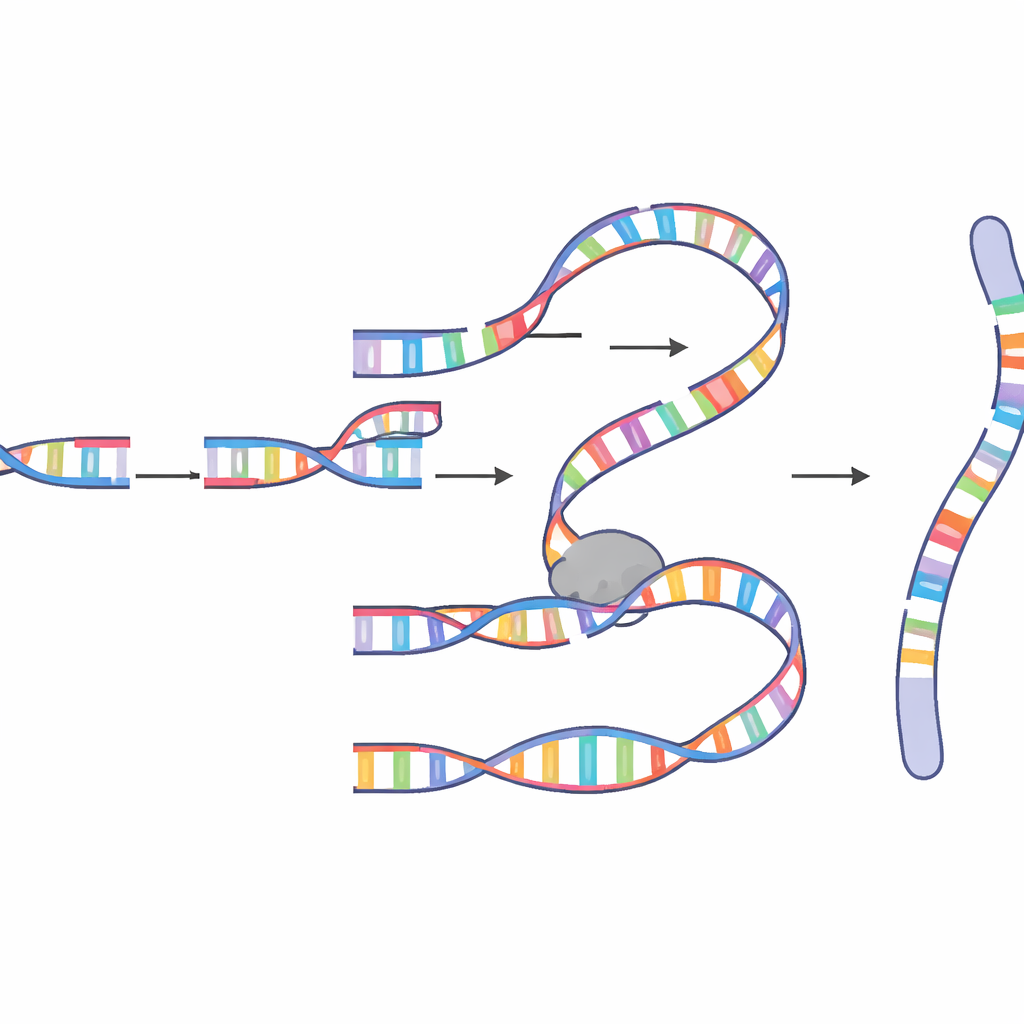
Waarom mitose een gevaarlijk moment is
Een belangrijke verrassing was de timing. Chromoanasynthese in dit systeem trad specifiek op tijdens de mitose, het korte venster waarin cellen zich delen en chromosomen sterk gecondenseerd zijn. De auteurs toonden aan dat wanneer de G2/M-schadecheckpoint van de cel—de belangrijkste schildwacht die de toegang tot mitose blokkeert bij gebroken DNA—verzwakt was, complexe gebeurtenissen veel frequenter werden. Ze toonden ook aan dat een enzym dat polymerase theta wordt genoemd, bekend als een “laatste redmiddel”-herstelfactor, een centrale rol speelt door gebroken uiteinden te helpen kleine overeenkomende sequenties te vinden en synthese te initiëren. Meer processieve enzymen zoals polymerase delta verlengen vervolgens het nieuwe DNA, geholpen door factoren zoals PIF1, POLD3 en PCNA die de replicatiemachinerie draaiende houden. Wanneer deze helpers werden veranderd, veranderden de lengte en het patroon van het ingevoegde DNA, wat bevestigt dat chromoanasynthese wordt aangedreven door een gespecialiseerde, mitotische variant van MM-BIR in plaats van door eenvoudige lijking van gebroken fragmenten.
Nieuwe aanwijzingen voor kanker en aangeboren afwijkingen
Alles bij elkaar onthult het werk een sterk mutageen “noodherstel”-pad dat in gang wordt gezet wanneer gebroken chromosomeinden mitose tegenkomen. In plaats van de oorspronkelijke sequentie voorzichtig te herstellen, kan mitotische MM-BIR snel genomische regio’s amplificeren en remixen, inclusief genrijke gebieden en potentiële oncogenen, in één enkele gebeurtenis. Voor een gezonde cel is dit een risicovolle maar soms onvermijdelijke manier om replicatie en deling af te ronden. Voor een precancereuze cel kan het echter precies het soort genomische omwenteling bieden dat agressieve tumorgroei aandrijft of bijdraagt aan complexe chromosomale veranderingen die bij aangeboren aandoeningen worden gezien. Door dit proces op moleculair niveau in kaart te brengen, wijst de studie op nieuwe manieren om de catastrofale genoomherschikking die ten grondslag ligt aan sommige van de meest hardnekkige menselijke ziekten te begrijpen—en mogelijk op termijn aan te pakken.
Bronvermelding: Ngo, G.H.P., Cleal, K., Seifan, S. et al. Mitotic microhomology-mediated break-induced replication promotes chromoanasynthesis. Nat Commun 17, 3375 (2026). https://doi.org/10.1038/s41467-026-70086-y
Trefwoorden: chromosomale herschikkingen, telomeercrisis, DNA-herstel, genoominstabiliteit, kankergenetica