Clear Sky Science · es
La replicación por rotura inducida mediada por microhomología en mitosis promueve la entroposíntesis cromosómica
Cuando los cromosomas se descontrolan
El cáncer y algunos defectos congénitos suelen surgir cuando nuestros cromosomas se reordenan de formas extremas: tramos de ADN se duplican, se invierten y se cosen en mosaicos extraños. Este artículo plantea una pregunta básica con grandes implicaciones médicas: ¿cómo ocurre tal caos de un solo golpe, en lugar de ocurrir poco a poco durante muchos años? Al observar de cerca los extremos cromosómicos dañados, los autores descubren un proceso de reparación muy propenso a errores que puede reescribir largas porciones del genoma de una sola vez.
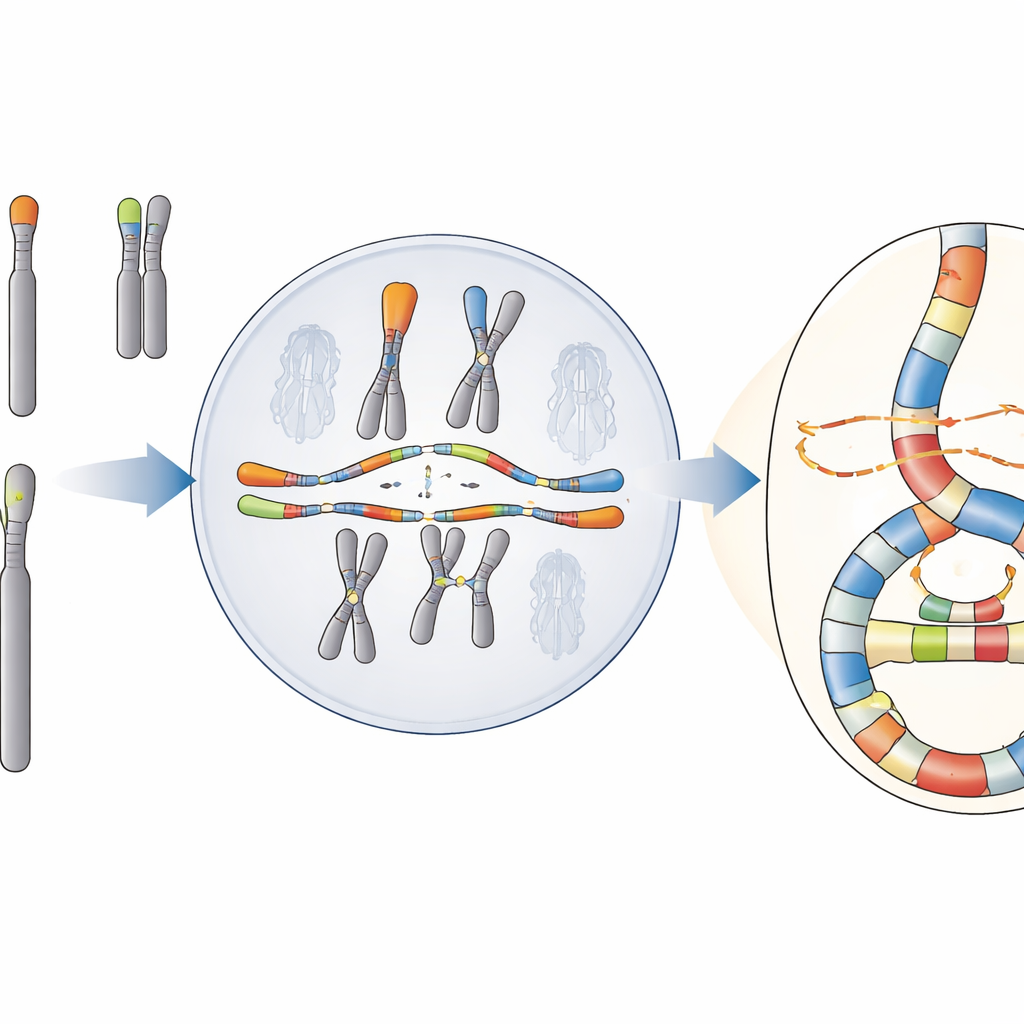
Una catástrofe con un patrón oculto
El equipo se centra en un fenómeno denominado entroposíntesis cromosómica (chromoanasynthesis), en el que fragmentos de ADN se copian y se reinsertan varias veces, creando densos racimos de reordenamientos y copias extra de genes. A diferencia de otra catástrofe bien conocida, la cromotripsis, que parece una re‑pegación aleatoria de ADN hecho añicos, la entroposíntesis muestra la huella de copias repetidas y cambios de plantilla durante la replicación. Estos eventos son frecuentes en cánceres y en algunos trastornos del desarrollo raros, pero sus orígenes en células humanas han sido difíciles de determinar porque las técnicas de secuenciación estándar a menudo no captan la complejidad completa de las regiones reordenadas.
Leer moléculas de ADN ultra‑largas
Para abordar esto, los autores desarrollaron un método de secuenciación de lectura larga de molécula única, Fusion‑seq Long‑Read (FSLR), dirigido específicamente a los extremos cromosómicos, o telómeros, que se han fusionado. Estudiaron fibroblastos humanos llevados a una “crisis de telómeros”, un estado en el que los extremos cromosómicos se vuelven peligrosamente cortos, y también usaron tijeras moleculares diseñadas para cortar el ADN justo dentro de los telómeros en líneas celulares de cáncer. La secuenciación de lectura larga les permitió seguir cada molécula de ADN fusionada de extremo a extremo, revelando no solo dónde se encontraban los dos telómeros, sino también cada fragmento extra intercalado y de qué lugar del genoma procedían esos fragmentos.
Una vía de reparación mutagénica de copiar‑y‑pegar
Las moléculas fusionadas que describieron eran asombrosamente complejas. Algunas contenían docenas o incluso más de un centenar de fragmentos insertados procedentes de muchos cromosomas, con “puntos calientes” frecuentes que se habían copiado repetidamente. Las uniones entre fragmentos a menudo compartían unas pocas bases coincidentes, sello característico de un emparejamiento basado en “microhomología” en lugar de una reparación limpia y de libro de texto. Los patrones apuntaban con fuerza a un mecanismo de copiar‑y‑pegar conocido como replicación por rotura inducida mediada por microhomología (MM‑BIR). En este proceso, un extremo de ADN roto se empareja brevemente con una secuencia coincidente corta en otra molécula de ADN, comienza a copiarse, luego se desprende y se acopla a otra plantilla, dejando tras de sí una estela de segmentos duplicados y reordenados. Experimentos genéticos y con fármacos mostraron que esta vía depende de la colaboración entre enzimas normalmente asociadas con la unión de extremos de pequeño parche y una máquina de replicación más potente que puede copiar tramos largos de ADN.
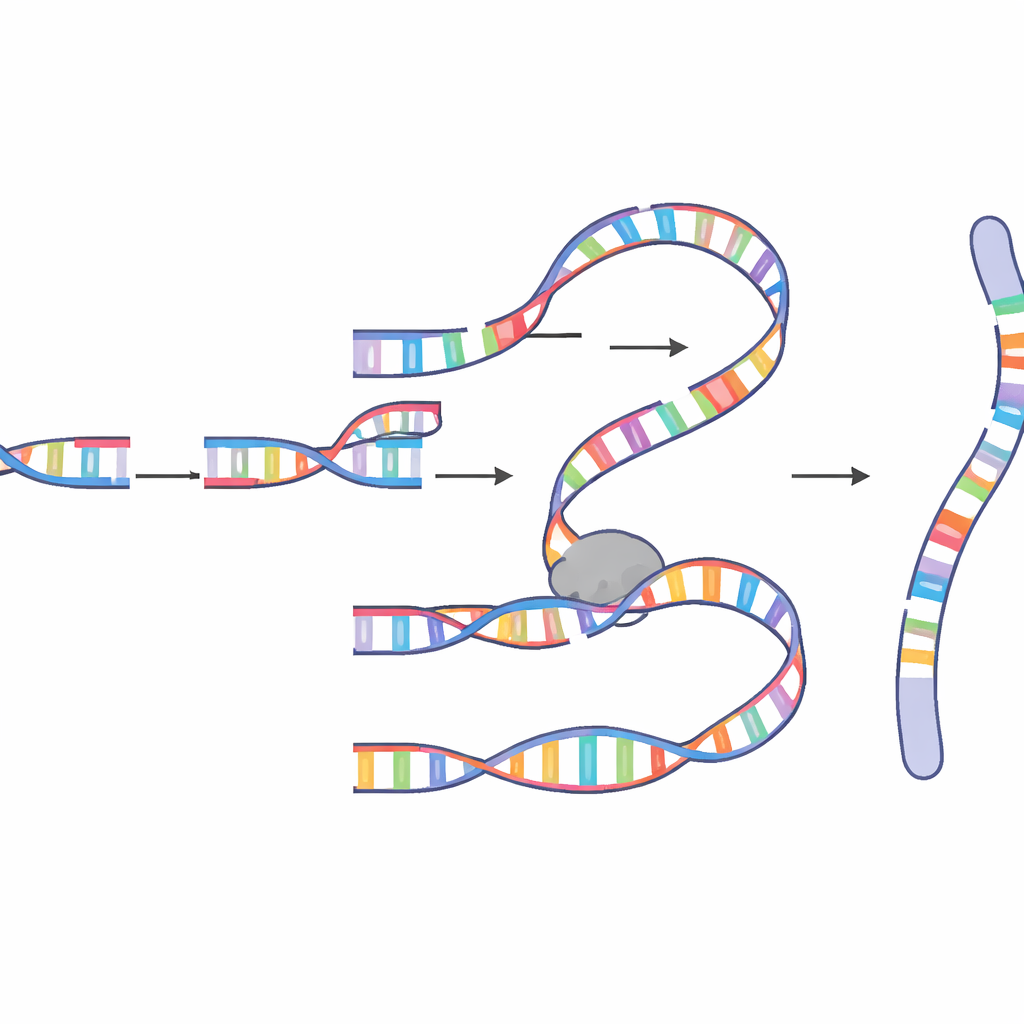
Por qué la mitosis es un momento peligroso
Una sorpresa clave fue el momento. La entroposíntesis en este sistema surgió específicamente durante la mitosis, la breve ventana en la que las células se dividen y los cromosomas están altamente condensados. Los autores demostraron que cuando el punto de control de daño G2/M de la célula —su principal salvaguarda que impide la entrada en mitosis con ADN roto— se debilitaba, los eventos complejos se volvían mucho más frecuentes. También mostraron que una enzima llamada polimerasa theta, conocida como un factor de reparación «del último recurso», desempeña un papel central, ayudando a los extremos rotos a encontrar pequeñas secuencias coincidentes e iniciar la síntesis. Enzimas más procesivas, como la polimerasa delta, extienden luego el nuevo ADN, ayudadas por factores como PIF1, POLD3 y PCNA que mantienen la maquinaria de replicación en marcha. Cuando estos auxiliares se alteraron, la longitud y el patrón del ADN insertado cambiaron, confirmando que la entroposíntesis es impulsada por una versión mitótica especializada de MM‑BIR en lugar de por una simple ligación de fragmentos rotos.
Nuevas pistas sobre cáncer y defectos congénitos
En conjunto, el trabajo revela una vía de «reparación de emergencia» altamente mutagénica que se activa cuando extremos cromosómicos rotos se encuentran con la mitosis. En lugar de restaurar suavemente la secuencia original, la MM‑BIR mitótica puede amplificar y remezclar rápidamente regiones genómicas, incluidas áreas ricas en genes y posibles oncogenes, en un solo evento. Para una célula sana, esto es un camino arriesgado pero a veces inevitable para completar la replicación y la división. Para una célula precancerosa, sin embargo, puede proporcionar exactamente el tipo de convulsión genómica que impulsa el crecimiento tumoral agresivo o contribuye a los cambios cromosómicos complejos observados en trastornos congénitos. Al mapear este proceso en detalle molecular, el estudio apunta a nuevas formas de comprender —y quizás algún día dirigir— la reestructuración catastrófica del genoma que subyace a algunas de las enfermedades humanas más difíciles.
Cita: Ngo, G.H.P., Cleal, K., Seifan, S. et al. Mitotic microhomology-mediated break-induced replication promotes chromoanasynthesis. Nat Commun 17, 3375 (2026). https://doi.org/10.1038/s41467-026-70086-y
Palabras clave: reordenamientos cromosómicos, crisis de telómeros, reparación del ADN, inestabilidad genómica, genética del cáncer