Clear Sky Science · it
La replicazione indotta da rotture mediata da microomologia mitotica promuove la chromoanasintesi
Quando i cromosomi impazziscono
Il cancro e alcuni difetti congeniti spesso insorgono quando i nostri cromosomi vengono rimescolati in modi estremi: tratti di DNA vengono duplicati, capovolti e ricuciti insieme in mosaici bizzarri. Questo articolo pone una domanda fondamentale con grandi implicazioni mediche: come può avvenire tale caos in un solo balzo, anziché pezzo per pezzo nel corso di molti anni? Esaminando da vicino le estremità cromosomiche danneggiate, gli autori scoprono un processo di riparazione altamente propenso all'errore che può riscrivere lunghe porzioni del genoma in un unico evento.
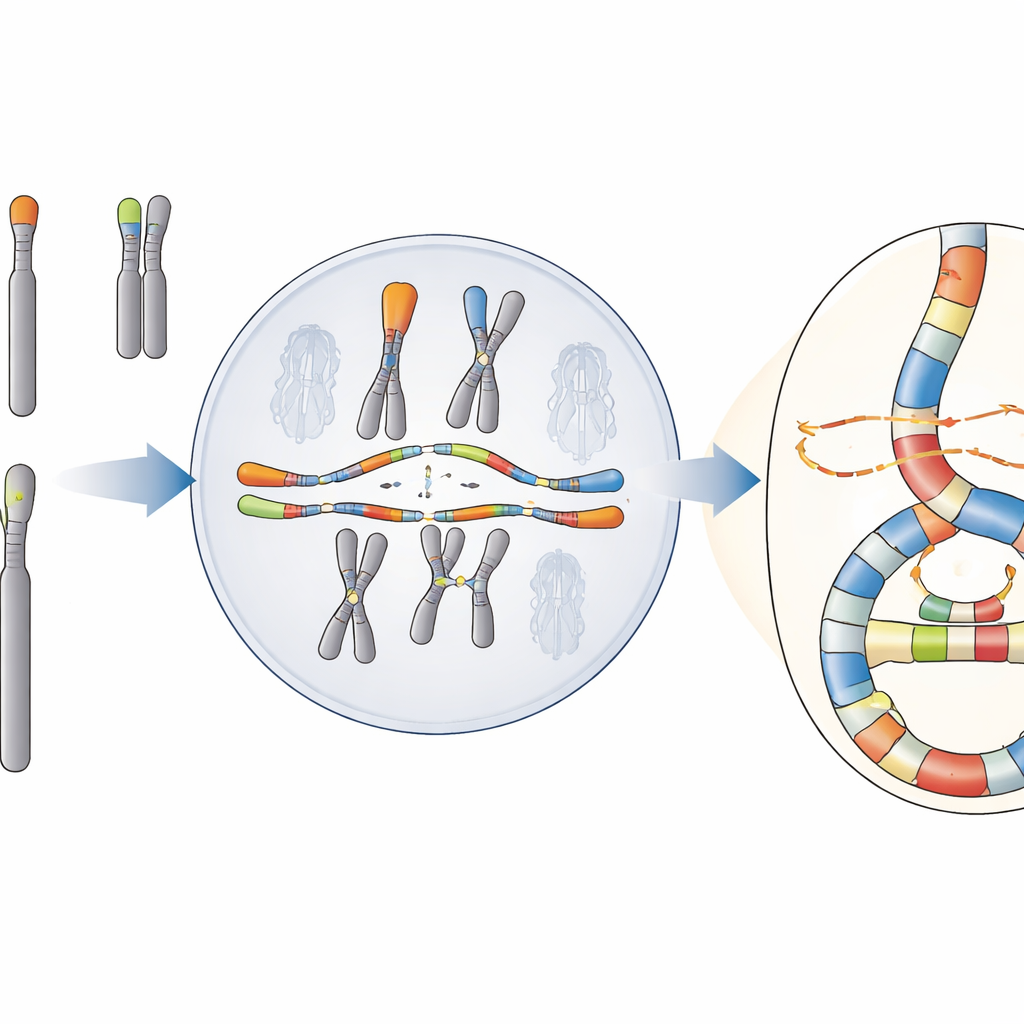
Una catastrofe con un modello nascosto
Il gruppo si concentra su un fenomeno chiamato chromoanasintesi, in cui frammenti di DNA vengono copiati e reinseriti più volte, creando fitti ammassi di riarrangiamenti e copie extra di geni. A differenza di un'altra catastrofe ben nota, la cromotrisipsi, che appare come una riassemblaggio casuale di DNA frantumato, la chromoanasintesi porta l'impronta di ripetute copie del DNA e di passaggi tra diversi stampi. Questi eventi sono comuni nei tumori e in alcuni rari disturbi dello sviluppo, ma le loro origini nelle cellule umane sono state difficili da individuare perché il sequenziamento standard spesso perde la piena complessità delle regioni rimescolate.
Leggere molecole di DNA ultra‑lunghe
Per affrontare il problema, gli autori hanno messo a punto un metodo di sequenziamento a singola molecola con letture lunghe, Fusion‑seq Long‑Read (FSLR), mirato specificamente alle estremità cromosomiche, o telomeri, che si sono fuse. Hanno studiato fibroblasti umani spinti in una “crisi dei telomeri”, uno stato in cui le estremità cromosomiche diventano pericolosamente corte, e hanno anche usato forbici molecolari ingegnerizzate per tagliare il DNA appena entro i telomeri in linee cellulari tumorali. Il sequenziamento a letture lunghe ha permesso di seguire ogni molecola di DNA fusa da un capo all'altro, rivelando non solo dove i due telomeri si incontravano ma anche ogni frammento aggiuntivo inserito tra loro e da dove nel genoma quei frammenti provenivano.
Una via di riparazione mutagena copia‑e‑incolla
Le molecole fuse che hanno scoperto erano sorprendentemente complesse. Alcune contenevano dozzine o anche più di cento frammenti inseriti provenienti da molti cromosomi, con frequenti “hotspot” che erano stati copiati ripetutamente. Le giunzioni tra i frammenti spesso condividevano poche basi corrispondenti, un marchio della coppia basata su “microomologia” piuttosto che di una riparazione pulita da manuale. I modelli indicavano con forza un meccanismo copia‑e‑incolla noto come replicazione indotta da rotture mediata da microomologia (MM‑BIR). In questo processo, un estremo di DNA rotto si appaia brevemente con una breve sequenza corrispondente su un altro filamento, inizia a copiare, poi si stacca e si aggancia a un altro stampo, lasciando dietro di sé una scia di segmenti duplicati e riarrangiati. Esperimenti genetici e farmacologici hanno mostrato che questa via dipende dalla collaborazione tra enzimi normalmente associati alla giunzione di piccole patch e una macchina di replicazione più potente in grado di copiare lunghe porzioni di DNA.
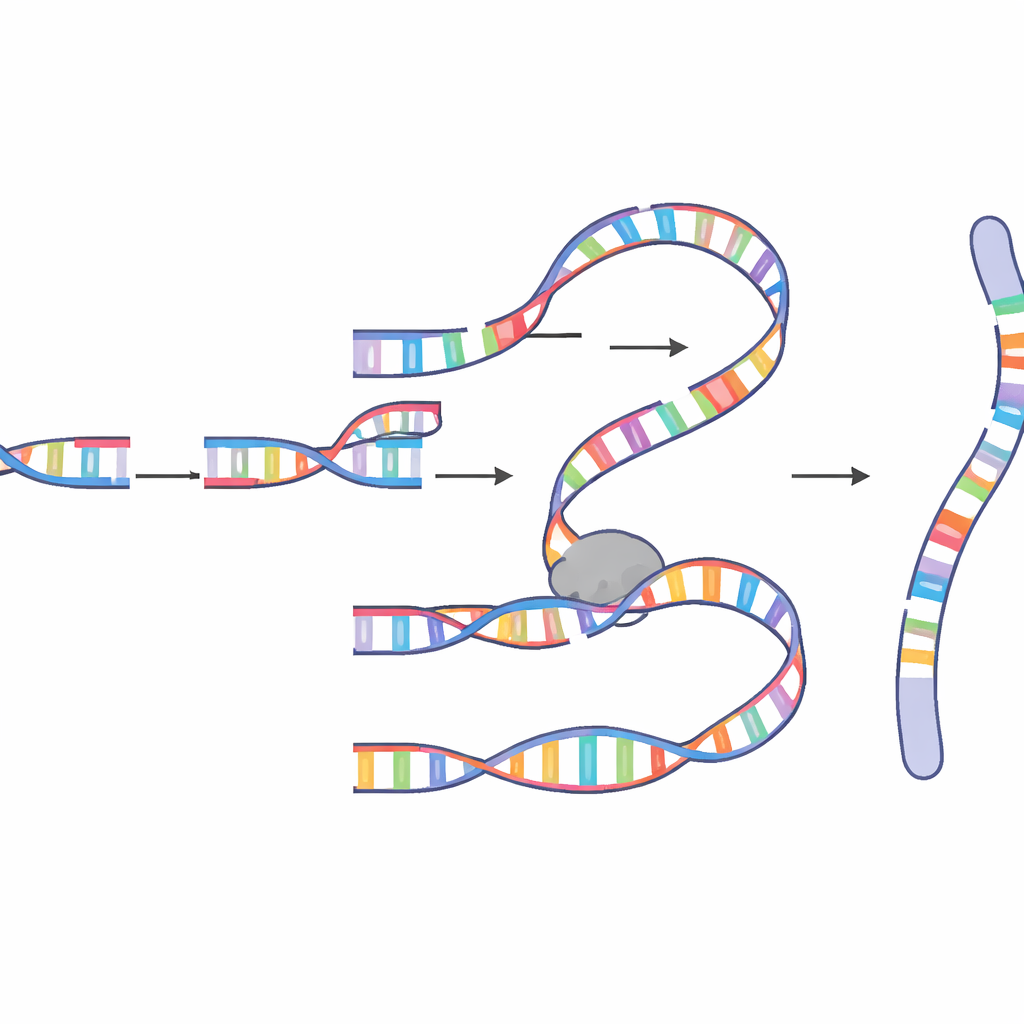
Perché la mitosi è un momento pericoloso
Una sorpresa chiave riguarda il timing. La chromoanasintesi in questo sistema è emersa specificamente durante la mitosi, la breve finestra in cui le cellule si dividono e i cromosomi sono altamente condensati. Gli autori hanno dimostrato che quando il checkpoint del danno G2/M della cellula—la sua principale salvaguardia che blocca l'ingresso in mitosi con DNA rotto—veniva indebolito, eventi complessi diventavano molto più frequenti. Hanno inoltre mostrato che un enzima chiamato polimerasi theta, noto come fattore di riparazione “ultima risorsa”, gioca un ruolo centrale, aiutando gli estremi rotti a trovare micro sequenze corrispondenti e a iniziare la sintesi. Enzimi più processivi come la polimerasi delta poi estendono il nuovo DNA, agevolati da fattori come PIF1, POLD3 e PCNA che mantengono in movimento la macchina di replicazione. Quando questi co‑fattori venivano alterati, la lunghezza e il modello del DNA inserito cambiavano, confermando che la chromoanasintesi è guidata da una versione mitotica specializzata di MM‑BIR piuttosto che da una semplice ligazione di frammenti rotti.
Nuovi indizi su cancro e difetti congeniti
Complessivamente, il lavoro rivela una via di “riparazione d'emergenza” altamente mutagena che entra in funzione quando estremità cromosomiche rotte incontrano la mitosi. Invece di ripristinare delicatamente la sequenza originale, la MM‑BIR mitotica può amplificare e rimescolare rapidamente regioni genomiche, incluse aree ricche di geni e potenziali oncogeni, in un singolo evento. Per una cellula sana questo è un modo rischioso ma talvolta inevitabile per completare la replicazione e la divisione. Per una cellula precancerosa, invece, può fornire esattamente il tipo di sconvolgimento genomico che guida una crescita tumorale aggressiva o contribuisce ai complessi cambiamenti cromosomici osservati nei disturbi congeniti. Mappando questo processo in dettaglio molecolare, lo studio indica nuovi modi per comprendere—e forse un giorno mirare—a quel rimescolamento catastrofico del genoma che sta alla base di alcune delle più difficili malattie umane.
Citazione: Ngo, G.H.P., Cleal, K., Seifan, S. et al. Mitotic microhomology-mediated break-induced replication promotes chromoanasynthesis. Nat Commun 17, 3375 (2026). https://doi.org/10.1038/s41467-026-70086-y
Parole chiave: riarrangiamenti cromosomici, crisi dei telomeri, riparazione del DNA, instabilità del genoma, genetica del cancro