Clear Sky Science · pt
Replicação induzida por quebras mediada por micro-homologia durante mitose promove a cronoanassíntese
Quando os cromossomos saem do controle
Câncer e alguns defeitos congênitos frequentemente surgem quando nossos cromossomos são embaralhados de formas extremas: trechos de DNA são duplicados, invertidos e costurados em mosaicos bizarros. Este artigo investiga uma pergunta básica com grandes implicações médicas: como tal caos acontece em um único salto, em vez de pouco a pouco ao longo de muitos anos? Ao observar de perto as extremidades cromossômicas danificadas, os autores revelam um processo de reparo altamente propenso a erros que pode reescrever longos trechos do genoma de uma só vez.
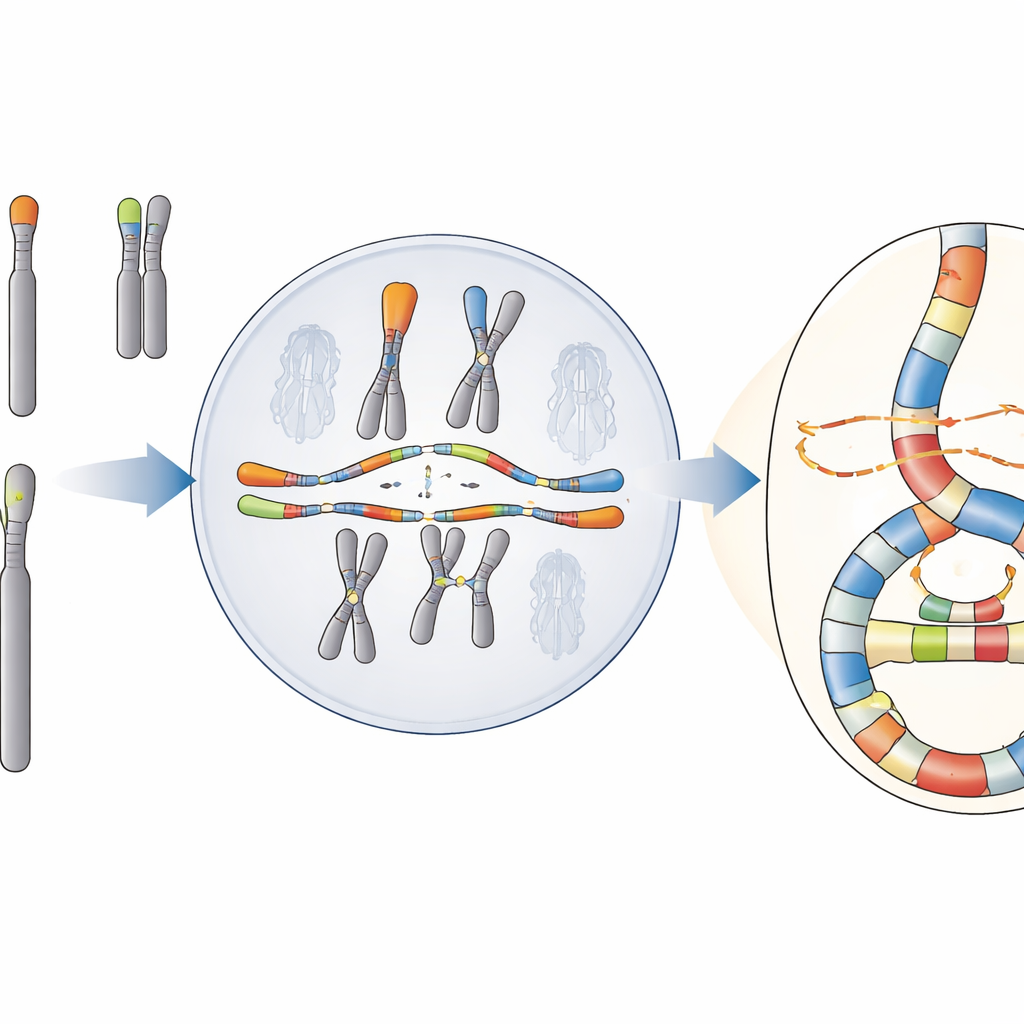
Uma catástrofe com um padrão oculto
O grupo concentra-se em um fenômeno chamado cronoanassíntese, no qual pedaços de DNA são copiados e reinseridos várias vezes, criando aglomerados densos de rearranjos e cópias extras de genes. Ao contrário de outra catástrofe bem conhecida, a cromotripse, que parece uma remendagem aleatória de DNA estilhaçado, a cronoanassíntese carrega a impressão digital da cópia repetida de DNA e da troca entre moldes. Esses eventos são comuns em cânceres e em alguns distúrbios de desenvolvimento raros, mas suas origens em células humanas têm sido difíceis de definir porque o sequenciamento padrão frequentemente perde a complexidade completa das regiões reordenadas.
Lendo moléculas de DNA ultra‑longas
Para enfrentar isso, os autores desenvolveram um método de sequenciamento de leitura longa por molécula única, Fusion‑seq Long‑Read (FSLR), voltado especificamente para extremidades cromossômicas, ou telômeros, que se fundiram. Eles estudaram fibroblastos humanos empurrados para uma “crise do telômero”, um estado em que as extremidades dos cromossomos ficam perigosamente curtas, e também usaram tesouras moleculares projetadas para cortar o DNA logo dentro dos telômeros em linhagens de células cancerosas. O sequenciamento de leitura longa permitiu que seguissem cada molécula de DNA fundida de ponta a ponta, revelando não apenas onde os dois telômeros se encontravam, mas também cada fragmento extra encaixado entre eles e de onde no genoma esses fragmentos se originaram.
Uma via de reparo copiar‑e‑colar mutagênica
As moléculas fundidas que descobriram eram surpreendentemente complexas. Algumas continham dezenas ou até mais de cem fragmentos inseridos provenientes de muitos cromossomos, com “hotspots” frequentes que haviam sido copiados repetidamente. As junções entre fragmentos frequentemente compartilhavam algumas bases correspondentes, um sinal característico de pareamento baseado em “micro-homologia” em vez de reparo limpo e convencional. Os padrões apontavam fortemente para um mecanismo de copiar‑e‑colar conhecido como replicação induzida por quebras mediada por micro‑homologia (MM‑BIR). Nesse processo, uma extremidade de DNA quebrada pareia brevemente com uma sequência curta correspondente em outra molécula de DNA, começa a copiar, depois se solta e se liga a outro molde, deixando um rastro de segmentos duplicados e rearranjados. Experimentos genéticos e com drogas mostraram que essa via depende da colaboração entre enzimas normalmente associadas à ligação de pequenos trechos e uma máquina de replicação mais robusta capaz de copiar longos trechos de DNA.
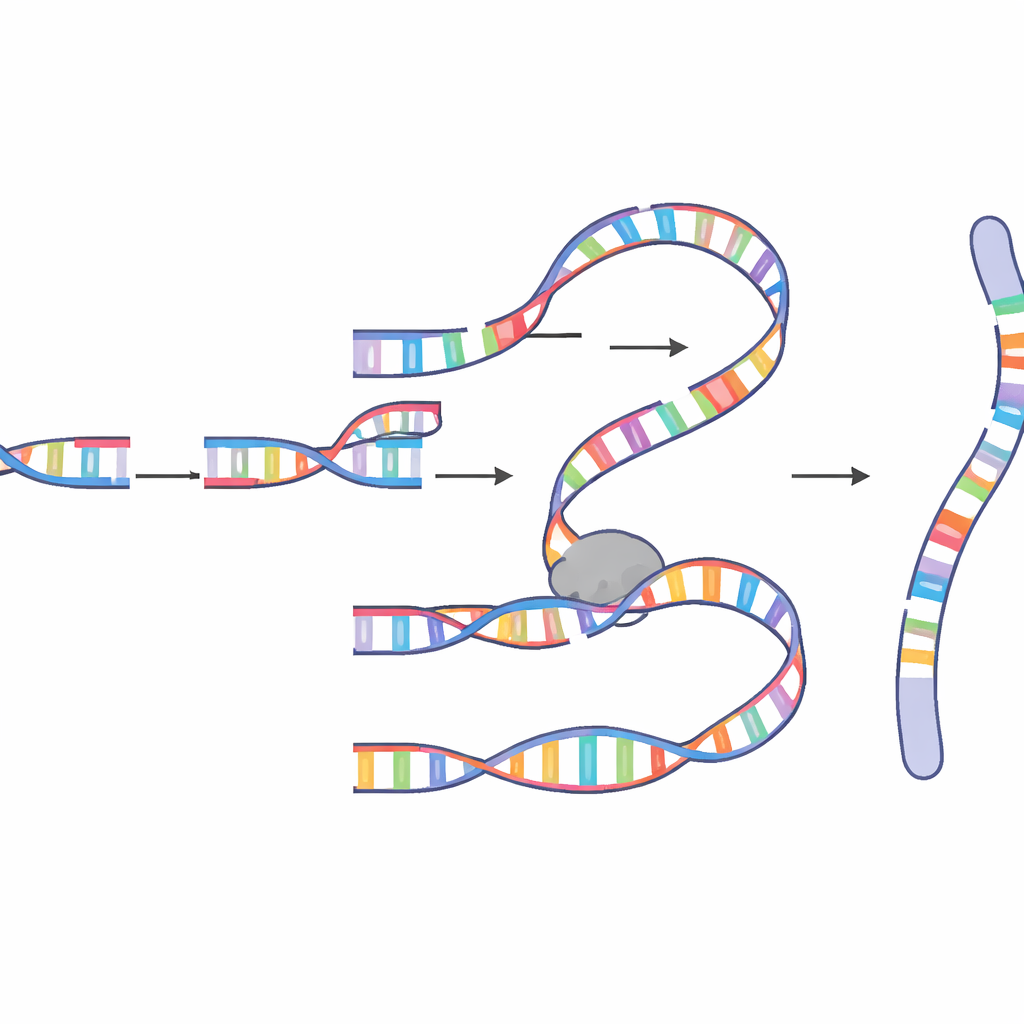
Por que a mitose é um momento perigoso
Uma surpresa chave foi o momento. A cronoanassíntese neste sistema surgiu especificamente durante a mitose, a janela breve em que as células se dividem e os cromossomos ficam altamente condensados. Os autores mostraram que quando o ponto de checagem de danos G2/M da célula—sua principal salvaguarda que bloqueia a entrada na mitose com DNA quebrado—estava enfraquecido, eventos complexos tornaram‑se muito mais frequentes. Eles também demonstraram que uma enzima chamada polimerase theta, conhecida como um fator de reparo de “último recurso”, desempenha um papel central, ajudando extremidades quebradas a encontrar pequenas sequências correspondentes e iniciar a síntese. Enzimas mais processivas, como a polimerase delta, então estendem o novo DNA, auxiliadas por fatores como PIF1, POLD3 e PCNA que mantêm a maquinaria de replicação em movimento. Quando esses ajudantes foram alterados, o comprimento e o padrão do DNA inserido mudaram, confirmando que a cronoanassíntese é impulsionada por uma versão mitótica especializada do MM‑BIR e não por simples ligadura de fragmentos quebrados.
Novas pistas sobre câncer e defeitos congênitos
No conjunto, o trabalho revela uma via de “reparo de emergência” altamente mutagênica que entra em ação quando extremidades cromossômicas quebradas encontram a mitose. Em vez de restaurar suavemente a sequência original, o MM‑BIR mitótico pode amplificar e remixar rapidamente regiões genômicas, incluindo áreas ricas em genes e potenciais oncogenes, em um único evento. Para uma célula saudável, isso é arriscado, mas às vezes inevitável para concluir a replicação e a divisão. Para uma célula precancerosa, entretanto, pode fornecer exatamente o tipo de convulsão genômica que impulsiona o crescimento tumoral agressivo ou contribui para alterações cromossômicas complexas vistas em doenças congênitas. Ao mapear esse processo em detalhes moleculares, o estudo aponta para novas maneiras de entender—e talvez um dia direcionar—o embaralhamento catastrófico do genoma que está na base de algumas das doenças humanas mais difíceis.
Citação: Ngo, G.H.P., Cleal, K., Seifan, S. et al. Mitotic microhomology-mediated break-induced replication promotes chromoanasynthesis. Nat Commun 17, 3375 (2026). https://doi.org/10.1038/s41467-026-70086-y
Palavras-chave: rearranjos cromossômicos, crise do telômero, reparo de DNA, instabilidade genômica, genética do câncer