Clear Sky Science · de
Mitotische, mikrohomologievermittelte break‑induced‑Replikation fördert Chromoanasynthese
Wenn Chromosomen außer Kontrolle geraten
Krebs und einige angeborene Fehlbildungen entstehen häufig, wenn unsere Chromosomen auf extreme Weise durcheinandergeraten: DNA‑Abschnitte werden vervielfältigt, umgedreht und zu bizarren Flickenteppichen zusammengesetzt. Diese Arbeit stellt eine grundlegende Frage mit großen medizinischen Folgen: Wie kann ein solches Chaos in einem einzigen Sprung entstehen, statt Stück für Stück über viele Jahre? Durch genaues Hinsehen an beschädigten Chromosomenenden enthüllen die Autorinnen und Autoren einen hochfehleranfälligen Reparaturprozess, der lange Abschnitte des Genoms auf einmal umschreiben kann.
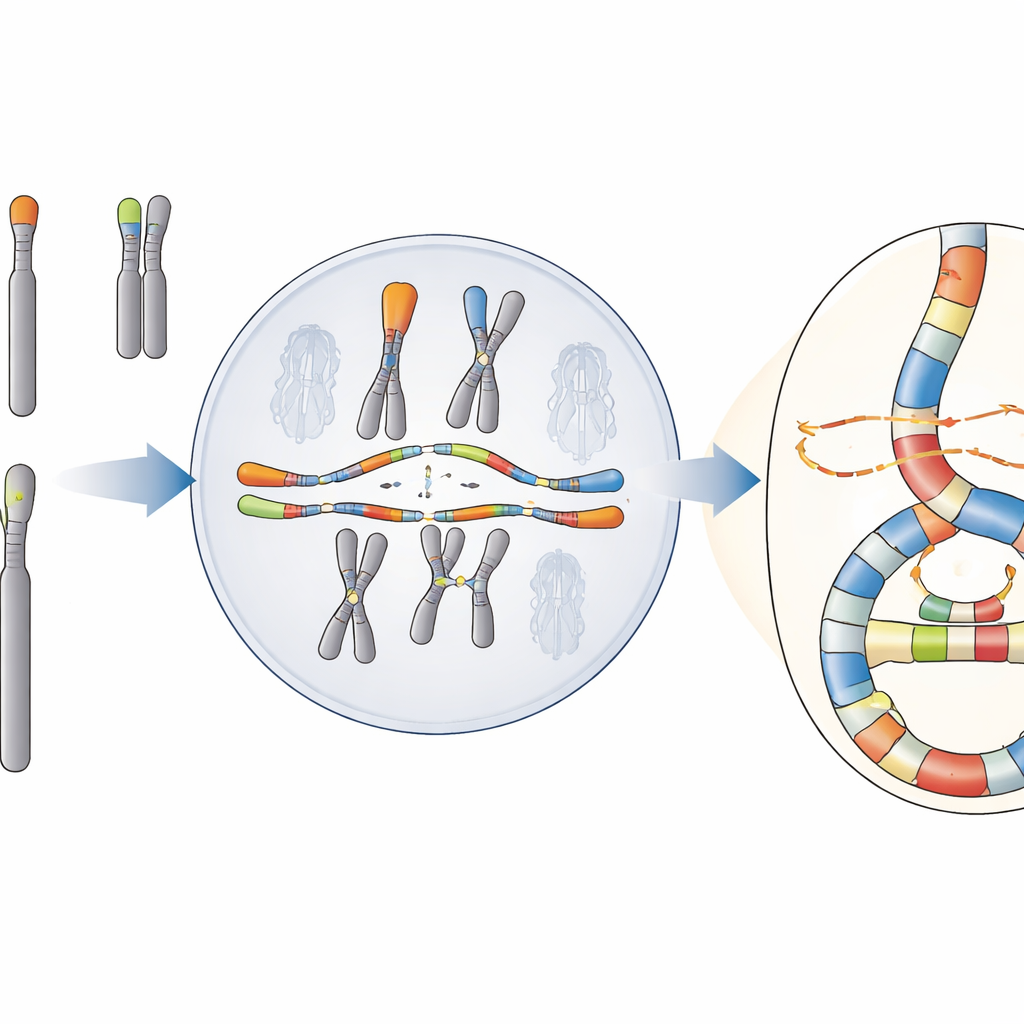
Eine Katastrophe mit verstecktem Muster
Das Team konzentriert sich auf ein Phänomen namens Chromoanasynthese, bei dem DNA‑Stücke kopiert und vielfach wieder eingefügt werden, wodurch dichte Cluster von Umlagerungen und zusätzliche Genkopien entstehen. Im Gegensatz zu einer anderen bekannten Katastrophe, der Chromothripsis, die wie zufälliges Wiederverkleben zersplitterter DNA aussieht, trägt die Chromoanasynthese die Signatur wiederholten DNA‑Kopierens und des Wechsels zwischen Matrizen. Diese Ereignisse sind in Tumoren und bei einigen seltenen Entwicklungsstörungen häufig, aber ihre Ursprünge in menschlichen Zellen waren schwer zu fassen, weil Standardsequenzierung oft die volle Komplexität der umgestalteten Regionen verfehlt.
Ultra‑lange DNA‑Moleküle lesen
Um das zu untersuchen, entwickelten die Autorinnen und Autoren eine Einzelmolekül‑Langlese‑Sequenziermethode, Fusion‑seq Long‑Read (FSLR), die speziell auf verschmolzene Chromosomenenden beziehungsweise Telomere abzielt. Sie untersuchten humane Fibroblasten, die in eine „Telomerkrise“ gedrängt wurden, einen Zustand, in dem Chromosomenenden gefährlich kurz werden, und nutzten außerdem gentechnisch gefertigte molekulare Scheren, um DNA kurz innerhalb der Telomere in Tumorzelllinien zu zerschneiden. Die Langlese‑Sequenzierung erlaubte es, jedes verschmolzene DNA‑Molekül von Ende zu Ende zu verfolgen und zeigte nicht nur, wo sich die beiden Telomere trafen, sondern auch jedes zusätzliche Fragment dazwischen und aus welchen Bereichen des Genoms diese Fragmente stammten.
Ein mutagenes Kopier‑und‑Einfüge‑Reparaturprogramm
Die entdeckten verschmolzenen Moleküle waren verblüffend komplex. Einige enthielten dutzende bis hin zu mehr als hundert eingesetzte Fragmente aus vielen Chromosomen, mit häufigen „Hotspots“, die wiederholt kopiert worden waren. Die Verbindungsstellen zwischen Fragmenten teilten oft wenige übereinstimmende Basen, ein Kennzeichen für mikrohomologiebasierte Paarung statt sauberer, schulbuchmäßiger Reparatur. Die Muster wiesen stark auf einen Kopier‑und‑Einfüge‑Mechanismus hin, bekannt als mikrohomologie‑vermittelte break‑induced‑Replikation (MM‑BIR). Bei diesem Prozess paart sich ein gebrochenes DNA‑Ende kurz mit einer kurzen, passenden Sequenz auf einer anderen DNA‑Vorlage, beginnt zu kopieren, löst sich dann wieder und heftet sich an eine weitere Vorlage an, wobei eine Spur von duplizierten und umgelagerten Segmenten zurückbleibt. Genetische und medikamentöse Experimente zeigten, dass dieser Weg auf einer Zusammenarbeit zwischen Enzymen beruht, die normalerweise mit kleineren End‑Joining‑Reparaturen assoziiert sind, und einer leistungsfähigeren Replikationsmaschinerie, die lange DNA‑Abschnitte kopieren kann.
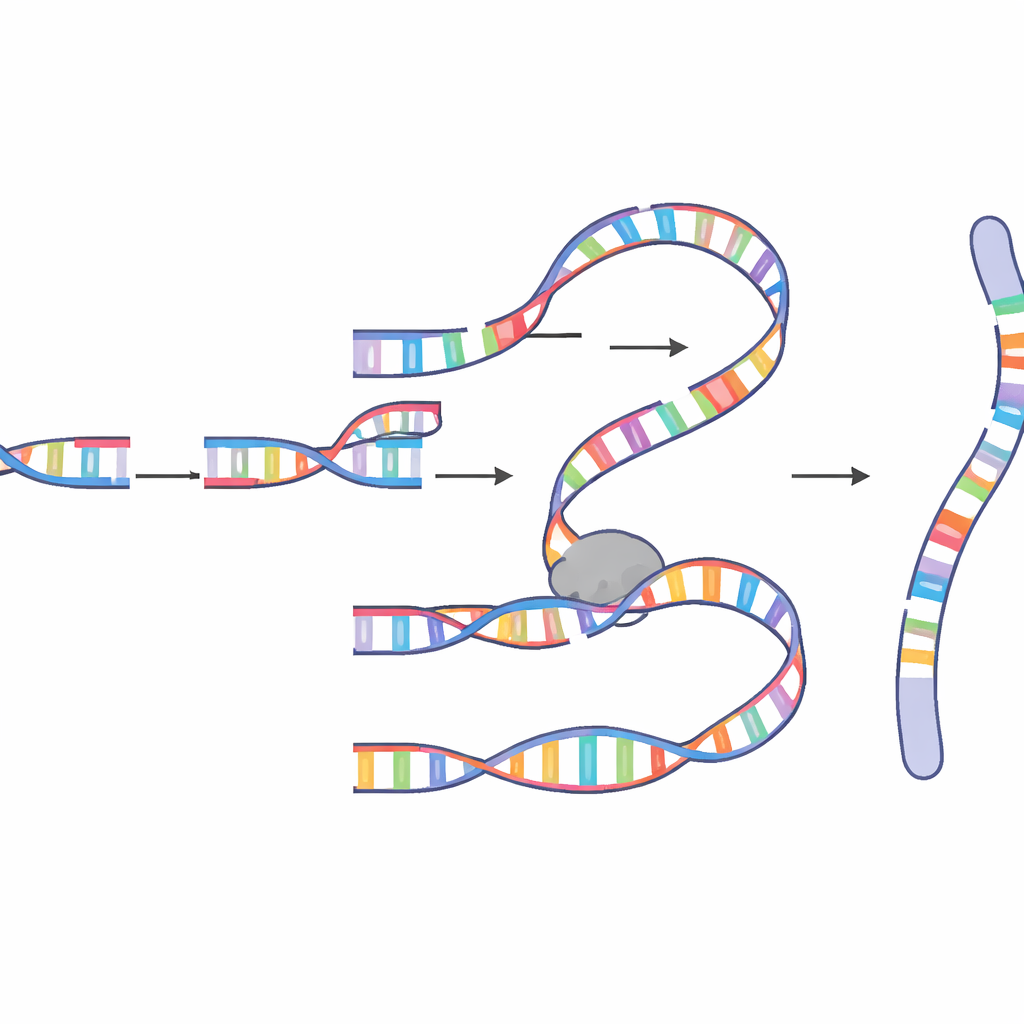
Warum die Mitose ein gefährlicher Moment ist
Eine wichtige Überraschung war das Timing. Die Chromoanasynthese in diesem System entstand spezifisch während der Mitose, dem kurzen Zeitfenster, in dem sich Zellen teilen und Chromosomen stark kondensiert sind. Die Autorinnen und Autoren zeigten, dass komplexe Ereignisse deutlich häufiger wurden, wenn die G2/M‑Schadens‑Checkpoint der Zelle – ihre wichtigste Schutzfunktion, die das Eintreten in die Mitose bei vorhandener DNA‑Schädigung verhindert – geschwächt war. Sie demonstrierten außerdem, dass ein Enzym namens Polymerase Theta, bekannt als „allerletzte“ Reparaturfaktor, eine zentrale Rolle spielt, indem es gebrochene Enden hilft, winzige passende Sequenzen zu finden und die Synthese zu initiieren. Anschließend erweitern prozessivere Enzyme wie Polymerase Delta das neue DNA‑Stück, unterstützt von Faktoren wie PIF1, POLD3 und PCNA, die die Replikationsmaschinerie in Bewegung halten. Wenn diese Helfer verändert wurden, änderten sich Länge und Muster der eingesetzten DNA, was bestätigt, dass Chromoanasynthese von einer spezialisierten, mitotischen Form der MM‑BIR angetrieben wird und nicht durch einfaches Verkleben gebrochener Fragmente.
Neue Hinweise auf Krebs und angeborene Fehlbildungen
Insgesamt offenbart die Arbeit einen hochmutagenen „Notfall‑Reparatur“‑Weg, der aktiv wird, wenn gebrochene Chromosomenenden auf die Mitose treffen. Statt die ursprüngliche Sequenz behutsam wiederherzustellen, kann die mitotische MM‑BIR genomische Regionen schnell amplifizieren und neu mischen, einschließlich genreicher Bereiche und potenzieller Onkogene, in einem einzigen Ereignis. Für eine gesunde Zelle ist dies ein riskanter, aber mitunter unvermeidbarer Weg, um Replikation und Zellteilung abzuschließen. Für eine präkanzeröse Zelle hingegen kann dies genau die Art genomischer Umwälzung liefern, die aggressives Tumorwachstum antreibt oder zu komplexen chromosomalen Veränderungen beiträgt, wie sie bei angeborenen Störungen beobachtet werden. Indem die Studie diesen Prozess auf molekularer Ebene kartiert, weist sie auf neue Wege hin, das katastrophale Umgestalten des Genoms zu verstehen – und möglicherweise eines Tages gezielt zu beeinflussen – das einigen der schwierigsten menschlichen Krankheiten zugrunde liegt.
Zitation: Ngo, G.H.P., Cleal, K., Seifan, S. et al. Mitotic microhomology-mediated break-induced replication promotes chromoanasynthesis. Nat Commun 17, 3375 (2026). https://doi.org/10.1038/s41467-026-70086-y
Schlüsselwörter: chromosomale Umlagerungen, Telomerkrise, DNA‑Reparatur, Genomintegritätsverlust, Krebsgenetik