Clear Sky Science · ar
التضاعف الناجم عن الكسر بوساطة الميكروتطابق في الطور الانقسامي يعزز التشكل الصبغي الشاذ
عندما تخرج الكروموسومات عن السيطرة
غالبًا ما ينشأ السرطان وبعض العيوب الخلقية عندما تُختلط كروموسوماتنا بطرق متطرفة: تُنسخ مقاطع من الحمض النووي، وتنقلب، وتُخاط معًا لتكوّن تركيبات غريبة. تطرح هذه الورقة سؤالًا أساسيًا ذو آثار طبية كبيرة: كيف يحدث مثل هذا الفوضى في قفزة واحدة بدلاً من أن تتراكم تدريجيًا على مدى سنوات؟ من خلال فحص نهايات الكروموسومات التالفة عن قرب، يكشف المؤلفون عملية إصلاح شديدة العرضة للأخطاء يمكنها إعادة كتابة مسافات طويلة من الجينوم دفعة واحدة.
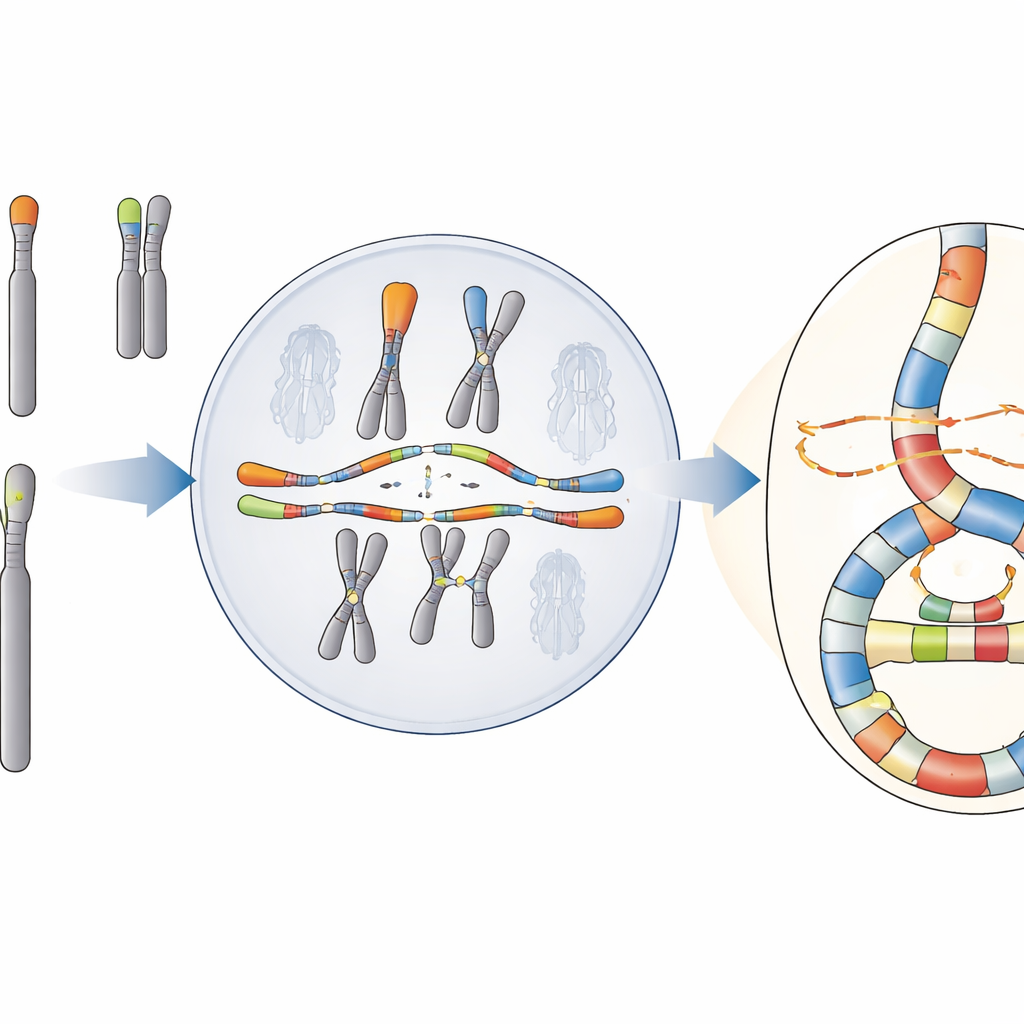
كارثة تحمل نمطًا خفيًا
تركز الفريق على ظاهرة تُسمى التشكل الصبغي الشاذ (chromoanasynthesis)، التي تُنسخ فيها قطع من الحمض النووي وتُعاد إدخالها عدة مرات، فتُكوّن عنقودًا كثيفًا من إعادة الترتيبات ونسخًا إضافية من الجينات. على خلاف كارثة معروفة أخرى، التحطيم الصبغي (chromothripsis)، التي تبدو كإعادة لصق عشوائية لحمض نووي مُحطّم، يحمل التشكل الصبغي الشاذ بصمة النسخ المتكرر والتبديل بين القوالب. تُرى هذه الأحداث غالبًا في السرطانات وبعض الاضطرابات التنموية النادرة، لكن أصلها في الخلايا البشرية كان من الصعب تحديده لأن التقنيات التسلسلية القياسية غالبًا ما تفوّت التعقيد الكامل للمناطق المُعاد تشكيلها.
قراءة جزيئات الحمض النووي فائقة الطول
لمعالجة هذا، طور المؤلفون أسلوب تسلسل طويل القراءة لجزيء واحد، Fusion-seq Long-Read (FSLR)، مخصّصًا تحديدًا لنهايات الكروموسومات، أو التيلوميرات، التي التحمت معًا. درسوا الأرومات الليفية البشرية التي دُفعت إلى «أزمة التيلومير»، وهي حالة تقصر فيها نهايات الكروموسومات بشكل خطير، واستخدموا أيضًا مقصات جزيئية معدّلة لقطع الحمض النووي داخل التيلوميرات في خطوط خلايا سرطانية. سمح التسلسل طويل القراءة لهم بتتبع كل جزيء DNA مُلتصق من طرف إلى طرف، كاشفًا ليس فقط مكان التقاء التيلوميرين بل أيضًا كل مقطع إضافي محشور بينهما ومن أين أتى ذلك المقطع في الجينوم.
مسار إصلاحٍ مُحرِّض للطفرات بالنسخ واللصق
كانت الجزيئات الملتحمة التي كشفوها معقدة بشكل مذهل. احتوت بعضها على عشرات أو حتى أكثر من مئة مقطع مُدرج مأخوذ من كروموسومات متعددة، مع «نقاط ساخنة» متكررة تعرضت للنسخ مرارًا. غالبًا ما شاركت الوصلات بين المقاطع بضع قواعد متطابقة، وهو سِمة من سمات الاقتران القائم على «الميكروتطابق» بدلًا من الإصلاح النظيف المألوف في الكتب الدراسية. أشارت الأنماط بقوة إلى آلية نسخ ولصق تُعرف باسم الاستنساخ الناجم عن الكسور بوساطة الميكروتطابق (microhomology-mediated break-induced replication, MM-BIR). في هذه العملية، يقترن طرف الحمض النووي المكسور مؤقتًا بتسلسل قصير مطابق على جزيء DNA آخر، يبدأ النسخ، ثم ينفك ويرتبط بقالب آخر، تاركًا وراءه سلسلة من المقاطع المكررة والمعاد ترتيبها. أظهرت تجارب وراثية وتجارب تعتمد على أدوية أن هذا المسار يعتمد على تعاون بين إنزيمات مرتبطة عادةً بربط الأطراف في رقع صغيرة وآلة تكرار أكثر قوة قادرة على نسخ مسافات طويلة من الحمض النووي.
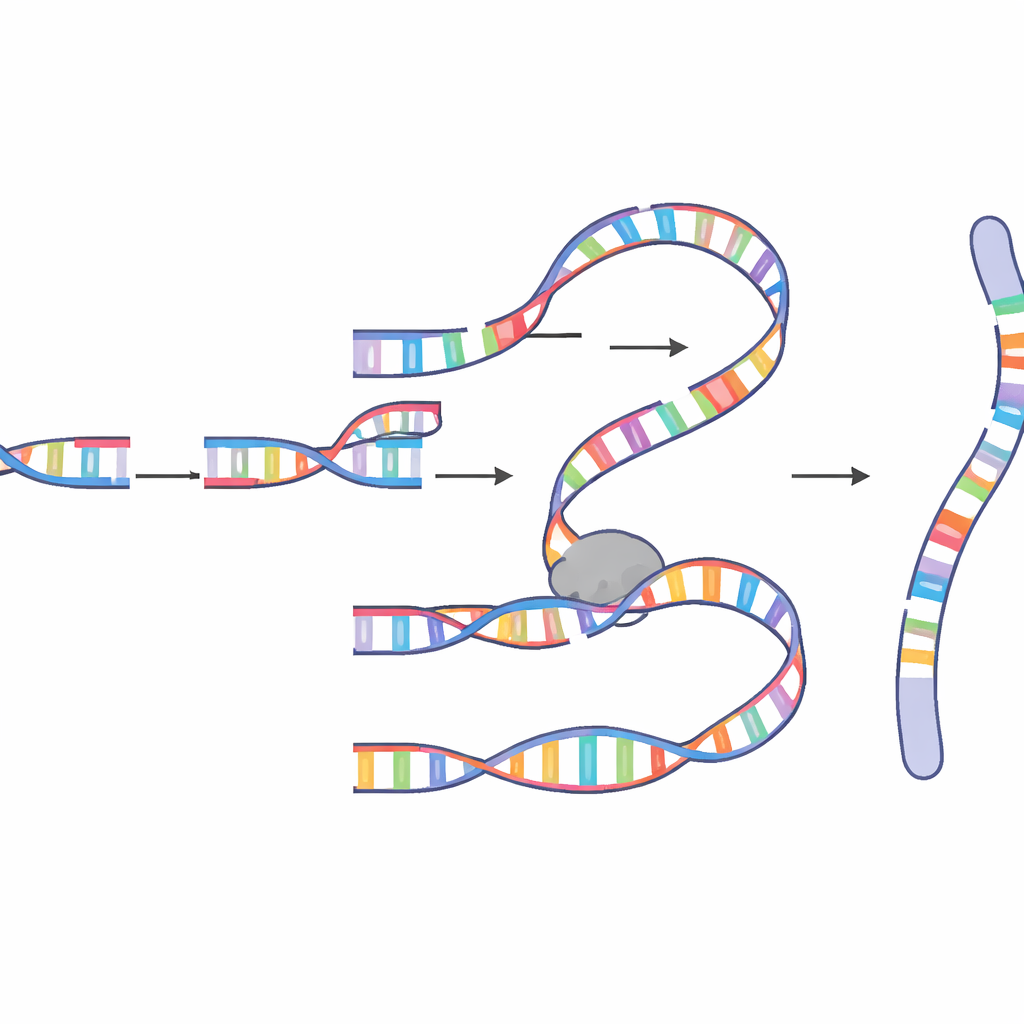
لماذا يمثل الانقسام الخلوي لحظة خطرة
كان توقيت حدوث ذلك مفاجأة رئيسية. ظهر التشكل الصبغي الشاذ في هذا النظام تحديدًا أثناء الطور الانقسامي، النافذة القصيرة عندما تنقسم الخلايا وتتكثف الكروموسومات بشدة. أظهر المؤلفون أنه عندما ضعُف حاجز فحص الأضرار في مرحلة G2/M—الحاجز الرئيسي الذي يمنع دخول الطور الانقسامي مع وجود حمض نووي مكسور—أصبحت الأحداث المعقدة أكثر تواترًا بكثير. وأثبتوا أيضًا أن إنزيمًا يسمى بوليميراز ثيتا، المعروف بعامل إصلاح «الملجأ الأخير»، يلعب دورًا مركزيًا، إذ يساعد النهايات المكسورة في العثور على تسلسلات مطابقة صغيرة وبدء التخليق. ثم تمدد إنزيمات أكثر قدرة على الاستمرار مثل بوليميراز دلتا الحمض النووي الجديد، بمساعدة عوامل مثل PIF1 وPOLD3 وPCNA التي تحافظ على حركة آلية النسخ. عندما تغيّرت هذه المساعدات، تغير طول ونمط الحمض النووي المُدرج، مما يؤكد أن التشكل الصبغي الشاذ يُقاد بواسطة نسخة متخصصة أثناء الطور الانقسامي من MM-BIR وليس بواسطة ربط بسيط للمقاطع المكسورة.
أدلة جديدة للسرطان والعيوب الخلقية
بالمحصلة، تكشف الدراسة عن مسار «إصلاح طارئ» شديد التحريضي للطفرات ينشط عندما تلتقي نهايات الكروموسومات المكسورة بالطور الانقسامي. بدلًا من استعادة التسلسل الأصلي بلطف، يمكن لـMM-BIR الانقسامي تضخيم وأعادة مزج مناطق جينومية بسرعة، بما في ذلك المناطق الغنية بالجينات والجينات المحتملة المسببة للسرطان، في حدث واحد. بالنسبة للخلية السليمة هذا مسار محفوف بالمخاطر لكنه قد يكون أحيانًا الطريقة الحتمية لإكمال النسخ والانقسام. أما بالنسبة للخلية قبل السرطانية، فربما يوفر بالضبط نوع الانقلاب الجينومي الذي يدفع نموّ الورم العدواني أو يساهم في التغيرات الصبغية المعقدة المرصودة في الاضطرابات الخلقية. من خلال رسم ملامح هذه العملية على المستوى الجزيئي، تشير الدراسة إلى طرق جديدة لفهم—وربما يومًا ما استهداف—عمليات إعادة تشكيل الجينوم الكارثية التي تكمن وراء بعض أصعب الأمراض البشرية.
الاستشهاد: Ngo, G.H.P., Cleal, K., Seifan, S. et al. Mitotic microhomology-mediated break-induced replication promotes chromoanasynthesis. Nat Commun 17, 3375 (2026). https://doi.org/10.1038/s41467-026-70086-y
الكلمات المفتاحية: إعادة ترتيب الكروموسومات, أزمة التيلومير, إصلاح الحمض النووي, عدم استقرار الجينوم, وراثة السرطان