Clear Sky Science · pl
Mitotyczna mikrodopasowana replikacja indukowana przez pęknięcia sprzyja chromoanasyntezie
Gdy chromosomy tracą kontrolę
Nowotwory i niektóre wrodzone wady często pojawiają się, gdy nasze chromosomy zostają skrajnie pofragmentowane: odcinki DNA są dublowane, odwracane i zszywane w dziwaczne mozaiki. Artykuł stawia podstawowe pytanie o duże konsekwencje medyczne: jak taka chaos powstaje jednym skokiem, zamiast narastać krok po kroku przez wiele lat? Dzięki szczegółowej analizie uszkodzonych końców chromosomów autorzy odkrywają wysoce błędny proces naprawy, który może przepisać długie fragmenty genomu w jednym zdarzeniu.
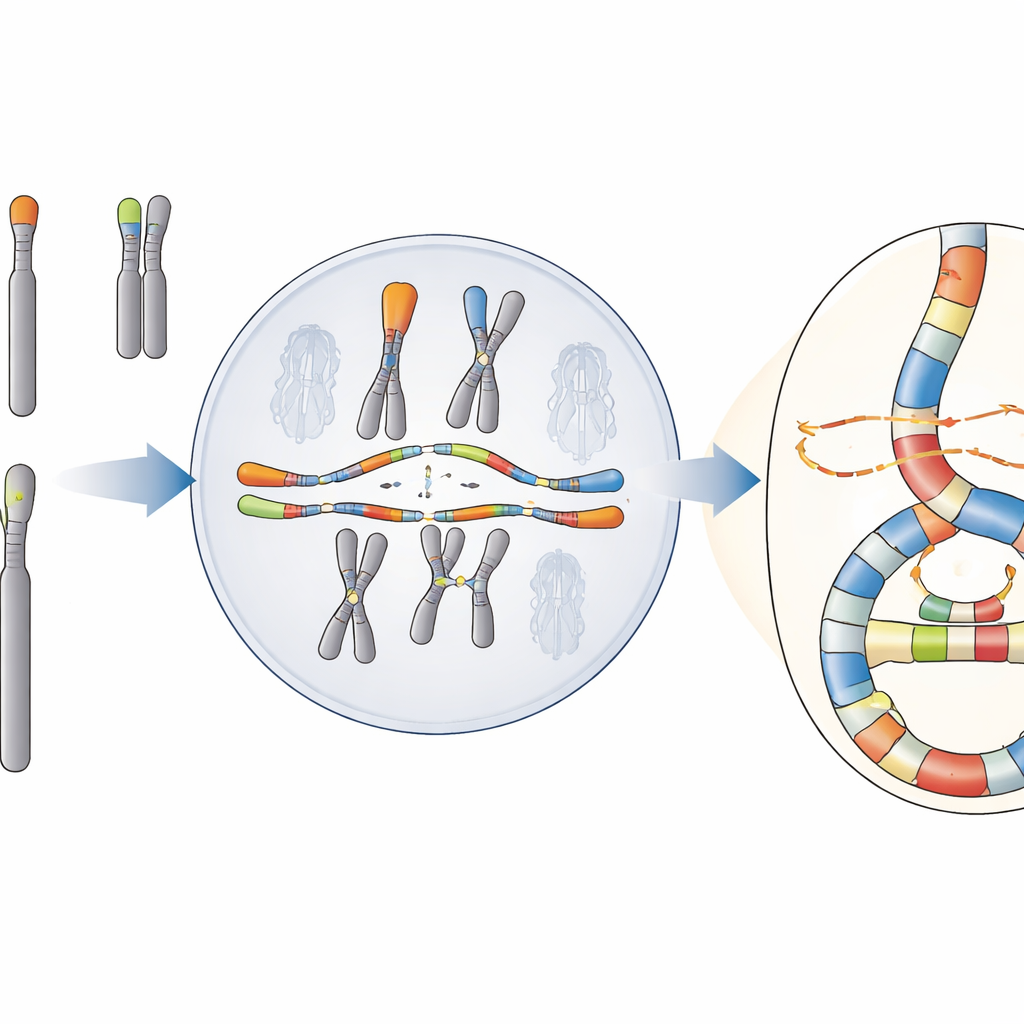
Kataklizm z ukrytym wzorcem
Zespół koncentruje się na zjawisku zwanym chromoanasyntezą, w którym fragmenty DNA są kopiowane i wstawiane wielokrotnie, tworząc gęste skupiska przearanżowań i dodatkowe kopie genów. W przeciwieństwie do innej dobrze znanej katastrofy, chromothripsis, która wygląda jak losowe ponowne sklejanie roztrzaskanego DNA, chromoanasynteza nosi ślady powtarzającego się kopiowania i przełączania między matrycami. Zdarzenia te są powszechne w nowotworach i w niektórych rzadkich zaburzeniach rozwojowych, lecz ich pochodzenie w komórkach ludzkich trudno było ustalić, ponieważ standardowe sekwencjonowanie często nie uchwytuje pełnej złożoności przetasowanych obszarów.
Odczytywanie ultradługich cząsteczek DNA
Aby temu sprostać, autorzy opracowali metodę sekwencjonowania długich odczytów pojedynczej cząsteczki, Fusion-seq Long-Read (FSLR), skierowaną specjalnie na końce chromosomów, czyli telomery, które zrosły się ze sobą. Badali fibroblasty ludzkie wprowadzane w „kryzys telomerowy”, stan, w którym końce chromosomów stają się niebezpiecznie krótkie, oraz używali zaprojektowanych nożyc molekularnych do przecinania DNA tuż wewnątrz telomerów w liniach komórkowych nowotworów. Sekwencjonowanie długich odczytów pozwoliło im śledzić każdą zrośniętą cząsteczkę DNA od końca do końca, ujawniając nie tylko miejsce zetknięcia dwóch telomerów, lecz także każdy dodatkowy fragment wciśnięty pomiędzy nimi oraz pochodzenie tych fragmentów w genomie.
Mutagenny mechanizm kopiuj‑i‑wklej naprawy
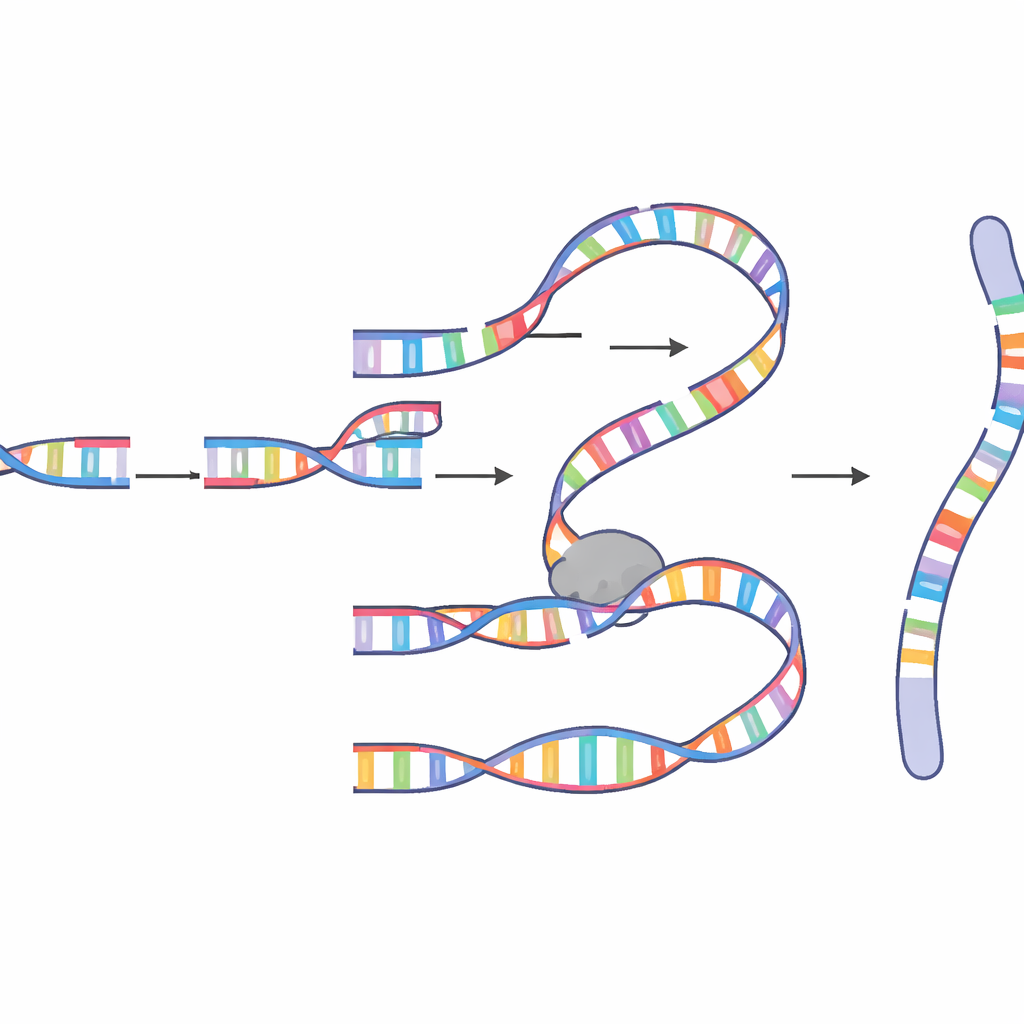
Odkryte zrośnięte cząsteczki były zadziwiająco złożone. Niektóre zawierały dziesiątki, a nawet ponad sto wstawionych fragmentów pochodzących z wielu chromosomów, z częstymi „hotspotami”, które były kopiowane wielokrotnie. Złącza między fragmentami często dzieliły kilka pasujących zasad, co jest znakiem rozpoznawczym parowania opartego na „mikrodopasowaniu” zamiast czystej, podręcznikowej naprawy. Wzorce te jednoznacznie wskazywały na mechanizm kopiuj‑i‑wklej znany jako mikrodopasowana replikacja indukowana przez pęknięcie (MM‑BIR). W tym procesie złamany koniec DNA chwilowo paruje się z krótką pasującą sekwencją na innym fragmencie DNA, zaczyna kopiować, a potem odrywa się i przyłącza do kolejnej matrycy, pozostawiając za sobą ślad zduplikowanych i przearanżowanych segmentów. Eksperymenty genetyczne i z użyciem leków wykazały, że ta ścieżka zależy od współpracy enzymów zwykle związanych z krótkopatchową ligacją końców oraz wydajniejszego aparatu replikacyjnego zdolnego kopiować długie odcinki DNA.
Dlaczego mitoza to niebezpieczny moment
Kluczowym zaskoczeniem był czas występowania zdarzeń. Chromoanasynteza w tym systemie powstawała specyficznie podczas mitozy, krótkiego okresu, kiedy komórki dzielą się, a chromosomy są silnie skondensowane. Autorzy pokazali, że gdy punkt kontrolny uszkodzeń w fazie G2/M—główne zabezpieczenie blokujące wejście w mitozę przy obecności złamanego DNA—został osłabiony, złożone zdarzenia stały się znacznie częstsze. Wykazali też, że enzym zwany polimerazą theta, znany jako czynnik naprawczy „ostatniej szansy”, odgrywa kluczową rolę, pomagając złamanym końcom znaleźć drobne pasujące sekwencje i zainicjować syntezę. Następnie bardziej procesywne enzymy, takie jak polimeraza delta, wydłużają nowy DNA, wspierane przez czynniki takie jak PIF1, POLD3 i PCNA, które utrzymują sprawność aparatu replikacyjnego. Gdy te pomocnicze czynniki były modyfikowane, zmieniała się długość i wzorzec wstawionego DNA, co potwierdza, że chromoanasynteza jest napędzana przez wyspecjalizowaną, mitotyczną wersję MM‑BIR, a nie przez proste zespalanie pękniętych fragmentów.
Nowe wskazówki dotyczące raka i wad wrodzonych
Łącznie praca ujawnia wysoce mutagenną „awaryjną ścieżkę naprawczą”, która uruchamia się, gdy złamane końce chromosomów napotkają mitozę. Zamiast delikatnie przywrócić oryginalną sekwencję, mitotyczna MM‑BIR może szybko amplifikować i przemieszać regiony genomowe, w tym obszary bogate w geny i potencjalne onkogeny, w pojedynczym zdarzeniu. Dla zdrowej komórki jest to ryzykowny, lecz czasem nieunikniony sposób dokończenia replikacji i podziału. Dla komórki przednowotworowej może to jednak stanowić dokładnie taki rodzaj przewrotu genomowego, który napędza agresywny wzrost guza lub przyczynia się do złożonych zmian chromosomalnych obserwowanych w wadach wrodzonych. Mapując ten proces w szczegółach molekularnych, badanie wskazuje nowe drogi rozumienia — i być może pewnego dnia celowania w — katastrofalne przetasowania genomowe leżące u podstaw niektórych z najtrudniejszych chorób ludzkich.
Cytowanie: Ngo, G.H.P., Cleal, K., Seifan, S. et al. Mitotic microhomology-mediated break-induced replication promotes chromoanasynthesis. Nat Commun 17, 3375 (2026). https://doi.org/10.1038/s41467-026-70086-y
Słowa kluczowe: przearanżowania chromosomalne, kryzys telomerowy, naprawa DNA, niestabilność genomu, genetyka nowotworów