Clear Sky Science · ru
Митотическая микроподобная медиируемая восстановлением репликация с прерыванием способствует хромоанасинтезу
Когда хромосомы выходят из строя
Рак и некоторые врожденные аномалии часто возникают, когда наши хромосомы в экстремальных масштабах оказываются перемешаны: участки ДНК дублируются, переворачиваются и сшиваются в причудливые мозаики. В этой работе поставлен базовый вопрос с важными медицинскими последствиями: как такое хаотическое состояние появляется разовым скачком, а не по частям в течение многих лет? Внимательно изучая повреждённые концы хромосом, авторы выявляют крайне ошибко-емкий механизм восстановления, способный переписать большие участки генома за один раз.
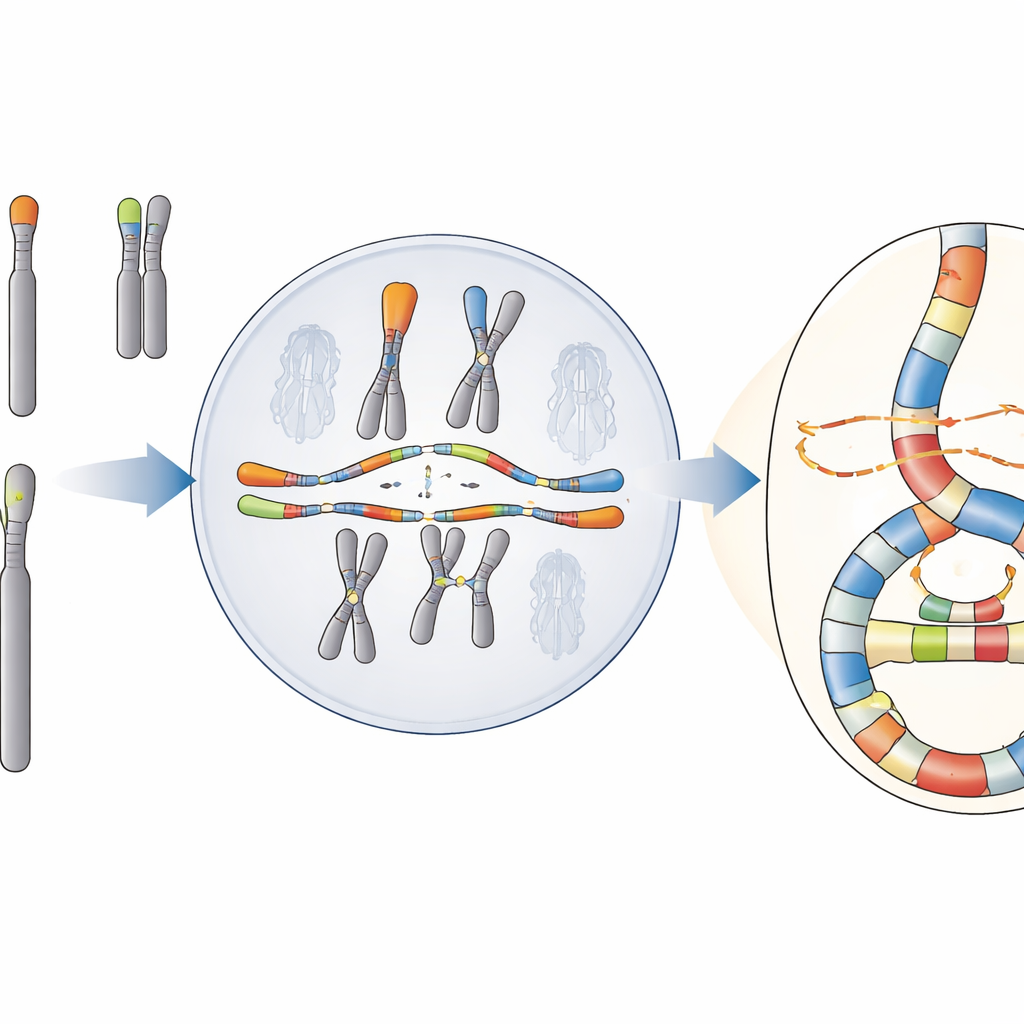
Катастрофа с скрытым узором
Команда сосредоточилась на явлении, называемом хромоанасинтезом, при котором фрагменты ДНК копируются и снова вставляются многократно, создавая плотные кластеры перестроек и дополнительные копии генов. В отличие от хорошо известной катастрофы — хромотрипсиса, выглядящего как случайное «переклеивание» рассыпавшейся ДНК, — хромоанасинтез несёт отпечаток повторного копирования ДНК и переключений между шаблонами. Эти события часто встречаются при раке и некоторых редких наследственных нарушениях, но их происхождение в клетках человека было трудно выяснить, поскольку стандартное секвенирование часто не фиксирует всю сложность перестроенных областей.
Чтение сверхдлинных молекул ДНК
Чтобы решить эту проблему, авторы разработали метод одиночномолекулярного длинного чтения, Fusion-seq Long-Read (FSLR), специально ориентированный на концы хромосом, или теломеры, которые слились друг с другом. Они изучали человеческие фибробласты, доведённые до «кризиса теломер» — состояния, при котором концы хромосом становятся опасно короткими, — а также использовали сконструированные молекулярные «ножницы» для разрезания ДНК непосредственно внутри теломер в линиях раковых клеток. Длинное чтение позволило проследить каждую слитую молекулу ДНК от конца до конца, выявив не только место слияния двух теломер, но и каждую вставленную фрагментную вставку и то, из каких участков генома эти фрагменты происходят.
Мутагенный путь восстановления «копировать‑и‑вставить»
Обнаруженные слитые молекулы были поразительно сложными. Некоторые содержали десятки или даже более сотни вставленных фрагментов, взятых из разных хромосом, с частыми «горячими точками», которые копировались повторно. Соединения между фрагментами часто имели несколько совпадающих оснований — признак связывания на основе «микроподобия», а не аккуратного, по учебнику, восстановления. Эти паттерны убедительно указывали на механизм «копировать‑и‑вставить», известный как микроподобная медиированная репликация с прерыванием (MM‑BIR). В этом процессе разорванный конец ДНК кратко спаривается с короткой совпадающей последовательностью на другой молекуле ДНК, начинает копирование, затем отпускает и присоединяется к другому шаблону, оставляя за собой след дублированных и перестроенных сегментов. Генетические и фармакологические эксперименты показали, что этот путь зависит от сотрудничества между ферментами, обычно связанными с короткопатческим сшиванием концов, и более мощным репликационным аппаратом, способным копировать длинные участки ДНК.
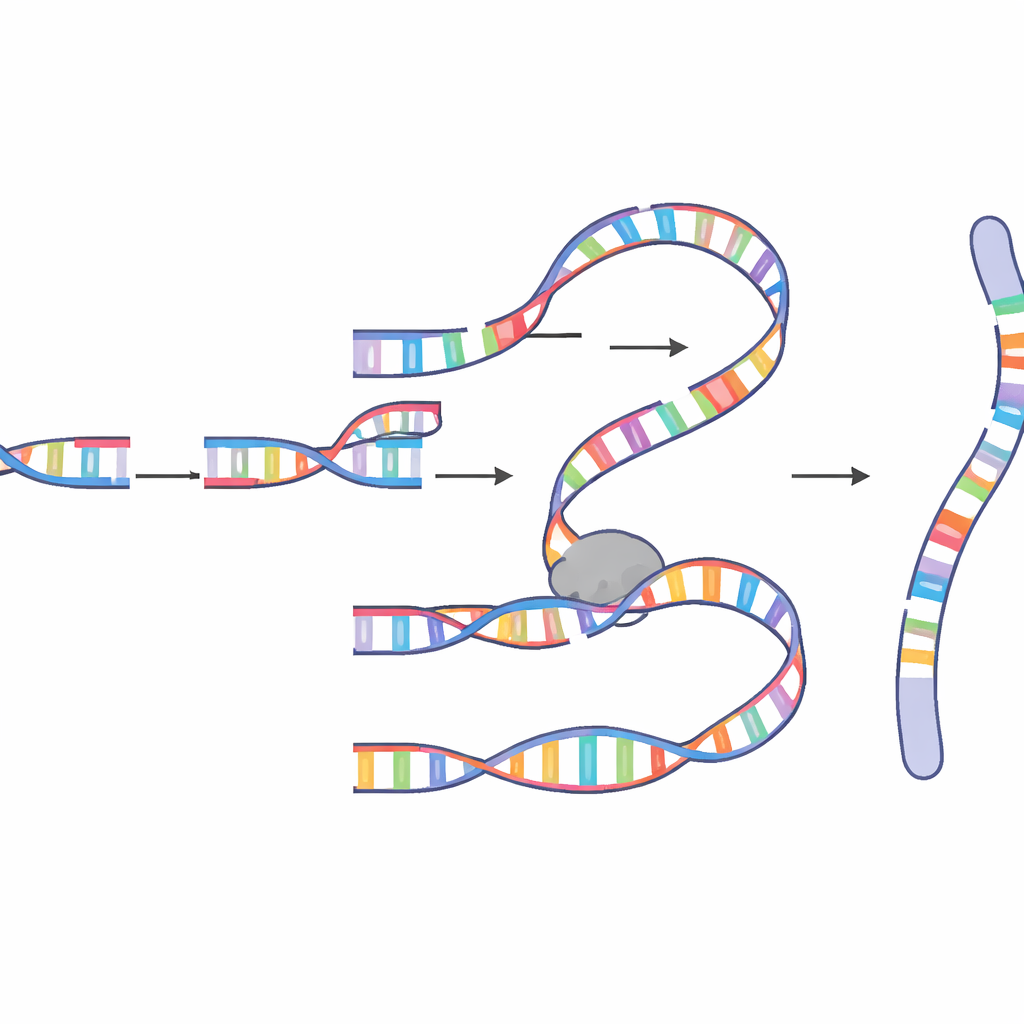
Почему митоз — опасный момент
Ключевой сюрприз заключался во времени. В этой системе хромоанасинтез возникал именно во время митоза — короткого периода деления клеток, когда хромосомы сильно конденсированы. Авторы показали, что при ослаблении контрольной точки повреждений G2/M — главного механизма защиты, блокирующего вход в митоз при наличии разрывов ДНК — сложные события происходили гораздо чаще. Они также продемонстрировали, что фермент полимераза тета, известная как «последняя черта» фактора ремонта, играет центральную роль, помогая разорванным концам найти крошечные совпадающие последовательности и запустить синтез. Более процессивные ферменты, такие как полимераза дельта, затем удлиняют новую ДНК при участии факторов вроде PIF1, POLD3 и PCNA, которые поддерживают движение репликационного механизма. При изменении этих помощников длина и шаблон вставленной ДНК менялись, что подтверждает, что хромоанасинтез вызывается специализированной митотической версией MM‑BIR, а не простым лигированием разорванных фрагментов.
Новые подсказки к раку и врожденным дефектам
В совокупности работа выявляет крайне мутагенный «аварийный» путь восстановления, который запускается, когда разорванные концы хромосом сталкиваются с митозом. Вместо аккуратного восстановления исходной последовательности митотический MM‑BIR может быстро амплифицировать и перемешивать участки генома, включая богатые генами области и потенциальные онкогены, в рамках одного события. Для здоровой клетки это рискованный, но порой неизбежный способ завершить репликацию и деление. Для прецеллюлярной клетки, однако, он может обеспечить тот самый геномный переворот, который способствует агрессивному росту опухоли или формированию сложных хромосомных изменений, наблюдаемых при врождённых расстройствах. Молекулярная детализация этого процесса открывает новые пути для понимания — и, возможно, в будущем для нацеливания — катастрофического перемешивания генома, лежащего в основе некоторых из самых тяжёлых заболеваний человека.
Цитирование: Ngo, G.H.P., Cleal, K., Seifan, S. et al. Mitotic microhomology-mediated break-induced replication promotes chromoanasynthesis. Nat Commun 17, 3375 (2026). https://doi.org/10.1038/s41467-026-70086-y
Ключевые слова: хромосомные перестройки, кризис теломер, репарация ДНК, нестабильность генома, генетика рака