Clear Sky Science · zh
调控烯香茅转移酶芳香笼占位以实现选择性高效地生成稀有C‑烯基化黄酮
为何更聪明的植物分子重要
当今许多药物和保健品来自一种被称为黄酮的植物化合物。当这些分子被小碳链构成的疏油“尾巴”修饰时,它们的生物活性常常大幅增强,在抗癌、抗感染、抗糖尿病和抗炎等方面显示出潜力。然而,这些增强型分子——称为烯基化黄酮——很难从植物或传统化学合成中以纯净和有用的数量获得。本研究描述了一种重新设计天然酶的方法,使其能够可靠且高效地构建稀有、按需定制的烯基化黄酮,为未来药物和营养补充品的更环保生产开辟了道路。 
微调植物化学的挑战
黄酮具有脆弱的多酚核心,不耐受苛刻的化学条件。在分子上精确地将一个烯基尾巴连接到指定位置并保持其余部分不被破坏,对合成化学家来说非常困难。自然界使用称为芳香烯基转移酶的酶来完成这项工作,但已知的这些酶通常活性低、选择性差且机制了解有限。因此,尽管已有上千种天然存在的烯基化黄酮被编目,许多仍然太稀少以至于难以深入研究,而最有趣的C‑烯基化品种——即尾巴直接连到碳原子上的——尤其难以按需合成。
重新编程一种多能酶
作者将注意力集中在AtaPT上,这是一种真菌来源的烯基转移酶,能作用于数十种芳香化合物,但通常活性一般并产生混合产物。通过多轮定向进化——系统性地突变并筛选数千个酶变体——他们重塑了AtaPT的活性口袋以偏好对黄酮槲皮素(kaempferol)发生特定反应。通过半随机突变与结构引导设计的结合,他们鉴定出三种功能强大的突变体。一个变体(M8)能高效地在槲皮素的8位执行一种不寻常的“反向”烯基化;另一个(G326W)把短的烯基定向到3′位;第三个(M7)以高产率和高选择性在3′位安装较长的法尼(geranyl)链。总体而言,这些酶能将单一起始黄酮转化为多种有价值的、精确修饰的产物。
发现分子对接的“笼”结构
为了解这些突变为何效果显著,团队解析了工程化酶的晶体结构并进行了分子动力学模拟。这些研究揭示了一个关键设计要点:由堆叠的芳环状氨基酸形成的“芳香笼”,环绕着黄酮分子的一部分。在M8中,一个关键突变用组氨酸取代了一个刚性的残基,有助于构建该笼并将黄酮锁定在一个姿态,使碳8完美对准以便被进入的烯基片段攻击。当使用更长的供体分子如法尼基焦磷酸(geranyl pyrophosphate)时,其尾部会伸入并填满该笼,迫使黄酮转入另一种构象,暴露出3′位。因此,仅通过改变占据笼的分子部分——以及所用供体的种类——就能切换尾巴连接的位置和偏好的烯基类型。 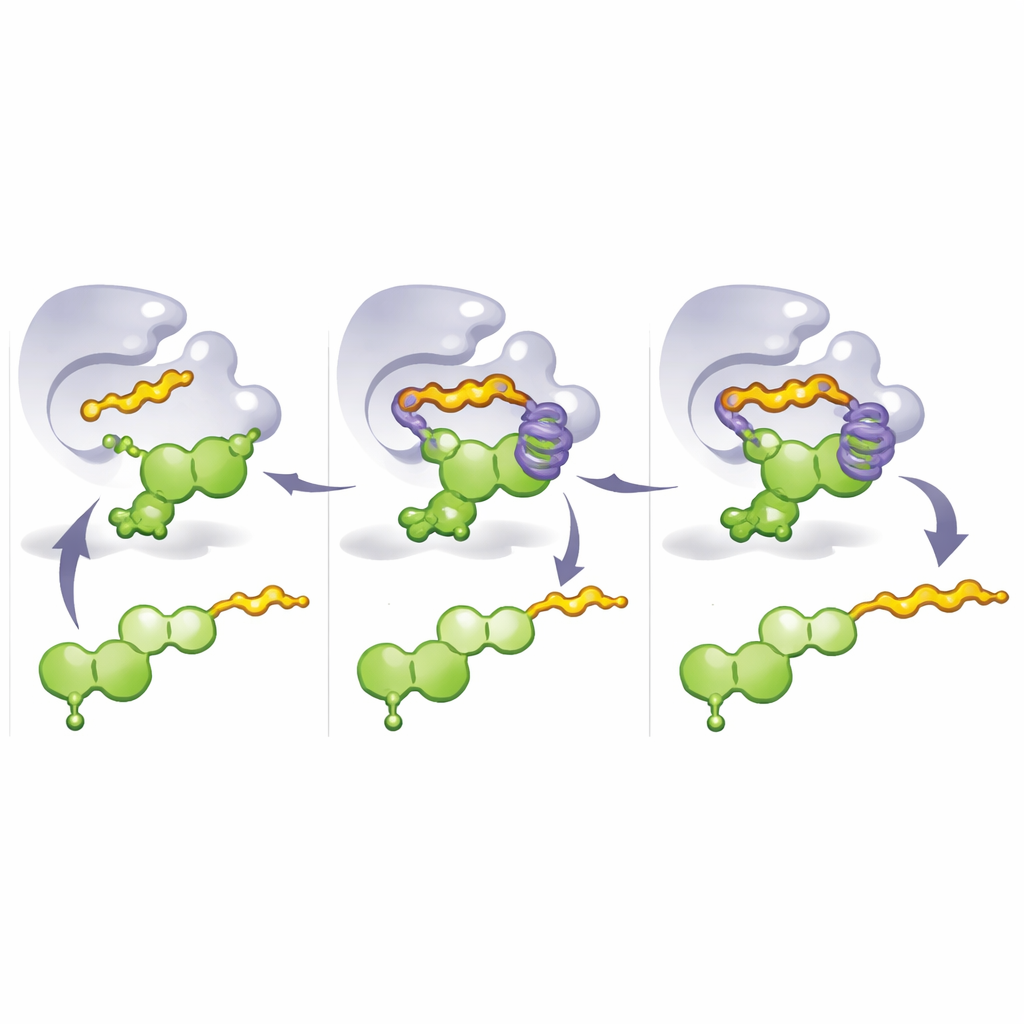
扩展蓝图并丰富目录
在掌握了这一机理图景后,研究者们测试了是否能将芳香笼的概念移植到相关酶上。通过在来自其他微生物的三种同源烯基转移酶中引入类似突变,他们显著提升了这些酶的活性和精确度,证实该笼是一个可转移的设计模体,而非单个蛋白的偶然特性。随后他们考察了26种不同的黄酮,显示工程化酶能对大多数进行烯基化,且常在确定的位置进行。合计而言,团队制备了31种烯基化黄酮,其中包括八种此前未曾报道的化合物,从而丰富了可用于生物学筛选和药物发现的结构库。
构建实用且可持续的生产线
为了将这些反应转化为可行的制造路线,作者将其工程化酶与紧凑的代谢通路耦合,使得工程化大肠杆菌(E. coli)细胞能从简单醇类如丙烯醇(prenol)或香叶醇(geraniol)内部生成反应性烯基供体。在优化的裂解液体系中,他们在制备规模上实现了高达每升400毫克的产物滴度,并成功将几种目标分子放大到升级反应。由于该过程在水相、温和温度下进行,并避免了苛刻试剂,它为从大量植物材料中提取微量产物提供了一种更环保的替代方案。
对未来药物的意义
这项工作表明,巧妙地重塑酶的一个小区域——芳香笼——可以将一个迟缓且多向的催化剂变为精确且高效的分子工具。利用这一原理,研究者们创建了一个灵活的生物催化平台,能够以高纯度和高产率制备稀有的C‑烯基化黄酮。对非专业读者来说,结论是:我们在要求生物体系按需合成复杂、定制化的类植物分子方面越来越擅长,这有望加速新疗法的发现并减少对环境的影响。
引用: Qiu, R., Huang, H., Chi, J. et al. Tuning aromatic cage occupancy in prenyltransferases enables selective and efficient production of rare c-prenylated flavonoids. Nat Commun 17, 2945 (2026). https://doi.org/10.1038/s41467-026-69706-4
关键词: 烯基化黄酮, 酶工程, 生物催化, 定向进化, 绿色化学