Clear Sky Science · pt
Ajustar a ocupação da "gaiola aromática" em preniltransferases permite produção seletiva e eficiente de flavonoides C-prenilados raros
Por que moléculas vegetais mais inteligentes importam
Muitos dos medicamentos e suplementos de saúde atuais derivam de compostos vegetais chamados flavonoides. Quando essas moléculas recebem “caudas” gordurosas formadas por pequenas cadeias de carbono, seu poder biológico frequentemente aumenta de maneira marcante, mostrando potencial contra câncer, infecções, diabetes e inflamação. No entanto, essas versões potencializadas, conhecidas como flavonoides prenilados, são difíceis de obter em forma pura e em quantidades úteis, seja a partir de plantas ou por síntese química tradicional. Este estudo descreve uma forma de reengenheirar uma enzima natural para que ela possa construir de maneira confiável e eficiente flavonoides prenilados raros e sob medida, abrindo um caminho para uma produção mais verde de futuros fármacos e nutracêuticos. 
O desafio de ajustar a química vegetal
Flavonoides compartilham um núcleo polifenólico frágil que não tolera condições químicas agressivas. Ligar uma cauda prenil em um único ponto desejado—sem alterar o restante da molécula—é difícil para químicos sintéticos. A natureza já usa enzimas chamadas preniltransferases aromáticas para essa tarefa, mas as enzimas conhecidas costumam ser lentas, pouco seletivas e pouco compreendidas. Como resultado, mais de mil flavonoides prenilados naturais foram catalogados, porém muitos continuam escassos para estudo aprofundado, e as variedades mais interessantes C‑preniladas, nas quais a cauda está ligada diretamente a um átomo de carbono, são especialmente desafiadoras de produzir sob demanda.
Reprogramando uma enzima versátil
Os autores concentraram‑se em AtaPT, uma preniltransferase fúngica que pode atuar sobre dezenas de compostos aromáticos, mas que normalmente apresenta atividade modesta e produz misturas de produtos. Utilizando rodadas de evolução dirigida—mutacionando sistematicamente e triando milhares de variantes enzimáticas—eles remodelaram o bolso ativo de AtaPT para favorecer reações específicas sobre o flavonoide kaempferol. Por meio de uma combinação de mutagênese semi‑aleatória e desenho guiado pela estrutura, identificaram três mutantes poderosos. Uma variante (M8) executa de modo eficiente uma prenilação “reversa” incomum na posição 8 do kaempferol; outra (G326W) direciona um grupo prenil curto para a posição 3′; e uma terceira (M7) instala uma cadeia geranil mais longa na posição 3′ com alto rendimento e seletividade. Juntas, essas enzimas transformam um único flavonoide de partida em vários produtos valiosos e precisamente modificados.
Descobrindo uma gaiola de acoplamento molecular
Para entender por que esses mutantes funcionaram tão bem, a equipe resolveu estruturas cristalinas das enzimas engenheiradas e realizou simulações de dinâmica molecular. Esses estudos revelaram uma característica de projeto chave: uma “gaiola aromática” formada por aminoácidos em anel empilhados que circundam parte do flavonoide. Em M8, uma mutação crítica substitui um resíduo rígido por histidina, ajudando a construir essa gaiola e a bloquear o flavonoide em uma pose onde o carbono 8 fica perfeitamente alinhado para o ataque pelo fragmento prenilador que chega. Quando um doador mais longo, como pirofosfato de geranila, é usado, sua cauda alcança e preenche essa gaiola, empurrando o flavonoide para uma conformação alternativa que expõe a posição 3′. Assim, simplesmente mudar qual parte da enzima ocupa a gaiola—e qual doador está presente—alterna o local de fixação da cauda e o tipo de cadeia preferida. 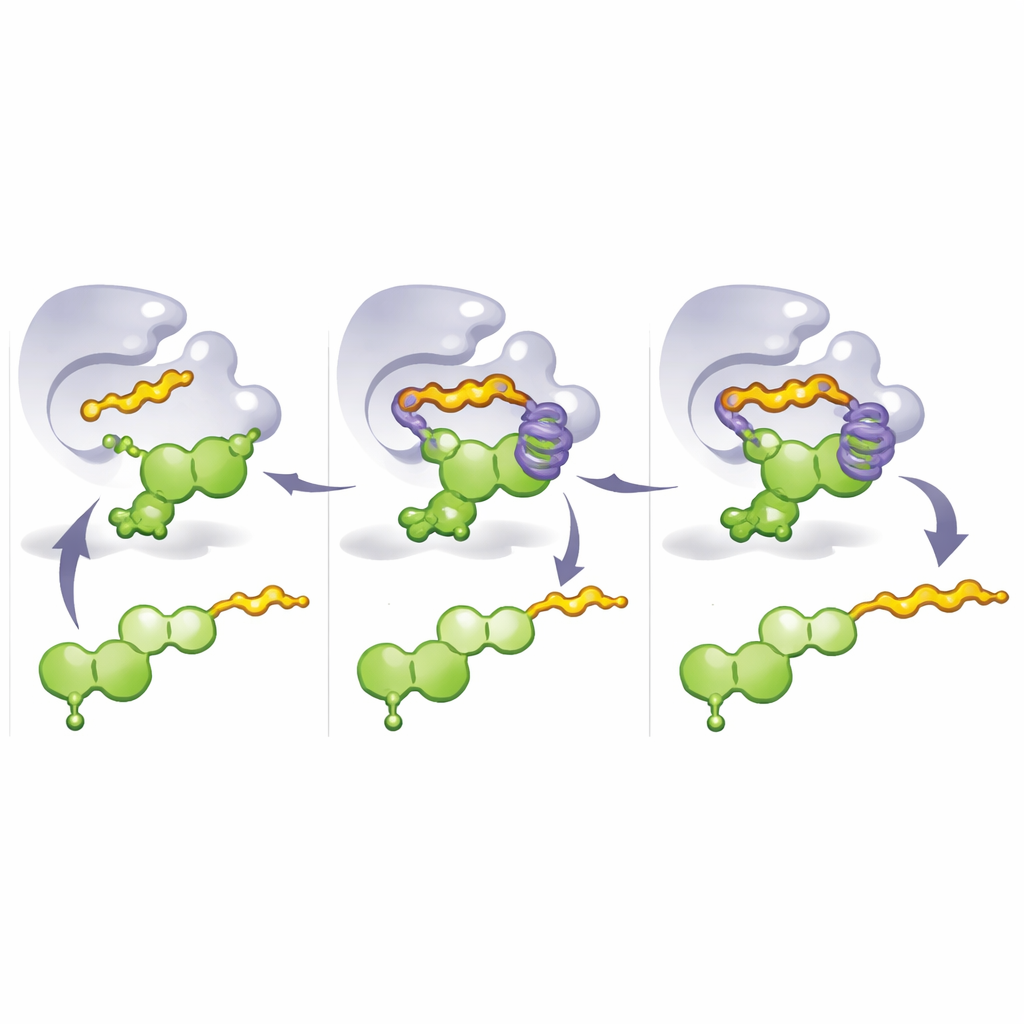
Ampliando o modelo e expandindo o catálogo
Munidos desse quadro mecanístico, os pesquisadores testaram se o conceito da gaiola aromática poderia ser exportado para enzimas relacionadas. Introduzindo mutações semelhantes em três preniltransferases homólogas de outros microrganismos, eles melhoraram dramaticamente sua atividade e precisão, confirmando que a gaiola é um motivo de desenho transferível e não uma peculiaridade de uma única proteína. Em seguida, exploraram um painel de 26 flavonoides diferentes, demonstrando que as enzimas engenheiradas puderam prenilar a maioria deles, frequentemente em posições definidas. Ao todo, a equipe preparou 31 flavonoides prenilados, incluindo oito compostos nunca antes relatados, ampliando a paleta de estruturas disponíveis para testes biológicos e descoberta de fármacos.
Construindo uma linha de produção prática e sustentável
Para transformar essas reações em uma rota de fabricação viável, os autores acoplaram suas enzimas engenheiradas a vias metabólicas compactas que geram os doadores prenil reativos dentro de células de E. coli engenheiradas a partir de álcoois simples, como prenol ou geraniol. Em sistemas otimizados baseados em lisados, alcançaram títulos de produto de até 400 miligramas por litro em escalas preparativas, e escalaram com sucesso várias moléculas‑alvo para reações em volume de litro. Como o processo ocorre em água, em temperaturas moderadas, e evita reagentes agressivos, oferece uma alternativa ambientalmente amigável à extração de quantidades traço de produto a partir de toneladas de material vegetal.
O que isso significa para medicamentos futuros
Este trabalho mostra que remodelar de forma inteligente uma pequena região de uma enzima—a gaiola aromática—pode transformar um catalisador lento e promíscuo em uma ferramenta molecular precisa e eficiente. Ao aproveitar esse princípio, os pesquisadores criaram uma plataforma biocatalítica flexível para produzir flavonoides C‑prenilados raros com alta pureza e rendimento. Para não especialistas, a conclusão é que estamos cada vez melhores em pedir aos sistemas vivos que construam moléculas vegetais complexas e sob medida sob comando, potencialmente acelerando a busca por novos tratamentos ao mesmo tempo em que reduzem o impacto ambiental.
Citação: Qiu, R., Huang, H., Chi, J. et al. Tuning aromatic cage occupancy in prenyltransferases enables selective and efficient production of rare c-prenylated flavonoids. Nat Commun 17, 2945 (2026). https://doi.org/10.1038/s41467-026-69706-4
Palavras-chave: flavonoides prenilados, engenharia de enzimas, biocatálise, evolução dirigida, química sustentável