Clear Sky Science · nl
Het afstemmen van de bezetting van de aromatische kooi in prenyltransferases maakt selectieve en efficiënte productie van zeldzame C‑prenyleerde flavonoïden mogelijk
Waarom slimere plantmoleculen ertoe doen
Veel van de medicijnen en voedingssupplementen van vandaag zijn afgeleid van plantchemicaliën die flavonoïden worden genoemd. Wanneer deze moleculen worden voorzien van vette “staarten” bestaande uit korte koolstofketens, neemt hun biologische werkzaamheid vaak sterk toe en tonen ze potentie tegen kanker, infecties, diabetes en ontsteking. Deze versterkte versies, bekend als prenyleerde flavonoïden, zijn echter moeilijk in zuivere vorm en in nuttige hoeveelheden te verkrijgen uit zowel planten als traditionele chemische synthese. Deze studie beschrijft een manier om een natuurlijk enzym zodanig te herontwerpen dat het betrouwbaar en efficiënt zeldzame, op maat gemaakte prenyleerde flavonoïden kan bouwen, waarmee een pad wordt geopend naar groenere productie van toekomstige geneesmiddelen en nutraceuticals. 
De uitdaging van het verfijnen van plantchemie
Flavonoïden delen een kwetsbare, polyfenolische kern die niet tegen harde chemische omstandigheden kan. Een prenylstaart op precies één gewenste plaats vastmaken—terwijl de rest van het molecuul onaangetast blijft—is moeilijk voor synthetische chemici. De natuur gebruikt al enzymen genaamd aromatische prenyltransferases om dit te doen, maar de bekende enzymen zijn vaak traag, slecht selectief en niet goed begrepen. Daarom zijn er meer dan duizend natuurlijk voorkomende prenyleerde flavonoïden gecatalogiseerd, maar velen blijven te schaars om grondig te bestuderen, en de meest interessante “C‑prenyleerde” varianten, waarbij de staart direct aan een koolstofatoom is gebonden, zijn bijzonder moeilijk op aanvraag te maken.
Een veelzijdig enzym herprogrammeren
De auteurs richtten zich op AtaPT, een schimmel‑prenyltransferase dat op tientallen aromatische verbindingen kan werken maar normaal gesproken slechts matige activiteit vertoont en mengsels van producten produceert. Met behulp van ronden van directed evolution—systematisch muteren en screenen van duizenden enzymvarianten—vormden ze de actieve pocket van AtaPT zodanig dat specifieke reacties op het flavonoïde kaempferol werden bevoordeeld. Door een combinatie van semi‑willekeurige mutagenese en structuurgeïnformeerd ontwerp identificeerden ze drie krachtige mutanten. Eén variant (M8) voert efficiënt een ongebruikelijke “reverse” prenylatie uit op de 8‑positie van kaempferol; een andere (G326W) dirigeert een korte prenylgroep naar de 3′‑positie; en een derde (M7) plaatst een langere geranylketen op de 3′‑positie met hoge opbrengst en selectiviteit. Samen veranderen deze enzymen één startflavonoïde in meerdere waardevolle, precies gemodificeerde producten.
Het ontdekken van een moleculaire dockingskooi
Om te begrijpen waarom deze mutanten zo goed werkten, loste het team kristalstructuren van de ontworpen enzymen op en voerde moleculaire dynamicasimulaties uit. Deze studies onthulden een belangrijk ontwerpelement: een “aromatische kooi” gevormd door gestapelde ringvormige aminozuren rond een deel van het flavonoïde. In M8 vervangt een cruciale mutatie een star residu door histidine, wat helpt deze kooi op te bouwen en het flavonoïde te vergrendelen in een houding waarin koolstof 8 perfect is uitgelijnd voor aanval door het binnenkomende prenylfragment. Wanneer een langer donormolecuul zoals geranylpyrofosfaat wordt gebruikt, reikt zijn staart in deze kooi en vult die op, waardoor het flavonoïde in een alternatieve conformatie wordt gedrukt die de 3′‑positie blootlegt. Simpelweg veranderen welk deel van het enzym de kooi bezet—en welke donor aanwezig is—verschuift dus waar de staart wordt aangehecht en welk soort keten wordt geprefereerd. 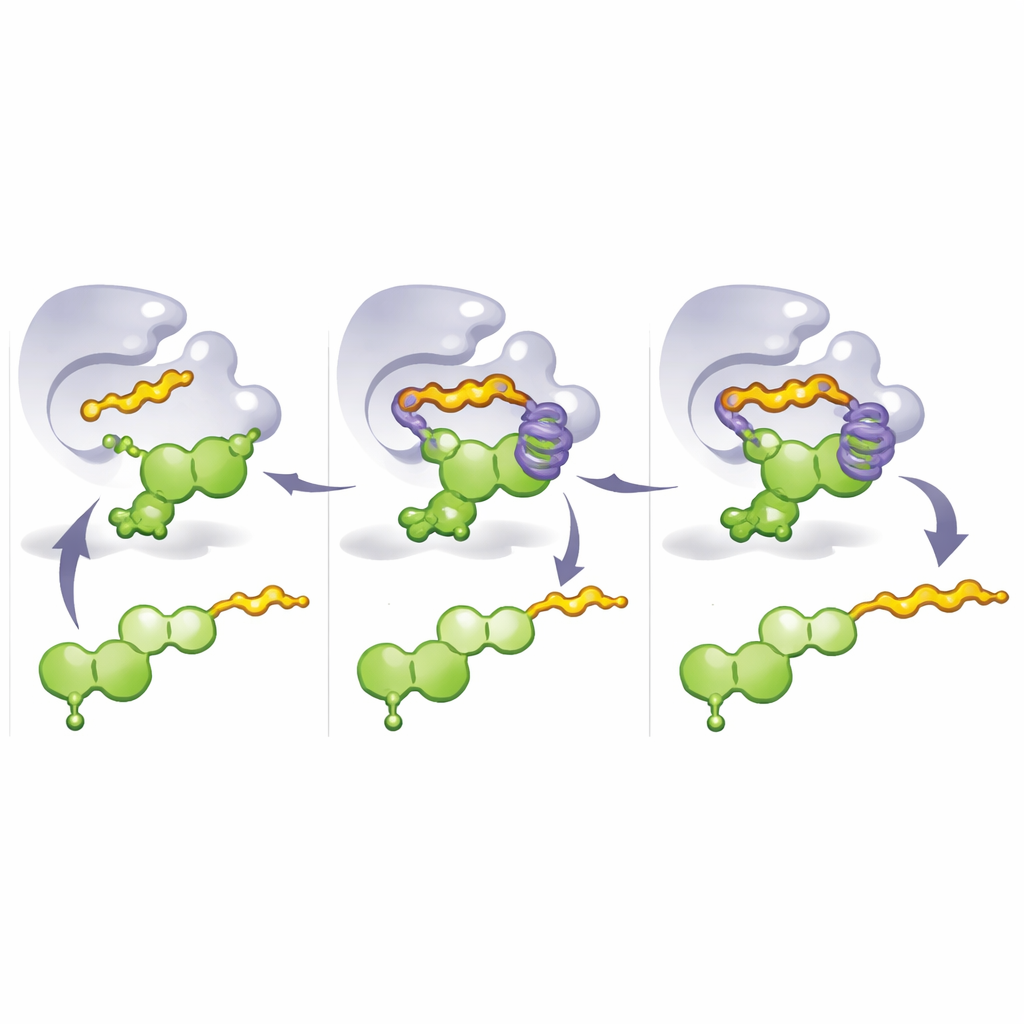
Het bouwplan uitbreiden en de catalogus verbreden
Gewapend met dit mechanistische beeld testten de onderzoekers of het aromatische kooi‑concept kon worden overgebracht naar verwante enzymen. Door vergelijkbare mutaties in te voeren in drie homologe prenyltransferases uit andere microben verbeterden ze hun activiteit en precisie dramatisch, waarmee werd bevestigd dat de kooi een overdraagbaar ontwerpmotief is en geen eigenaardigheid van één eiwit. Ze onderzochten vervolgens een panel van 26 verschillende flavonoïden en toonden aan dat de ontworpen enzymen de meeste daarvan konden prenyleren, vaak op gedefinieerde posities. In totaal bereidde het team 31 prenyleerde flavonoïden, waaronder acht verbindingen die nog nooit eerder waren gerapporteerd, waarmee het palet aan structuren voor biologische testen en geneesmiddelenontdekking werd verrijkt.
Een praktische, duurzame productielijn bouwen
Om deze reacties tot een levensvatbare productieroute te maken, koppelden de auteurs hun ontworpen enzymen aan compacte metabole routes die de reactieve prenyldonoren binnen ontworpen E. coli‑cellen genereren uit eenvoudige alcoholen zoals prenol of geraniol. In geoptimaliseerde lysaat‑gebaseerde systemen bereikten ze producttiter tot 400 milligram per liter op preparatieve schaal, en schaaldeden ze meerdere doelmoleculen succesvol op liter‑volume reacties. Omdat het proces in water verloopt, bij milde temperaturen en zonder agressieve reagentia, biedt het een milieuvriendelijk alternatief voor het winnen van sporen hoeveelheden product uit tonnen plantmateriaal.
Wat dit betekent voor toekomstige medicijnen
Dit werk laat zien dat het slim herschikken van een klein deel van een enzym—de aromatische kooi—een trage, promiscuïteit vertonende katalysator kan veranderen in een nauwkeurig en efficiënt moleculair werktuig. Door dit principe te benutten, creëerden de onderzoekers een flexibel biokatalytisch platform voor het vervaardigen van zeldzame C‑prenyleerde flavonoïden met hoge zuiverheid en opbrengst. Voor niet‑specialisten is de conclusie dat we veel beter worden in het vragen aan levende systemen om complexe, op maat gemaakte plantaardige‑achtige moleculen op commando te bouwen, wat mogelijk het zoeken naar nieuwe behandelingen versnelt en de milieuimpact vermindert.
Bronvermelding: Qiu, R., Huang, H., Chi, J. et al. Tuning aromatic cage occupancy in prenyltransferases enables selective and efficient production of rare c-prenylated flavonoids. Nat Commun 17, 2945 (2026). https://doi.org/10.1038/s41467-026-69706-4
Trefwoorden: prenyleerde flavonoïden, enzymengineering, biokatalyse, directed evolution, groene chemie