Clear Sky Science · ar
ضبط إشغال القفص العطري في برينيل ترانسفيرازات يمكّن الإنتاج الانتقائي والفعّال للفلافونويدات القليلة الـ C-برينيلية
لماذا جزيئات النباتات الأذكى مهمة
تأتي كثير من الأدوية والمكمِّلات الصحية اليوم من مركبات نباتية تُسمى الفلافونويدات. عندما تُزوَّد هذه الجزيئات بذُيول دهنية قصيرة مكوَّنة من سلاسل كربونية، غالبًا ما تزداد فعاليتها البيولوجية بشكل كبير، ما يفتح آفاقًا مضادة للسرطان والعدوى والسكري والالتهاب. ومع ذلك، فإن هذه النسخ المعزَّزة، المعروفة بالفلافونويدات البرينيلية، يصعب الحصول عليها بنقاء وكميات مناسبة من النباتات أو عبر التخليق الكيميائي التقليدي. تصف هذه الدراسة طريقة لإعادة هندسة إنزيم طبيعي ليتمكن بشكل موثوق وفعّال من بناء فلافونويدات برينيلية نادرة ومصممة خصيصًا، فتفتح مسارًا لإنتاج أكثر خضرة للأدوية والمغذيات المستقبلية. 
تحدي ضبط كيمياء النبات بدقة
تشارك الفلافونويدات جوهرًا بوليفينوليًا هشًا لا يتحمّل ظروفًا كيميائية قاسية. إن ربط ذيل برينيل في موضع واحد محدد—مع ترك بقية الجزيء دون تبديل—هو أمر صعب على الكيميائيين التخليقيين. تستخدم الطبيعة بالفعل إنزيمات تُسمّى برينيل ترانسفيرازات عطرية لأداء هذه المهمة، لكن الإنزيمات المعروفة غالبًا ما تكون بطيئة، قليلة الاختيار، وغير مفهومة جيدًا. نتيجة لذلك، تم تسجيل أكثر من ألف فلافونويد برينيل طبيعي، ومع ذلك يبقى كثير منها نادرًا بدرجة تمنع دراسته تفصيليًا، والأنواع الأكثر إثارة للاهتمام —«C-برينيلية» حيث يرتبط الذيل مباشرة بذرة كربون—تُعدّ تحديًا خاصًا للتصنيع حسب الطلب.
إعادة برمجة إنزيم متعدد الاستخدامات
ركز المؤلفون على AtaPT، وهو برينيل ترانسفيراز فطري يمكنه العمل على عشرات المركبات العطرية لكنه عادةً ما يظهر نشاطًا متواضعًا وينتج خليطًا من المنتجات. باستخدام جولات من التطور الموجَّه—تغييرُ الطفرات وفحصُ آلاف متغيرات الإنزيم بشكل منهجي—أعادوا تشكيل جيب الفاعلية في AtaPT لتفضيل تفاعلات محددة على الفلافونويد كامبفيرول. من خلال مزيج من الطفرات شبه العشوائية والتصميم المبني على البنية، حددوا ثلاثة طفرات قوية. أحد المتغيرات (M8) ينفذ بكفاءة برينلة "عكسية" غير معتادة عند الوضع 8 من كامبفيرول؛ ومتغير آخر (G326W) يوجه مجموعة برينيل قصيرة إلى الموضع 3′؛ وثالث (M7) يركب سلسلة جيرانيلية أطول في الموضع 3′ بعوائد وانتقائية عالية. معًا، تحول هذه الإنزيمات فلافونويدًا بداية واحدًا إلى عدة منتجات قيمة ومعدلة بدقة.
اكتشاف قفص تثبيت جزيئي
لفهم سبب فعالية هذه الطفرات، حلّل الفريق هياكل بلورية للإنزيمات المهندَسة وأجرى محاكاة ديناميكيات جزيئية. كشفت هذه الدراسات ميزة تصميمية رئيسية: "قفص عطري" يتكوّن من أحماض أمينية حلقية مترابطة تحيط بجزء من الفلافونويد. في M8، تستبدل طفرة حاسمة بقاعدة صلبة بهستيدين، ما يساعد على بناء هذا القفص وقفل الفلافونويد في وضع حيث يكون الكربون 8 محاذيًا تمامًا لهجوم قطعة البرينيل الواردة. عندما يُستخدم ناقل أطول مثل جيرانيل بيوفوسفات، يمتد ذيله إلى داخل هذا القفص ويملأه بدلاً من ذلك، ليندفع الفلافونويد إلى توافقية بديلة تكشف الموضع 3′. وهكذا، فإن تغيير أي جزء من الإنزيم يشغل القفص—وأي ناقل حاضر—يبدّل مكان ارتباط الذيل ونوع السلسلة المفضّل. 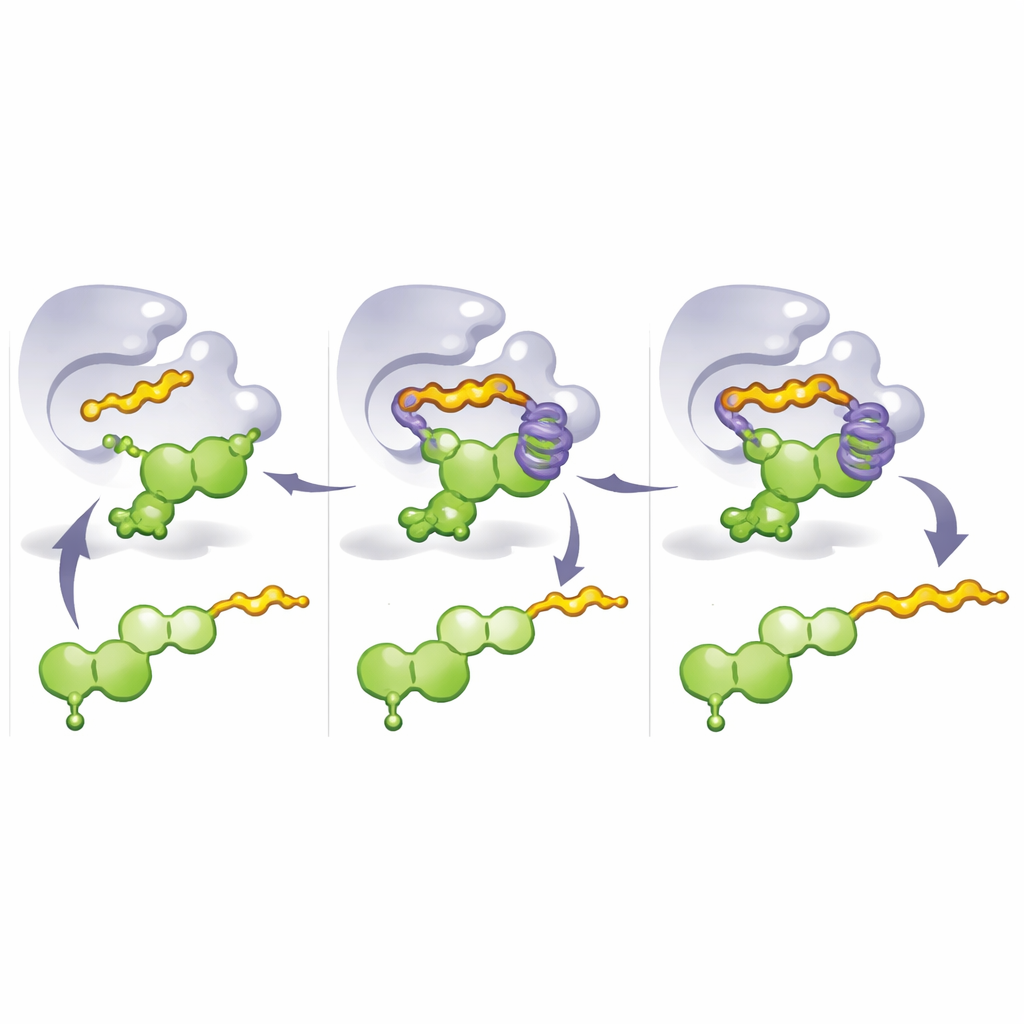
توسيع المخطط وتوسيع الكتالوج
مسلحين بهذه الصورة الآلية، اختبر الباحثون ما إذا كان مفهوم القفص العطري يمكن نقله إلى إنزيمات قريبة. عبر إدخال طفرات مماثلة في ثلاثة برينيل ترانسفيرازات متجانسة من ميكروبات أخرى، حسّنوا نشاطها ودقّتها بشكل كبير، مؤكدين أن القفص هو نموذج تصميم قابل للنقل وليس خصوصية لبروتين واحد. ثم استعرضوا لوحة مكوّنة من 26 فلافونويدًا مختلفًا، مظهرين أن الإنزيمات المهندَسة استطاعت برينلة معظمها، غالبًا في مواضع محددة. في المجموع، أعدّ الفريق 31 فلافونويدًا برينيلًا، بما في ذلك ثمانية مركبات لم تُبلّغ من قبل، موسعين بذلك مجموعة البنى المتاحة للاختبار البيولوجي واكتشاف الأدوية.
بناء خط إنتاج عملي ومستدام
لتحويل هذه التفاعلات إلى مسار صناعي قابل للتطبيق، ربط المؤلفون إنزيماتهم المهندَسة بمسارات أيضية مدمجة تولّد ناقلات البرينيل التفاعلية داخل خلايا E. coli مُهندَسة من كحوليات بسيطة مثل البرينول أو الجيرانول. في أنظمة قائمة على المستخلصات المحسّنة، حققوا تركيزات منتج تصل إلى 400 ملليغرام لكل لتر على مقاييس تحضيرية، ونفذوا بنجاح تحجيم عدة جزيئات مستهدفة لتفاعلات بحجم لتر. وبما أن العملية تتم في الماء، وفي درجات حرارة معتدلة، وتتجنّب المواد القاسية، فإنها تقدّم بديلاً صديقًا للبيئة لاستخراج كميات ضئيلة من المنتج من أطنان من المادة النباتية.
ما يعنيه هذا للأدوية المستقبلية
تُظهر هذه الدراسة أن إعادة تشكيل منطقة صغيرة من الإنزيم—القفص العطري—يمكن أن يحول محفزًا بطيئًا وغير انتقائي إلى أداة جزيئية دقيقة وفعّالة. من خلال استغلال هذا المبدأ، أنشأ الباحثون منصة تحفيز حيوي مرنة لصنع فلافونويدات C-برينيلية نادرة بنقاء وعائد عالٍ. للمطّلع غير المتخصّص، الخلاصة هي أننا نصبح أفضل بكثير في توجيه الأنظمة الحية لبناء مركبات نباتية معقّدة ومصممة حسب الطلب، ما قد يسرع البحث عن علاجات جديدة ويقلّل الأثر البيئي.
الاستشهاد: Qiu, R., Huang, H., Chi, J. et al. Tuning aromatic cage occupancy in prenyltransferases enables selective and efficient production of rare c-prenylated flavonoids. Nat Commun 17, 2945 (2026). https://doi.org/10.1038/s41467-026-69706-4
الكلمات المفتاحية: الفلافونويدات البرينيلية, هندسة الإنزيمات, التحفيز الحيوي, التطور الموجّه, الكيمياء الخضراء