Clear Sky Science · sv
Finjustering av aromatiska korgens upptag i prenyltransferaser möjliggör selektiv och effektiv produktion av sällsynta c‑prenylated flavonoider
Varför smartare växtmolekyler spelar roll
Många av dagens läkemedel och kosttillskott kommer från växtkemikalier som kallas flavonoider. När dessa molekyler dekoreras med fettliknande ”svansar” bestående av små kolkedjor ökar deras biologiska effekt ofta dramatiskt, vilket visar löfte mot cancer, infektioner, diabetes och inflammation. Men dessa förstärkta varianter, kända som prenylated flavonoider, är svåra att få i ren form och i användbara mängder varken från växter eller traditionell kemisk syntes. Denna studie beskriver ett sätt att omkonstruera ett naturligt enzym så att det tillförlitligt och effektivt kan bygga sällsynta, skräddarsydda prenylated flavonoider, vilket öppnar en väg till grönare produktion av framtida läkemedel och nutraceuticals. 
Utmaningen i att finjustera växtkemi
Flavonoider delar en skör, polyfenolisk kärna som inte tål hårda kemiska förhållanden. Att fästa en prenylsvans på precis en önskad plats—utan att påverka resten av molekylen—är svårt för syntetiska kemister. Naturen använder redan enzymer som kallas aromatiska prenyltransferaser för denna uppgift, men de kända enzymerna är ofta långsamma, dåligt selektiva och inte väl förstådda. Som ett resultat har mer än tusen naturligt förekommande prenylated flavonoider katalogiserats, men många förblir för sällsynta för att studeras noggrant, och de mest intressanta ”C‑prenylated” varianterna, där svansen är direkt bunden till en kolatom, är särskilt svåra att framställa på begäran.
Omkodning av ett mångsidigt enzym
Författarna fokuserade på AtaPT, en svamp‑prenyltransferas som kan verka på dussintals aromatiska föreningar men normalt visar måttlig aktivitet och ger produktblandningar. Genom omgångar av riktad evolution—systematiskt muterande och screens av tusentals enzymvarianter—formade de om AtaPT:s aktiva ficka för att gynna specifika reaktioner på flavonoiden kaempferol. Genom en kombination av semi‑slumpmässig mutagenes och strukturguidade designidentifierade de tre kraftfulla mutanter. En variant (M8) utför effektivt en ovanlig ”reverse” prenylering vid 8‑positionen av kaempferol; en annan (G326W) riktar en kort prenylgrupp till 3′‑positionen; och en tredje (M7) installerar en längre geranylkedja vid 3′‑positionen med hög utbyte och selektivitet. Tillsammans omvandlar dessa enzymer en enda utgångsflavonoid till flera värdefulla, precist modifierade produkter.
Upptäckten av en molekylär dockningskorg
För att förstå varför dessa mutanter fungerade så bra löste teamet kristallstrukturer av de konstruerade enzymerna och körde molekyldynamiksimuleringar. Dessa studier avslöjade en viktig designfunktion: en ”aromatisk korg” bildad av staplade ringformade aminosyror som omsluter en del av flavonoiden. I M8 ersätter en kritisk mutation en stel rest med histidin, vilket hjälper till att bygga denna korg och låser flavonoiden i en position där kol 8 är perfekt inriktat för attack av den inkommande prenylfragmentet. När en längre donormolekyl som geranylpyrofosfat används, når dess svans in i och fyller denna korg istället, vilket pressar flavonoiden till en alternativ konformation som exponerar 3′‑positionen. Alltså, genom att helt enkelt ändra vilken del av enzymet som upptar korgen—och vilken donor som är närvarande—växlar man var svansen fästs och vilken typ av kedja som föredras. 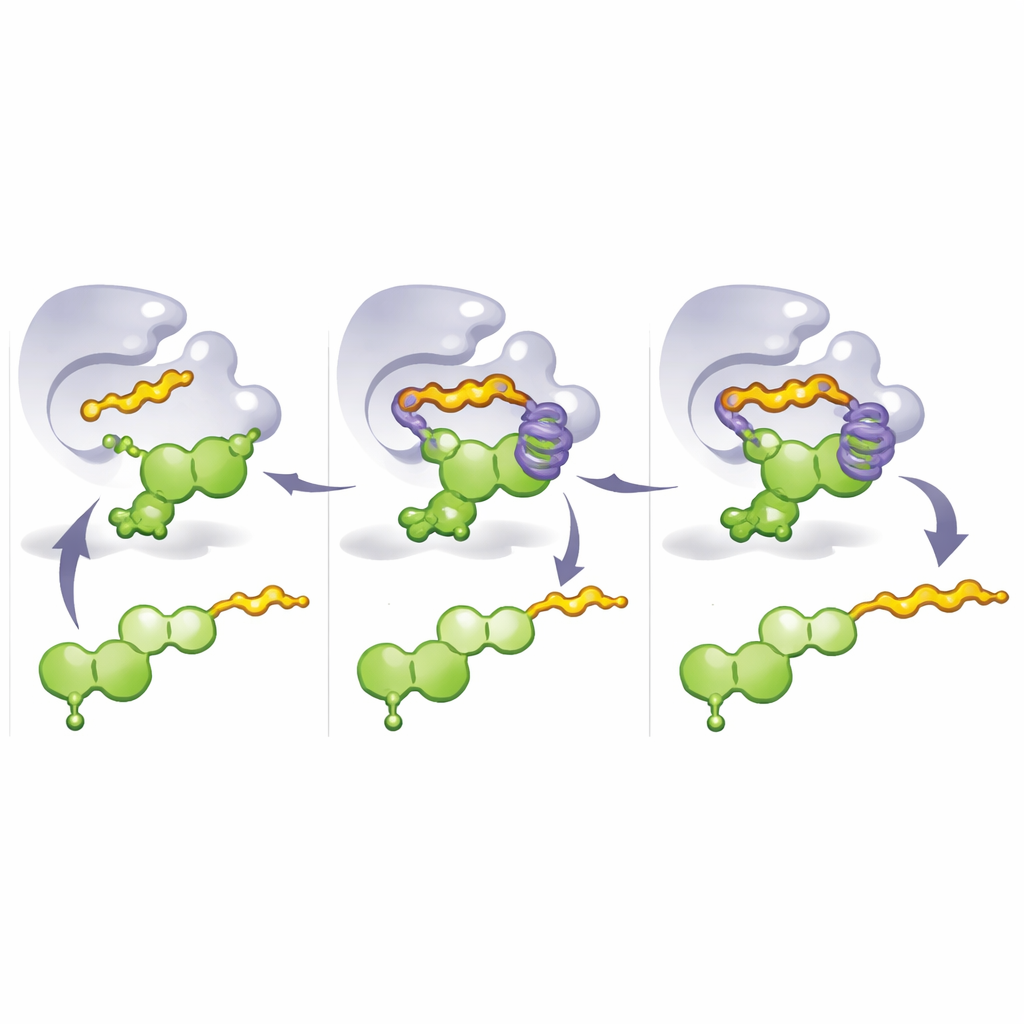
Utvidgning av ritningen och breddning av katalogen
Utrustade med denna mekanistiska bild testade forskarna om konceptet med den aromatiska korgen kunde överföras till besläktade enzymer. Genom att införa liknande mutationer i tre homologa prenyltransferaser från andra mikrober förbättrade de dramatiskt deras aktivitet och precision, vilket bekräftar att korgen är ett överförbart designmotiv snarare än en egendomlighet hos ett enda protein. De utforskade därefter en panel av 26 olika flavonoider och visade att de konstruerade enzymerna kunde prenylera de flesta av dem, ofta på definierade positioner. Totalt förberedde teamet 31 prenylated flavonoider, inklusive åtta föreningar som aldrig tidigare rapporterats, och berikade därigenom paletten av strukturer tillgängliga för biologisk testning och läkemedelsupptäckt.
Att bygga en praktisk, hållbar produktionslinje
För att omvandla dessa reaktioner till en praktikbar tillverkningsväg kopplade författarna sina konstruerade enzymer till kompakta metaboliska vägar som genererar de reaktiva prenyl donorerna inne i konstruerade E. coli-celler från enkla alkoholer såsom prenol eller geraniol. I optimerade lysatbaserade system uppnådde de produkttitrar upp till 400 milligram per liter i preparativa skalor, och de kunde framgångsrikt skala flera mål‑molekyler till litervolymreaktioner. Eftersom processen körs i vatten, vid milda temperaturer och undviker hårda reagenser, erbjuder den ett miljövänligt alternativ till att extrahera spårmängder av produkt från tonvis av växtmaterial.
Vad detta betyder för framtida läkemedel
Detta arbete visar att en smart omformning av en liten region i ett enzym—den aromatiska korgen—kan förvandla en långsam, promiscuös katalysator till ett precist och effektivt molekylärt verktyg. Genom att utnyttja denna princip skapade forskarna en flexibel biokatalytisk plattform för att tillverka sällsynta C‑prenylated flavonoider med hög renhet och utbyte. För icke‑specialister är slutsatsen att vi blir mycket bättre på att be levande system bygga komplexa, skräddarsydda växtliga molekyler på begäran, vilket potentiellt kan påskynda sökandet efter nya behandlingar samtidigt som miljöpåverkan minskar.
Citering: Qiu, R., Huang, H., Chi, J. et al. Tuning aromatic cage occupancy in prenyltransferases enables selective and efficient production of rare c-prenylated flavonoids. Nat Commun 17, 2945 (2026). https://doi.org/10.1038/s41467-026-69706-4
Nyckelord: prenylated flavonoider, enzymteknik, biokatalys, riktad evolution, grön kemi