Clear Sky Science · es
Ajustar la ocupación de la jaula aromática en preniltransferasas permite la producción selectiva y eficiente de raros flavonoides C-prenilados
Por qué importan moléculas vegetales más inteligentes
Muchos de los medicamentos y suplementos de salud actuales proceden de compuestos vegetales llamados flavonoides. Cuando estas moléculas se decoran con "colas" grasosas formadas por pequeñas cadenas de carbono, su potencia biológica suele aumentar de forma notable, mostrando potencial frente al cáncer, las infecciones, la diabetes y la inflamación. Sin embargo, estas versiones potenciadas, conocidas como flavonoides prenilados, son difíciles de obtener en forma pura y en cantidades útiles tanto a partir de plantas como por síntesis química tradicional. Este estudio describe una forma de reingeniería de una enzima natural para que pueda construir de manera fiable y eficiente flavonoides prenilados raros y hechos a medida, abriendo un camino hacia una producción más ecológica de futuros fármacos y nutracéuticos. 
El desafío de afinar la química vegetal
Los flavonoides comparten un núcleo polifenólico frágil que no tolera condiciones químicas agresivas. Añadir una cola prenil en un único lugar deseado—dejar intacto el resto de la molécula—es difícil para los químicos sintéticos. La naturaleza ya utiliza enzimas llamadas preniltransferasas aromáticas para realizar este trabajo, pero las enzimas conocidas suelen ser lentas, poco selectivas y no están bien comprendidas. Como resultado, se han catalogado más de mil flavonoides prenilados de origen natural, pero muchos siguen siendo demasiado escasos para estudiarse a fondo, y las variedades más interesantes «C-preniladas», donde la cola se une directamente a un átomo de carbono, son especialmente difíciles de fabricar a demanda.
Reprogramando una enzima versátil
Los autores se centraron en AtaPT, una preniltransferasa fúngica que puede actuar sobre docenas de compuestos aromáticos pero que normalmente muestra una actividad modesta y produce mezclas de productos. Mediante rondas de evolución dirigida—mutando y cribando sistemáticamente miles de variantes enzimáticas—moldearon el bolsillo activo de AtaPT para favorecer reacciones específicas sobre el flavonoide kaempferol. A través de una combinación de mutagénesis semialeatoria y diseño guiado por estructura, identificaron tres mutantes potentes. Una variante (M8) realiza de forma eficiente una prenilación inusual "inversa" en la posición 8 del kaempferol; otra (G326W) dirige un grupo prenil corto a la posición 3′; y una tercera (M7) instala una cadena geranil más larga en la posición 3′ con alto rendimiento y selectividad. En conjunto, estas enzimas transforman un único flavonoide inicial en varios productos valiosos y modificados con precisión.
Descubriendo una jaula de acoplamiento molecular
Para entender por qué estos mutantes funcionaban tan bien, el equipo resolvió estructuras cristalinas de las enzimas diseñadas y realizó simulaciones de dinámica molecular. Estos estudios revelaron una característica clave de diseño: una "jaula aromática" formada por aminoácidos con anillos apilados que rodean parte del flavonoide. En M8, una mutación crítica sustituye un residuo rígido por histidina, contribuyendo a construir esta jaula y bloqueando el flavonoide en una orientación donde el carbono 8 queda perfectamente alineado para el ataque del fragmento prenil entrante. Cuando se utiliza un donante más largo, como el pirofosfato de geranilo, su cola alcanza y llena esta jaula, desplazando al flavonoide a una conformación alternativa que expone la posición 3′. Así, simplemente cambiando qué parte de la enzima ocupa la jaula—y qué donante está presente—se altera el lugar de unión de la cola y el tipo de cadena preferida. 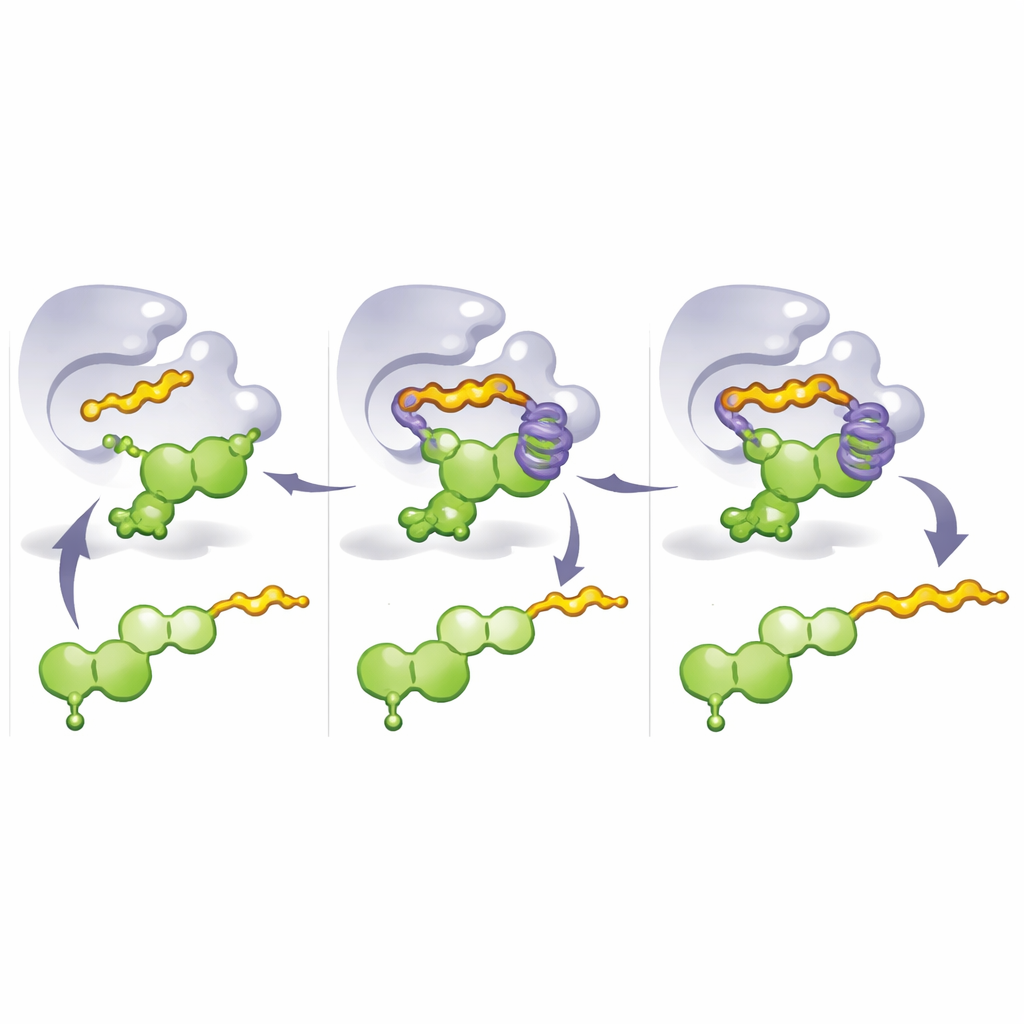
Ampliando el plano y ensanchando el catálogo
Armados con este cuadro mecanístico, los investigadores probaron si el concepto de la jaula aromática podía transferirse a enzimas relacionadas. Introduciendo mutaciones similares en tres preniltransferasas homólogas de otros microbios, mejoraron drásticamente su actividad y precisión, confirmando que la jaula es un motivo de diseño transferible y no una peculiaridad de una única proteína. Luego exploraron un panel de 26 flavonoides diferentes, demostrando que las enzimas diseñadas podían prenilar la mayoría de ellos, a menudo en posiciones definidas. En total, el equipo preparó 31 flavonoides prenilados, incluidos ocho compuestos nunca antes reportados, enriqueciendo así la paleta de estructuras disponibles para pruebas biológicas y descubrimiento de fármacos.
Construyendo una línea de producción práctica y sostenible
Para convertir estas reacciones en una ruta de fabricación viable, los autores acoplaron sus enzimas diseñadas con rutas metabólicas compactas que generan los donantes prenil reactivos dentro de células de E. coli diseñadas a partir de alcoholes simples como prenol o geraniol. En sistemas optimizados basados en lisados, alcanzaron titulaciones de producto de hasta 400 miligramos por litro a escala preparativa, y escalaron con éxito varias moléculas objetivo hasta reacciones de volumen en litros. Dado que el proceso funciona en agua, a temperaturas suaves y evita reactivos agresivos, ofrece una alternativa respetuosa con el medio ambiente frente a la extracción de trazas de producto de toneladas de material vegetal.
Qué significa esto para futuros medicamentos
Este trabajo demuestra que remodelar de forma inteligente una pequeña región de una enzima—la jaula aromática—puede convertir un catalizador lento y promiscuo en una herramienta molecular precisa y eficiente. Aprovechando este principio, los investigadores crearon una plataforma biocatalítica flexible para fabricar raros flavonoides C-prenilados con alta pureza y rendimiento. Para el público no especializado, la conclusión es que somos cada vez mejores pidiendo a los sistemas vivos que construyan moléculas complejas y a medida similares a las vegetales bajo demanda, lo que podría acelerar la búsqueda de nuevos tratamientos y reducir el impacto ambiental.
Cita: Qiu, R., Huang, H., Chi, J. et al. Tuning aromatic cage occupancy in prenyltransferases enables selective and efficient production of rare c-prenylated flavonoids. Nat Commun 17, 2945 (2026). https://doi.org/10.1038/s41467-026-69706-4
Palabras clave: flavonoides prenilados, ingeniería de enzimas, biocatálisis, <keyword>química verde