Clear Sky Science · de
Feinabstimmung der Besetzung einer aromatischen Käfige in Prenyltransferasen ermöglicht selektive und effiziente Herstellung seltener C‑prenylierter Flavonoide
Warum intelligentere Pflanzenmoleküle wichtig sind
Viele der heutigen Medikamente und Nahrungsergänzungsmittel stammen von pflanzlichen Verbindungen, den sogenannten Flavonoiden. Wenn diese Moleküle mit fettigen „Schwänzen“ aus kurzen Kohlenstoffketten versehen werden, steigt ihre biologische Wirksamkeit oft deutlich an und zeigt Potenzial gegen Krebs, Infektionen, Diabetes und Entzündungen. Diese aufgewerteten Varianten, bekannt als prenylierte Flavonoide, sind jedoch schwer in reiner Form und nützlichen Mengen aus Pflanzen oder durch klassische chemische Synthese zu gewinnen. Die vorliegende Studie beschreibt eine Methode, ein natürliches Enzym so umzuprogrammieren, dass es zuverlässig und effizient seltene, maßgeschneiderte prenylierte Flavonoide herstellt und damit einen Weg für eine umweltfreundlichere Produktion künftiger Arzneimittel und Nutraceuticals öffnet. 
Die Herausforderung der Feinabstimmung pflanzlicher Chemie
Flavonoide besitzen einen empfindlichen, polyphenolischen Kern, der raue chemische Bedingungen schlecht verträgt. Einen Prenyl‑Schwanz an genau einer gewünschten Stelle zu befestigen — ohne den Rest des Moleküls zu verändern — ist für synthetische Chemiker schwierig. Die Natur benutzt bereits Enzyme, sogenannte aromatische Prenyltransferasen, für diese Aufgabe, doch die bekannten Enzyme sind oft langsam, wenig selektiv und schlecht verstanden. Infolgedessen wurden zwar mehr als tausend natürlich vorkommende prenylierte Flavonoide katalogisiert, viele sind aber zu selten, um sie gründlich zu untersuchen, und die interessantesten „C‑prenylierten“ Formen, bei denen die Seitenkette direkt an ein Kohlenstoffatom gebunden ist, sind besonders schwer auf Abruf herzustellen.
Ummoden eines vielseitigen Enzyms
Die Autoren konzentrierten sich auf AtaPT, eine pilzliche Prenyltransferase, die an Dutzenden aromatischer Verbindungen wirken kann, jedoch normalerweise nur moderate Aktivität zeigt und Produktgemische erzeugt. Durch Runden gerichteter Evolution — systematisches Mutieren und Screening tausender Varianten — formten sie die aktive Tasche von AtaPT so um, dass bestimmte Reaktionen am Flavonoid Kaempferol bevorzugt werden. Mit einer Kombination aus semi‑zufälliger Mutagenese und strukturgeleitetem Design identifizierten sie drei leistungsfähige Mutanten. Eine Variante (M8) führt effizient eine ungewöhnliche „reverse“ Prenylierung an Position 8 von Kaempferol durch; eine andere (G326W) leitet eine kurze Prenylgruppe an die 3′‑Position; und eine dritte (M7) setzt eine längere Geranyl‑Kette an der 3′‑Position mit hoher Ausbeute und Selektivität ein. Zusammen verwandeln diese Enzyme ein einzelnes Ausgangsflavonoid in mehrere wertvolle, präzise modifizierte Produkte.
Entdeckung eines molekularen Andockkäfigs
Um zu verstehen, warum diese Mutanten so gut funktionieren, löste das Team Kristallstrukturen der ingenieurmäßigen Enzyme und führte Molekulardynamik‑Simulationen durch. Diese Studien enthüllten ein zentrales Designelement: einen „aromatischen Käfig“, gebildet von gestapelten ringförmigen Aminosäuren, die einen Teil des Flavonoids umgeben. In M8 ersetzt eine kritische Mutation einen starren Rest durch Histidin, was beim Aufbau dieses Käfigs hilft und das Flavonoid in eine Pose verriegelt, in der Kohlenstoff 8 perfekt für den Angriff durch das eintretende Prenylfragment ausgerichtet ist. Wenn ein längeres Donormolekül wie Geranylpyrophosphat verwendet wird, reicht dessen Schwanz in diesen Käfig hinein und füllt ihn, wodurch das Flavonoid in eine alternative Konformation gedrängt wird, die die 3′‑Position freilegt. Einfach dadurch zu verändern, welcher Teil des Enzyms den Käfig besetzt — und welcher Donor vorhanden ist —, schaltet also um, an welcher Stelle die Seitenkette angefügt wird und welche Kettenlänge bevorzugt wird. 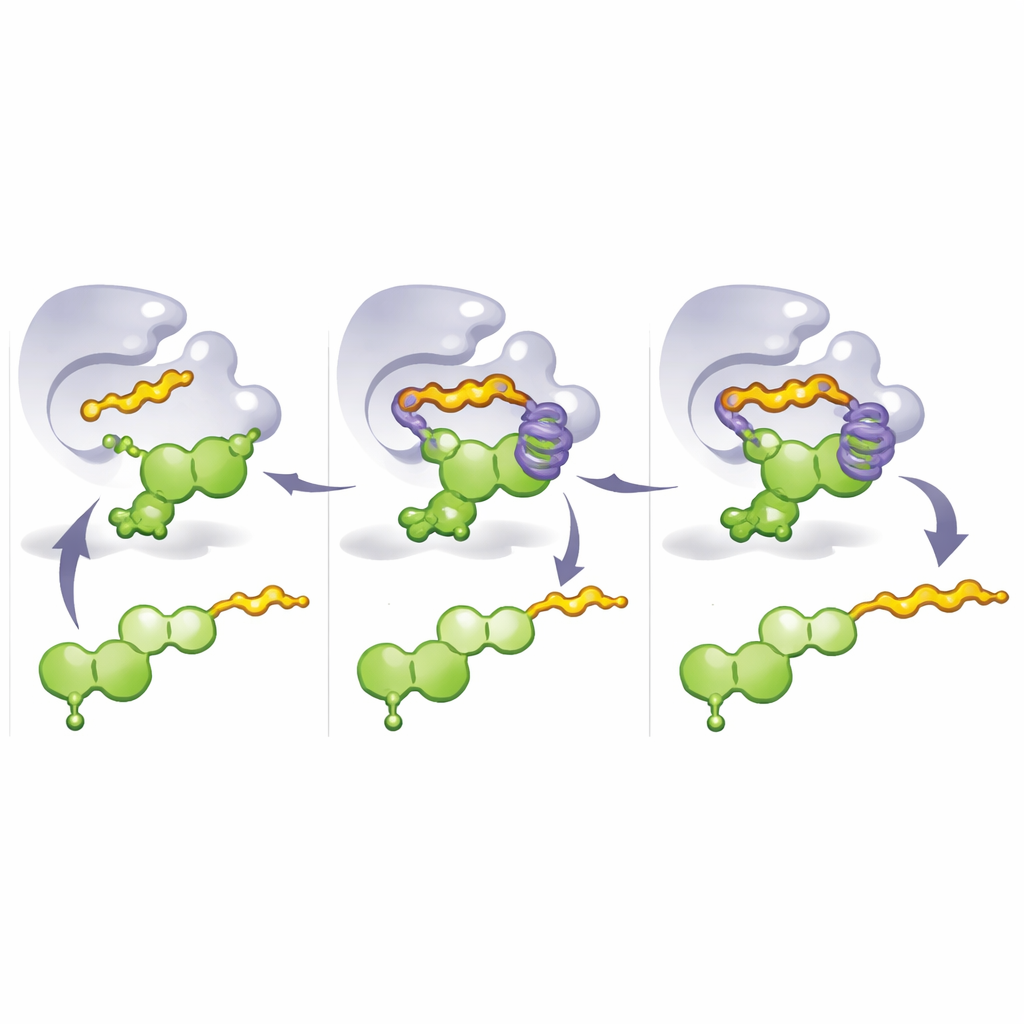
Ausdehnung des Konzepts und Vergrößerung des Katalogs
Mit diesem mechanistischen Verständnis testeten die Forschenden, ob sich das Aromenkäfig‑Konzept auf verwandte Enzyme übertragen lässt. Durch Einführung ähnlicher Mutationen in drei homologe Prenyltransferasen aus anderen Mikroben verbesserten sie deren Aktivität und Präzision deutlich und bestätigten, dass der Käfig ein übertragbares Designmotiv und keine Eigenheit eines einzelnen Proteins ist. Anschließend untersuchten sie ein Panel von 26 verschiedenen Flavonoiden und zeigten, dass die ingenieurisierten Enzyme die meisten von ihnen prenylieren konnten, oft an definierten Positionen. Insgesamt bereitete das Team 31 prenylierte Flavonoide zu, darunter acht Verbindungen, die zuvor noch nie berichtet wurden, und bereicherte so die Palette an Strukturen für biologische Tests und Wirkstoffsuche.
Aufbau einer praktischen, nachhaltigen Produktionslinie
Um diese Reaktionen in einen brauchbaren Produktionsweg zu überführen, kombinierten die Autoren ihre ingenieurisierten Enzyme mit kompakten Stoffwechselwegen, die die reaktiven Prenyl‑Donoren in ingenieurmäßigen E. coli‑Zellen aus einfachen Alkoholen wie Prenol oder Geraniol erzeugen. In optimierten lysatbasierten Systemen erreichten sie Produkttiter von bis zu 400 Milligramm pro Liter im Präparativmaßstab und konnten mehrere Zielmoleküle auf Liter‑Volumina hochskalieren. Da der Prozess in Wasser, bei milden Temperaturen und ohne starke Reagenzien abläuft, bietet er eine umweltfreundliche Alternative zur Gewinnung von Spurenmengen aus Tonnen Pflanzenmaterial.
Was das für zukünftige Medikamente bedeutet
Diese Arbeit zeigt, dass schon die geschickte Umgestaltung einer kleinen Region eines Enzyms — des aromatischen Käfigs — einen trägen, promisken Katalysator in ein präzises und effizientes molekulares Werkzeug verwandeln kann. Durch Nutzung dieses Prinzips schufen die Forschenden eine flexible biokatalytische Plattform zur Herstellung seltener C‑prenylierter Flavonoide in hoher Reinheit und Ausbeute. Für Nichtfachleute lautet die Schlussfolgerung: Wir werden immer besser darin, lebende Systeme dazu zu bringen, komplexe, maßgeschneiderte pflanzenähnliche Moleküle auf Abruf zu bauen, was die Suche nach neuen Therapien beschleunigen und die Umweltbelastung verringern kann.
Zitation: Qiu, R., Huang, H., Chi, J. et al. Tuning aromatic cage occupancy in prenyltransferases enables selective and efficient production of rare c-prenylated flavonoids. Nat Commun 17, 2945 (2026). https://doi.org/10.1038/s41467-026-69706-4
Schlüsselwörter: prenylierte Flavonoide, Enzymtechnik, Biokatalyse, gerichtete Evolution, grüne Chemie