Clear Sky Science · fr
Régler l’occupation de la « cage aromatique » dans les prényltransférases permet une production sélective et efficace de rares flavonoïdes C‑prénylés
Pourquoi des molécules végétales plus intelligentes comptent
Beaucoup des médicaments et compléments santé d’aujourd’hui proviennent de composés végétaux appelés flavonoïdes. Lorsque ces molécules sont équipées de « queues » lipophiles constituées de courtes chaînes carbonées, leur puissance biologique augmente souvent de manière spectaculaire, montrant un potentiel contre le cancer, les infections, le diabète et l’inflammation. Pourtant, ces versions améliorées, appelées flavonoïdes prénylés, sont difficiles à obtenir en forme pure et en quantités utiles, que ce soit à partir des plantes ou par synthèse chimique classique. Cette étude décrit une manière de ré‑ingénier l’un des enzymes naturels pour qu’il produise de façon fiable et efficace des flavonoïdes prénylés rares et sur‑mesure, ouvrant la voie à une production plus écologique de futurs médicaments et nutraceutiques. 
Le défi de l’affinage de la chimie végétale
Les flavonoïdes partagent un noyau polyphénolique fragile qui ne tolère pas les conditions chimiques agressives. Fixer une chaîne de prényle en un seul emplacement désiré — tout en laissant le reste de la molécule intact — est difficile pour les chimistes synthéticiens. La nature utilise déjà des enzymes appelées prényltransférases aromatiques pour accomplir cette tâche, mais les enzymes connues sont souvent lentes, peu sélectives et insuffisamment comprises. Par conséquent, plus d’un millier de flavonoïdes prénylés naturels ont été catalogués, mais beaucoup restent trop rares pour être étudiés en profondeur, et les variétés les plus intéressantes, les C‑prénylés où la queue est directement liée à un atome de carbone, sont particulièrement difficiles à produire à la demande.
Reprogrammer une enzyme polyvalente
Les auteurs se sont concentrés sur AtaPT, une prényltransférase fongique capable d’agir sur des dizaines de composés aromatiques mais qui, en condition normale, présente une activité modeste et génère des mélanges de produits. En utilisant des cycles d’évolution dirigée — muter systématiquement et criblage de milliers de variantes enzymatiques — ils ont remodelé la poche active d’AtaPT pour favoriser des réactions spécifiques sur le flavonoïde kaempférol. Par une combinaison de mutagenèse semi‑aléatoire et de conception guidée par la structure, ils ont identifié trois mutants puissants. Une variante (M8) réalise efficacement une prénylation « inversée » inhabituelle en position 8 du kaempférol ; une autre (G326W) oriente un petit groupe prényle vers la position 3′ ; et une troisième (M7) installe une chaîne plus longue de type géranyl en 3′ avec un rendement et une sélectivité élevés. Ensemble, ces enzymes transforment un flavonoïde de départ unique en plusieurs produits précieux et précisément modifiés.
Découverte d’une cage de positionnement moléculaire
Pour comprendre pourquoi ces mutants fonctionnaient si bien, l’équipe a résolu des structures cristallographiques des enzymes modifiées et a réalisé des simulations de dynamique moléculaire. Ces études ont révélé un élément clé : une « cage aromatique » formée par des acides aminés à anneaux empilés entourant une partie du flavonoïde. Dans M8, une mutation critique remplace un résidu rigide par une histidine, contribuant à construire cette cage et à verrouiller le flavonoïde dans une conformation où le carbone 8 est parfaitement aligné pour l’attaque par le fragment prényle entrant. Lorsqu’un donneur plus long tel que le pyrophosphate de géranyle est utilisé, sa chaîne s’insère et remplit la cage à la place, repoussant le flavonoïde dans une conformation alternative qui expose la position 3′. Ainsi, changer simplement quelle partie de l’enzyme occupe la cage — et quel donneur est présent — modifie l’emplacement d’attachment de la queue et le type de chaîne favorisé. 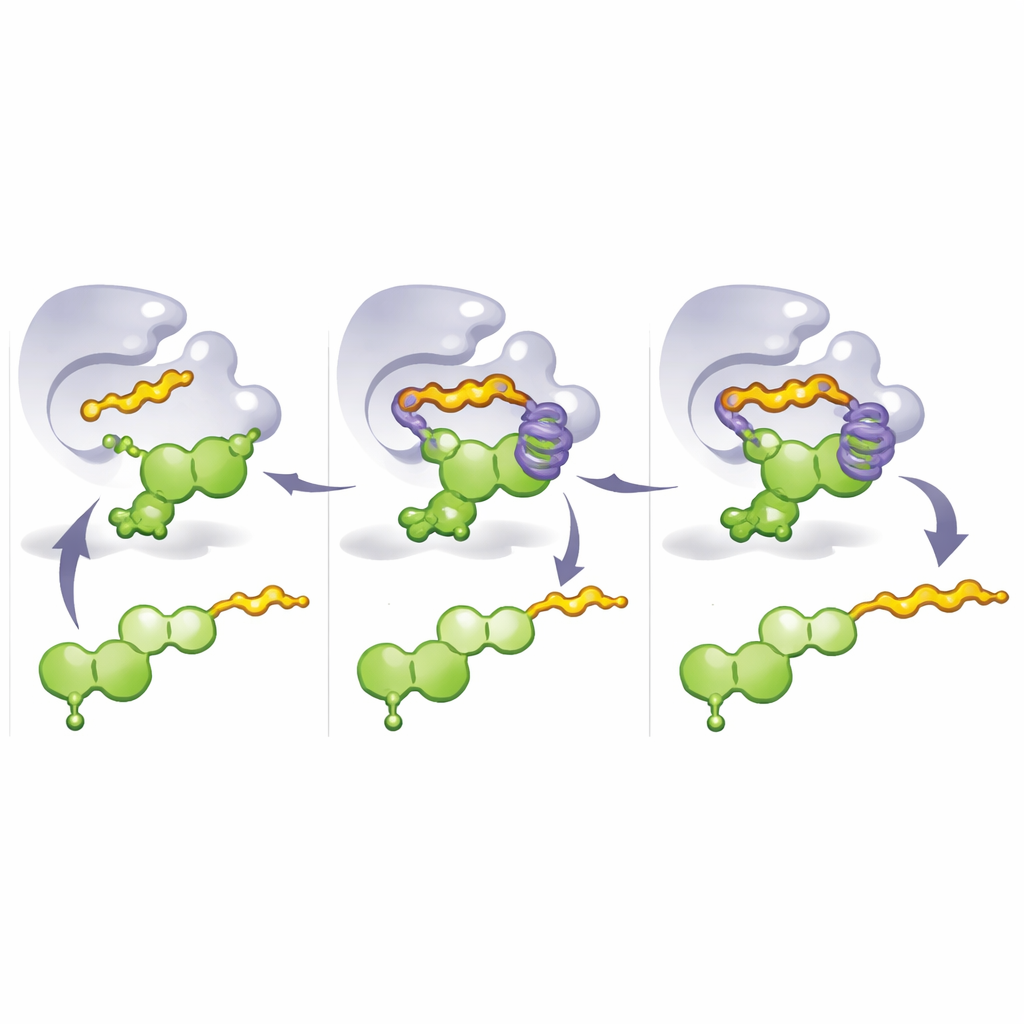
Étendre le plan et élargir le catalogue
Armés de ce modèle mécanistique, les chercheurs ont testé si le concept de la cage aromatique pouvait être exporté vers des enzymes apparentées. En introduisant des mutations similaires dans trois prényltransférases homologues issues d’autres microbes, ils ont considérablement amélioré leur activité et leur précision, confirmant que la cage est un motif de conception transférable plutôt qu’une particularité d’une seule protéine. Ils ont ensuite exploré un panel de 26 flavonoïdes différents, montrant que les enzymes ingénierées pouvaient prényler la plupart d’entre eux, souvent en positions définies. Au total, l’équipe a préparé 31 flavonoïdes prénylés, dont huit composés jamais décrits auparavant, enrichissant ainsi la palette de structures disponibles pour les tests biologiques et la découverte de médicaments.
Construire une ligne de production pratique et durable
Pour transformer ces réactions en une voie de fabrication viable, les auteurs ont couplé leurs enzymes modifiées à des voies métaboliques compactes générant les donneurs prényle réactifs à l’intérieur de cellules d’E. coli ingénierées, à partir d’alcools simples tels que le prenol ou le géraniol. Dans des systèmes optimisés à base de lysats, ils ont atteint des titres de produit allant jusqu’à 400 milligrammes par litre à l’échelle préparative, et ont mis à l’échelle plusieurs molécules cibles jusqu’à des réactions au volume du litre. Parce que le procédé se déroule en milieu aqueux, à températures douces, et évite les réactifs agressifs, il offre une alternative respectueuse de l’environnement à l’extraction de traces de produit à partir de tonnes de matière végétale.
Ce que cela signifie pour les médicaments de demain
Ce travail montre que remodeler intelligemment une petite région d’une enzyme — la cage aromatique — peut transformer un catalyseur lent et promiscuous en un outil moléculaire précis et efficace. En exploitant ce principe, les chercheurs ont créé une plateforme biocatalytique flexible pour fabriquer des flavonoïdes C‑prénylés rares en haute pureté et avec de bons rendements. Pour les non‑spécialistes, la conclusion est que nous devenons beaucoup plus aptes à demander aux systèmes vivants de construire, à la demande, des molécules complexes et sur‑mesure de type végétal, accélérant potentiellement la découverte de nouveaux traitements tout en réduisant l’impact environnemental.
Citation: Qiu, R., Huang, H., Chi, J. et al. Tuning aromatic cage occupancy in prenyltransferases enables selective and efficient production of rare c-prenylated flavonoids. Nat Commun 17, 2945 (2026). https://doi.org/10.1038/s41467-026-69706-4
Mots-clés: flavonoïdes prénylés, ingénierie enzymatique, biocatalyse, évolution dirigée, chimie verte