Clear Sky Science · it
Regolare l’occupazione della «gabbia» aromatica nelle preniltransferasi consente la produzione selettiva ed efficiente di rari flavonoidi c‑prenilati
Perché le molecole vegetali più intelligenti contano
Molti dei medicinali e degli integratori attuali provengono da composti vegetali chiamati flavonoidi. Quando queste molecole vengono decorate con «code» lipofile costituite da brevi catene di carbonio, la loro attività biologica spesso aumenta notevolmente, mostrando potenziale contro tumori, infezioni, diabete e infiammazione. Tuttavia, queste versioni potenziate, note come flavonoidi prenilati, sono difficili da ottenere in forma pura e in quantità utili sia dalle piante sia dalla sintesi chimica tradizionale. Questo studio descrive un modo per reingegnerizzare un enzima naturale in modo che costruisca in modo affidabile ed efficiente rari flavonoidi prenilati su misura, aprendo la strada a una produzione più sostenibile di futuri farmaci e nutraceutici. 
La sfida di mettere a punto la chimica vegetale
I flavonoidi condividono un nucleo polifenolico fragile che non sopporta condizioni chimiche aggressive. Attaccare una coda prenilica in un punto preciso—lasciando intatto il resto della molecola—è difficile per i chimici sintetici. La natura usa già enzimi chiamati preniltransferasi aromatiche per svolgere questo compito, ma gli enzimi noti sono spesso lenti, poco selettivi e non completamente compresi. Di conseguenza, sono stati catalogati oltre mille flavonoidi prenilati naturali, ma molti rimangono troppo rari per essere studiati a fondo, e le varietà più interessanti «C‑prenilate», in cui la coda è legata direttamente a un atomo di carbonio, sono particolarmente difficili da produrre su richiesta.
Riprogrammare un enzima versatile
Gli autori si sono concentrati su AtaPT, una preniltransferasi fungina in grado di agire su dozzine di composti aromatici ma che normalmente mostra attività modesta e produce miscele di prodotti. Attraverso cicli di evoluzione diretta—mutando sistematicamente e schermando migliaia di varianti enzimatiche—hanno rimodellato la tasca attiva di AtaPT per favorire reazioni specifiche sul flavonoide kaempferolo. Con una combinazione di mutagenesi semi‑casuale e progettazione guidata dalla struttura, hanno identificato tre mutanti potenti. Una variante (M8) esegue efficacemente una insolita prenilazione «inversa» in posizione 8 del kaempferolo; un’altra (G326W) dirige un breve gruppo prenilico alla posizione 3′; e una terza (M7) installa una catena geranilica più lunga in posizione 3′ con elevata resa e selettività. Insieme, questi enzimi trasformano un singolo flavonoide di partenza in diversi prodotti preziosi e precisamente modificati.
Scoprire una gabbia di ancoraggio molecolare
Per capire perché questi mutanti funzionassero così bene, il gruppo ha risolto strutture cristalline degli enzimi ingegnerizzati e ha eseguito simulazioni di dinamica molecolare. Questi studi hanno rivelato una caratteristica progettuale chiave: una «gabbia aromatica» formata da amminoacidi ad anello impilati che circondano parte del flavonoide. In M8, una mutazione critica sostituisce un residuo rigido con istidina, contribuendo a costruire questa gabbia e a bloccare il flavonoide in una posa in cui il carbonio 8 è perfettamente allineato per l’attacco dal frammento prenilico in arrivo. Quando viene usato un donatore più lungo come il geranil pirofosfato, la sua «coda» raggiunge e riempie la gabbia invece, spingendo il flavonoide in una conformazione alternativa che espone la posizione 3′. Così, modificare quale parte dell’enzima occupa la gabbia—e quale donatore è presente—cambia il punto di attacco della coda e il tipo di catena favorito. 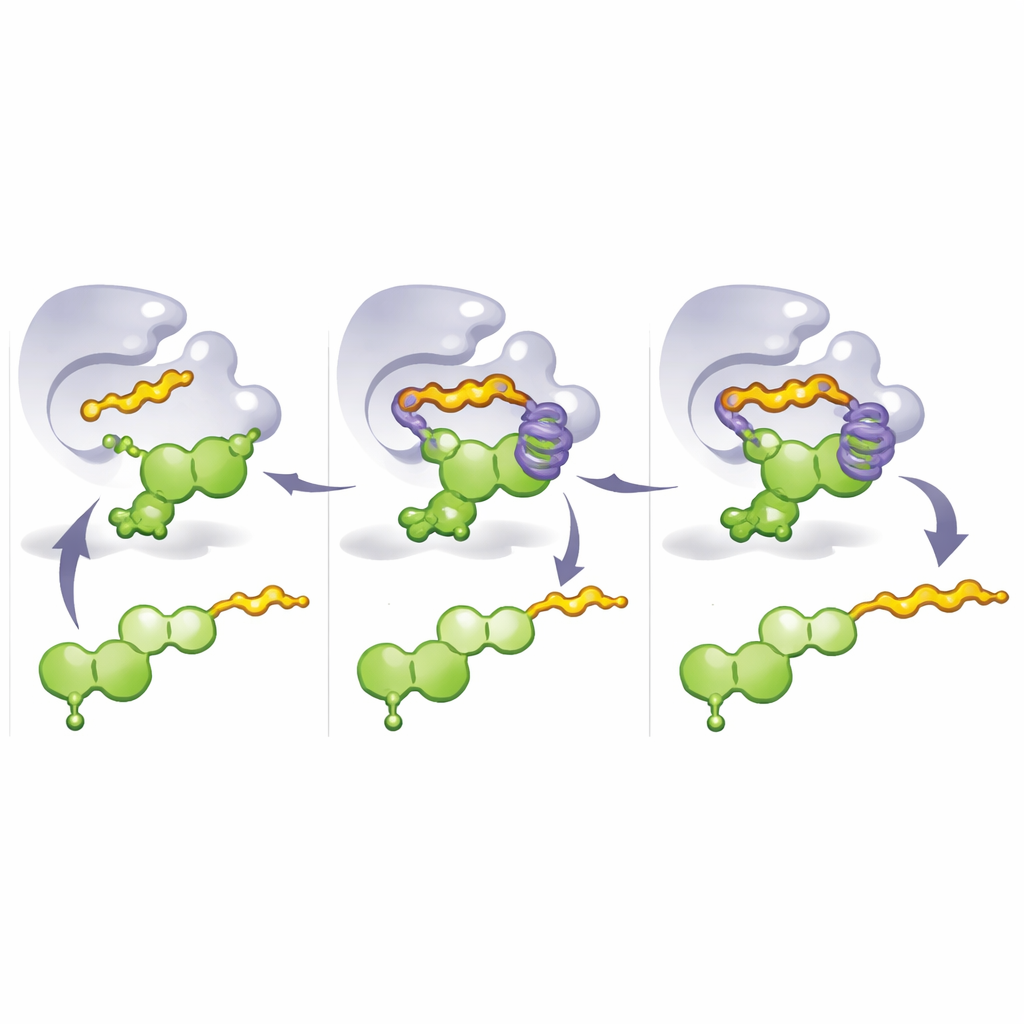
Estendere il progetto e ampliare il catalogo
Muniti di questa visione meccanicistica, i ricercatori hanno testato se il concetto della gabbia aromatica potesse essere trasferito ad enzimi correlati. Introducendo mutazioni analoghe in tre preniltransferasi omologhe provenienti da altri microrganismi, hanno migliorato drasticamente la loro attività e precisione, confermando che la gabbia è un motivo progettuale trasferibile e non una peculiarità di una singola proteina. Hanno quindi esplorato un pannello di 26 flavonoidi diversi, dimostrando che gli enzimi ingegnerizzati potevano prenilare la maggior parte di essi, spesso in posizioni definite. In totale, il team ha preparato 31 flavonoidi prenilati, inclusi otto composti mai descritti prima, arricchendo così la gamma di strutture disponibili per test biologici e scoperta di farmaci.
Costruire una linea di produzione pratica e sostenibile
Per trasformare queste reazioni in una via di produzione praticabile, gli autori hanno accoppiato i loro enzimi ingegnerizzati a percorsi metabolici compatti che generano i donatori prenilici reattivi all’interno di cellule di E. coli ingegnerizzate a partire da alcoli semplici come prenolo o geraniolo. In sistemi ottimizzati basati su lisati, hanno raggiunto concentrazioni di prodotto fino a 400 milligrammi per litro su scale preparative, e hanno scalato con successo diversi target a reazioni di volume litro. Poiché il processo avviene in acqua, a temperature miti, ed evita reagenti aggressivi, offre un’alternativa ecologica all’estrazione di tracce di prodotto da tonnellate di materiale vegetale.
Cosa significa per i farmaci futuri
Questo lavoro dimostra che rimodellare con intelligenza una piccola regione di un enzima—la gabbia aromatica—può trasformare un catalizzatore lento e promiscuo in uno strumento molecolare preciso ed efficiente. Sfruttando questo principio, i ricercatori hanno creato una piattaforma biocatalitica flessibile per produrre rari flavonoidi C‑prenilati ad alta purezza e resa. Per i non specialisti, la conclusione è che stiamo diventando molto più bravi a far sì che i sistemi viventi costruiscano molecole complesse, simili a quelle vegetali, su richiesta, accelerando potenzialmente la ricerca di nuovi trattamenti e riducendo l’impatto ambientale.
Citazione: Qiu, R., Huang, H., Chi, J. et al. Tuning aromatic cage occupancy in prenyltransferases enables selective and efficient production of rare c-prenylated flavonoids. Nat Commun 17, 2945 (2026). https://doi.org/10.1038/s41467-026-69706-4
Parole chiave: flavonoidi prenilati, ingegneria enzimatica, biocatalisi, evoluzione diretta, chimica verde