Clear Sky Science · pl
Dostosowywanie zajętości aromatycznej klatki w prenylotransferazach umożliwia selektywną i wydajną produkcję rzadkich c-prenylowanych flawonoidów
Dlaczego inteligentniejsze cząsteczki roślinne mają znaczenie
Wiele współczesnych leków i suplementów zdrowotnych pochodzi z roślinnych związków chemicznych zwanych flawonoidami. Gdy te cząsteczki zostają „ozdobione” tłustymi „ogonami” utworzonymi z małych łańcuchów węglowych, ich aktywność biologiczna często rośnie znacząco, wykazując potencjał przeciw nowotworom, infekcjom, cukrzycy i zapaleniom. Jednak te wzmocnione wersje, znane jako prenylowane flawonoidy, są trudne do uzyskania w czystej postaci i w użytecznych ilościach zarówno z roślin, jak i poprzez tradycyjną syntezę chemiczną. Niniejsze badanie opisuje sposób przeprojektowania naturalnego enzymu, tak aby mógł niezawodnie i wydajnie wytwarzać rzadkie, szyte na miarę prenylowane flawonoidy, otwierając drogę do bardziej ekologicznej produkcji przyszłych leków i nutraceutyków. 
Wyzwanie precyzyjnego strojenia chemii roślinnej
Flawonoidy mają delikatne, polifenolowe jądro, które źle znosi surowe warunki chemiczne. Przyłączenie ogona prenylowego w jednym, pożądanym miejscu — pozostawiając resztę cząsteczki nietkniętą — jest trudne dla chemików syntetycznych. Natura już wykorzystuje enzymy zwane aromatycznymi prenylotransferazami do tego zadania, lecz znane enzymy często działają wolno, mają słabą selektywność i nie są dobrze zrozumiane. W rezultacie skatalogowano ponad tysiąc naturalnie występujących prenylowanych flawonoidów, lecz wiele z nich pozostaje zbyt rzadkich, by dokładnie je badać, a najbardziej interesujące odmiany „C‑prenylowane”, gdzie ogon jest bezpośrednio połączony z atomem węgla, są szczególnie trudne do otrzymania na żądanie.
Przeprogramowanie wszechstronnego enzymu
Autorzy skupili się na AtaPT, grzybowej prenylotransferazie, która może działać na dziesiątki związków aromatycznych, ale zazwyczaj wykazuje umiarkowaną aktywność i produkuje mieszaniny produktów. Używając rund ewolucji kierowanej — systematycznie mutując i przesiewając tysiące wariantów enzymu — przekształcili kieszeń aktywną AtaPT tak, aby faworyzowała specyficzne reakcje na flawonoidzie kaempferolu. Dzięki kombinacji półlosowej mutagenezy i projektowania opartego na strukturze zidentyfikowali trzy silne mutacje. Jeden wariant (M8) efektywnie przeprowadza nietypową „odwrotną” prenylację w pozycji 8 kaempferolu; inny (G326W) kieruje krótki fragment prenylowy do pozycji 3′; a trzeci (M7) umieszcza dłuższy łańcuch geranylowy w pozycji 3′ z wysoką wydajnością i selektywnością. Razem te enzymy przekształcają pojedynczy wyjściowy flawonoid w kilka wartościowych, precyzyjnie zmodyfikowanych produktów.
Odkrycie molekularnej klatki dokującej
Aby zrozumieć, dlaczego te mutanty działały tak dobrze, zespół rozwiązał struktury krystaliczne zmodyfikowanych enzymów i przeprowadził symulacje dynamiki molekularnej. Badania te ujawniły kluczową cechę projektową: „aromatyczną klatkę” utworzoną przez ułożone jedna nad drugą pierścieniowe aminokwasy okalające część flawonoidu. W M8 krytyczna mutacja zastępuje sztywny resztę histydyną, pomagając zbudować tę klatkę i zablokować flawonoid w pozycji, w której węgiel 8 jest idealnie ustawiony do ataku przez nadchodzący fragment prenylowy. Gdy użyty zostaje dłuższy donor, taki jak pirofosforan geranylu, jego ogon wpada do tej klatki i ją wypełnia, wypychając flawonoid do alternatywnej konformacji, która odsłania pozycję 3′. Zatem proste zmiany tego, która część enzymu zajmuje klatkę — oraz jaki donor jest obecny — przełączają miejsce przyłączenia ogona i preferowany rodzaj łańcucha. 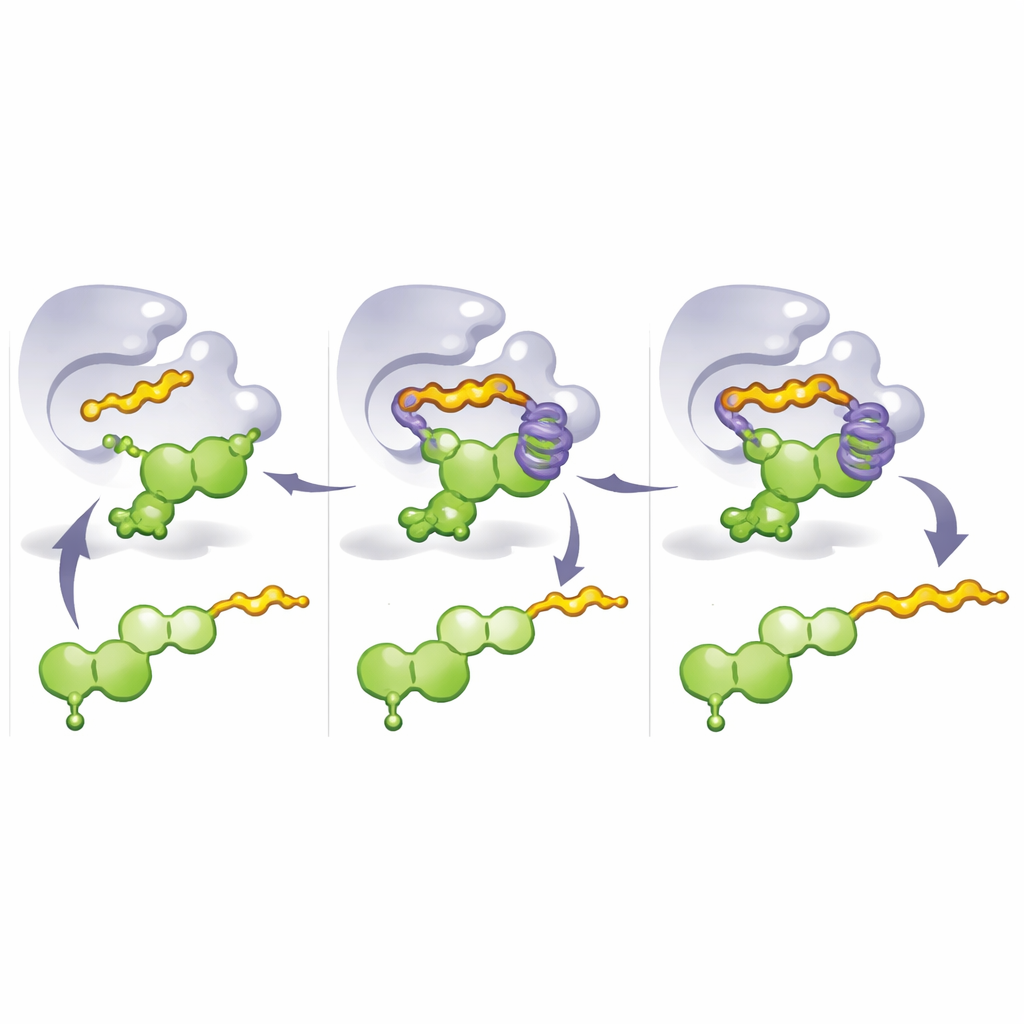
Rozszerzenie planu i poszerzenie katalogu
Uzbrojeni w to mechanistyczne wyjaśnienie, badacze sprawdzili, czy koncepcję aromatycznej klatki można przenieść do spokrewnionych enzymów. Wprowadzając podobne mutacje do trzech homologicznych prenylotransferaz z innych mikroorganizmów, znacząco poprawili ich aktywność i precyzję, potwierdzając, że klatka to przenośny motyw projektowy, a nie wyjątkowa cecha pojedynczego białka. Następnie przebadali panel 26 różnych flawonoidów, pokazując, że zmodyfikowane enzymy potrafią prenylować większość z nich, często w określonych pozycjach. W sumie zespół przygotował 31 prenylowanych flawonoidów, w tym osiem związków nigdy wcześniej nieopisanych, wzbogacając paletę struktur dostępną do testów biologicznych i poszukiwania leków.
Budowanie praktycznej, zrównoważonej linii produkcyjnej
Aby przekształcić te reakcje w wykonalną ścieżkę produkcyjną, autorzy połączyli swoje zmodyfikowane enzymy z zwartymi szlakami metabolicznymi, które generują reaktywne donory prenylowe wewnątrz zmodyfikowanych komórek E. coli z prostych alkoholów, takich jak prenol czy geraniol. W zoptymalizowanych systemach opartych na lizatach osiągnęli miana produktu do 400 miligramów na litr w skali preparatywnej i z powodzeniem skalowali kilka docelowych cząsteczek do reakcji o objętości litra. Ponieważ proces przebiega w wodzie, w łagodnych temperaturach i unika ostrych reagentów, stanowi przyjazną dla środowiska alternatywę dla ekstrakcji śladowych ilości produktu z ton materiału roślinnego.
Co to oznacza dla przyszłych leków
Ta praca pokazuje, że sprytne przekształcenie niewielkiego obszaru enzymu — aromatycznej klatki — może zmienić powolny, nietechniczny katalizator w precyzyjne i wydajne narzędzie molekularne. Wykorzystując tę zasadę, badacze stworzyli elastyczną platformę biokatalityczną do wytwarzania rzadkich C‑prenylowanych flawonoidów o wysokiej czystości i wydajności. Dla osób niebędących specjalistami kluczowy wniosek jest taki, że coraz lepiej potrafimy poprosić systemy żywe o wytwarzanie złożonych, szytych na miarę cząsteczek roślinnych na żądanie, co może przyspieszyć poszukiwanie nowych terapii przy jednoczesnym zmniejszeniu wpływu na środowisko.
Cytowanie: Qiu, R., Huang, H., Chi, J. et al. Tuning aromatic cage occupancy in prenyltransferases enables selective and efficient production of rare c-prenylated flavonoids. Nat Commun 17, 2945 (2026). https://doi.org/10.1038/s41467-026-69706-4
Słowa kluczowe: prenylowane flawonoidy, inżynieria enzymów, biokataliza, ewolucja kierowana, zielona chemia