Clear Sky Science · zh
FATE-MAP 通过整合深度学习与机理建模预测致畸性与人类胚胎原肠胚形成失败模式
为什么早期胚胎错误很重要
许多妊娠在最早几周就终止,原因常常对父母和医生而言都不可见。一个关键关卡是称为原肠胚形成的阶段,此时一个简单的细胞球重组为将形成身体各个器官的基本层次。如果这一步出错,可能导致流产或出生缺陷。然而,科学家缺乏针对人类的工具来观察药物和化学物质如何扰乱这一脆弱过程。本研究提出了 FATE-MAP,一种将干细胞模型、先进成像与人工智能相结合的新平台,用以预测哪些化合物可能危害早期人类发育,并揭示这些失败是如何产生的。
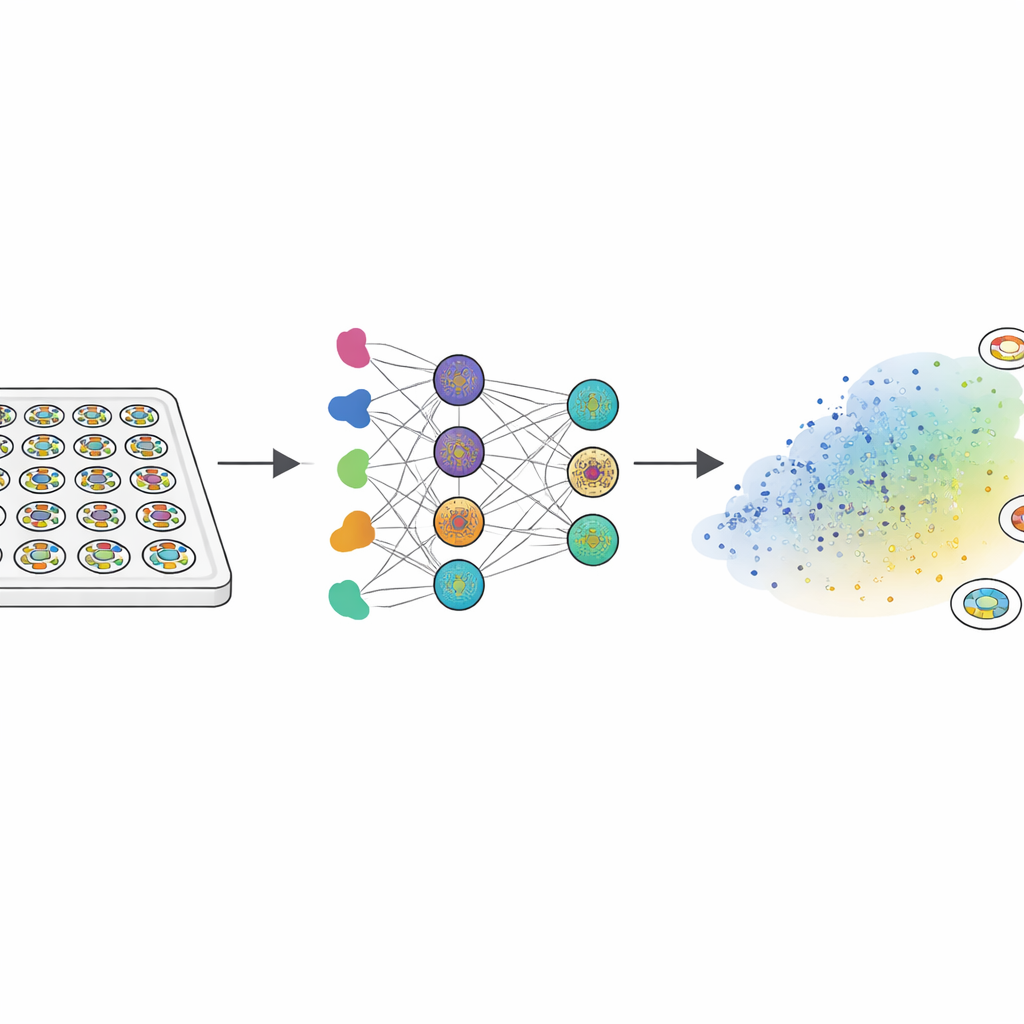
在实验室构建早期胚胎的替代模型
由于真实的人类胚胎无法深入研究,研究人员转而使用“原肠体”——由人胚胎干细胞培养出的微小平盘。当暴露于一种称为 BMP4 的信号蛋白时,这些圆盘会自组织形成三个同心区域,对应早期胚胎组织:内部区域保持类干细胞状态,中间带发育为中胚层(肌肉、骨骼和血液的前体),外环与早期胚外组织相关。团队用一个包含 210 种针对关键生长与信号通路药物的库处理了约 2000 个此类菌落。通过荧光标记与定制图像分析,他们将每个菌落的模式转化为一个由 150 个数字组成的指纹,捕捉从边缘到中心三种组织类型的排列情况。
绘制正常模式与失败模式的映射
为了解读这一庞大数据集,科学家使用了一种将相似模式在二维“形态空间”中聚类在一起的技术。大多数菌落落在一个广泛区域内,三种组织按径向顺序正确出现,主要差异在于每个环的宽度。但出现了若干不同的“失败模式”:有些模式缺失中央的类干细胞区,有些丧失了中胚层带,还有一些完全破坏了径向对称性。由于此类缺陷很可能阻碍正确的体轴与体节形成,团队将这些簇视为发育失败模式而非无害变异。这个映射成为对比实验数据与计算模型的参考。
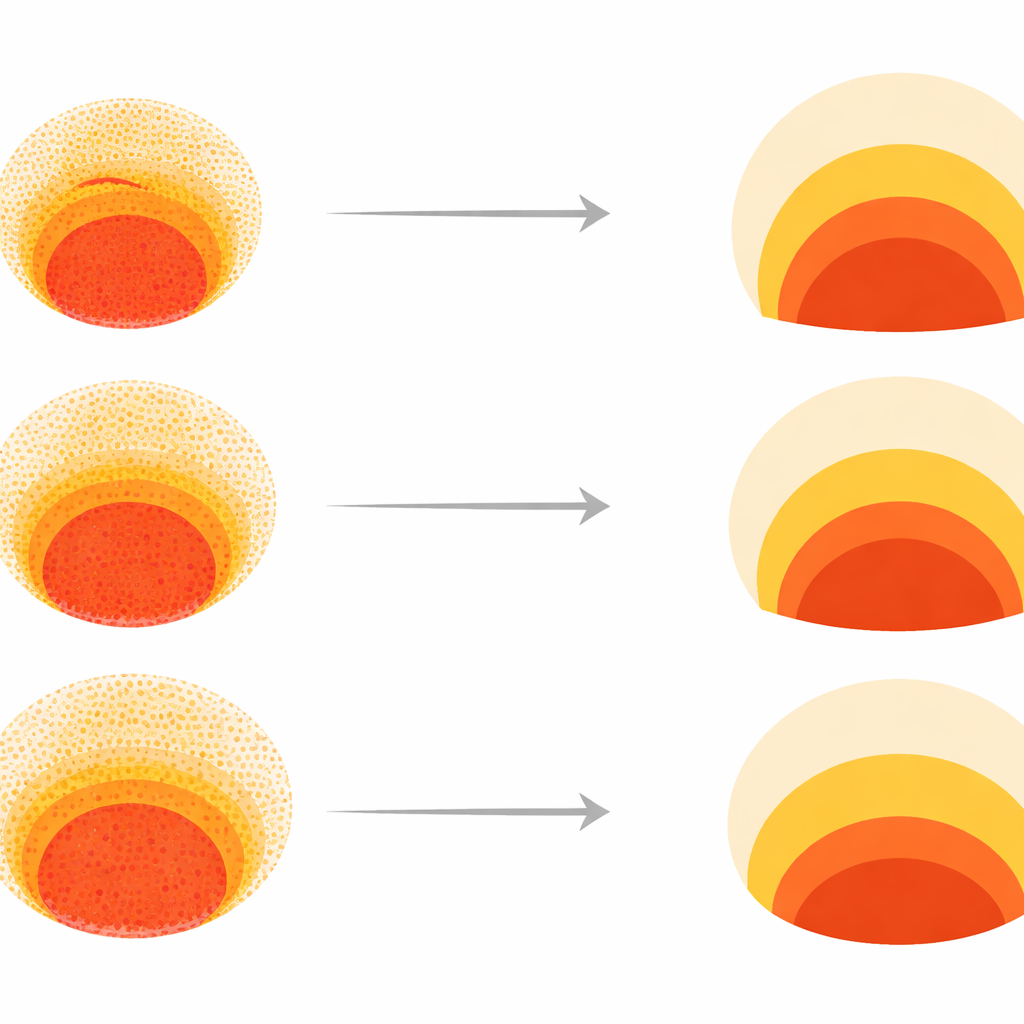
教计算机预测高风险化合物
下一步是测试计算机是否仅凭化学式就能预测新化合物在形态空间中的落点。作者使用了一种变换器模型(transformer)——一种最初用于语言处理的深度学习方法——将每个分子的 SMILES 字符串转换为高维数值描述。随后,一个神经网络学习将这些描述映射到 150 维的菌落指纹,第二个网络再把这些指纹翻译为形态空间上的位置。对于数十种已知妊娠结果的药物,FATE-MAP 的纯计算预测在将化合物分类为有风险或安全方面,与领先的干细胞与计算致畸性检测方法相当甚至更优。值得注意的是,多种著名致畸物都汇聚到同一失败簇,其特征是中胚层的丧失。
揭示失败发生的机制,而不仅仅是指出发生
单靠“黑箱”人工智能无法解释菌落为何失败。为增加机理解释,团队构建了一个数学模型,描述三种主要信号分子——BMP、Wnt 与 Nodal——如何在菌落中扩散并随时间推动细胞走向不同命运。通过调整参数,例如初始细胞密度以及中央类干细胞对分化的抵抗力(以他们称为 SOX2 稳定性的量来表征),他们能够模拟模式并将其投射进相同的形态空间。这表明大多数正常模式变异可由两条几乎独立的轴线解释:细胞拥挤程度与放弃类干细胞身份的易难度。较低的细胞密度允许 Wnt 与 Nodal 信号更向内扩散,从而拓宽中胚层带;而较高的 SOX2 稳定性则在分化信号作用下使中央区域保持更原始的状态。
从预警走向更安全的未来药物
最后,研究人员用 FATE-MAP 标记了两种临床阶段药物——在此之前无人体妊娠数据——作为潜在致畸物。两者均被预测并随后实验证实会产生与经典类维甲酸致畸物相同的中胚层丧失失败模式,并在斑马鱼胚胎中引起特征性缺陷。更广泛地看,这项工作展示了将现实的干细胞模型、机器学习与机理方程结合,如何把早期人类发育转化为可绘制的景观。从长远来看,像 FATE-MAP 这样的 平台可以帮助药物开发者在药物进入患者之前筛查大量化合物的细微发育风险,同时阐明引导胚胎从一张简单细胞片发展为完整身体的基本规则。
引用: Rufo, J., Qiu, C., Han, D. et al. FATE-MAP predicts teratogenicity and human gastrulation failure modes by integrating deep learning and mechanistic modeling. Nat Commun 17, 3327 (2026). https://doi.org/10.1038/s41467-026-69596-6
关键词: 致畸性, 原肠胚形成, 干细胞模型, 深度学习, 发育毒性