Clear Sky Science · nl
FATE-MAP voorspelt teratogeniciteit en menselijke gastrulatie‑faalmodi door diepe leertechnieken en mechanistische modellering te integreren
Waarom fouten in het vroege embryo ertoe doen
Veel zwangerschappen halen de eerste weken niet, vaak om redenen die voor ouders en artsen onzichtbaar blijven. Een cruciale hindernis is een stadium dat gastrulatie heet, waarin een eenvoudige celbol zich herstructureert tot de basale lagen waaruit elk orgaan zal ontstaan. Als dit proces misgaat, kan dat leiden tot zwangerschapsverlies of aangeboren afwijkingen. Toch hadden wetenschappers weinig mensspecifieke instrumenten om te zien hoe geneesmiddelen en chemicaliën dit kwetsbare proces kunnen verstoren. Deze studie introduceert FATE‑MAP, een nieuw platform dat stamcelmodellen, geavanceerde beeldvorming en kunstmatige intelligentie combineert om te voorspellen welke verbindingen de vroege menselijke ontwikkeling kunnen schaden en om te onthullen hoe die mislukkingen ontstaan.
Een laboratorium‑vervanger voor het vroege embryo bouwen
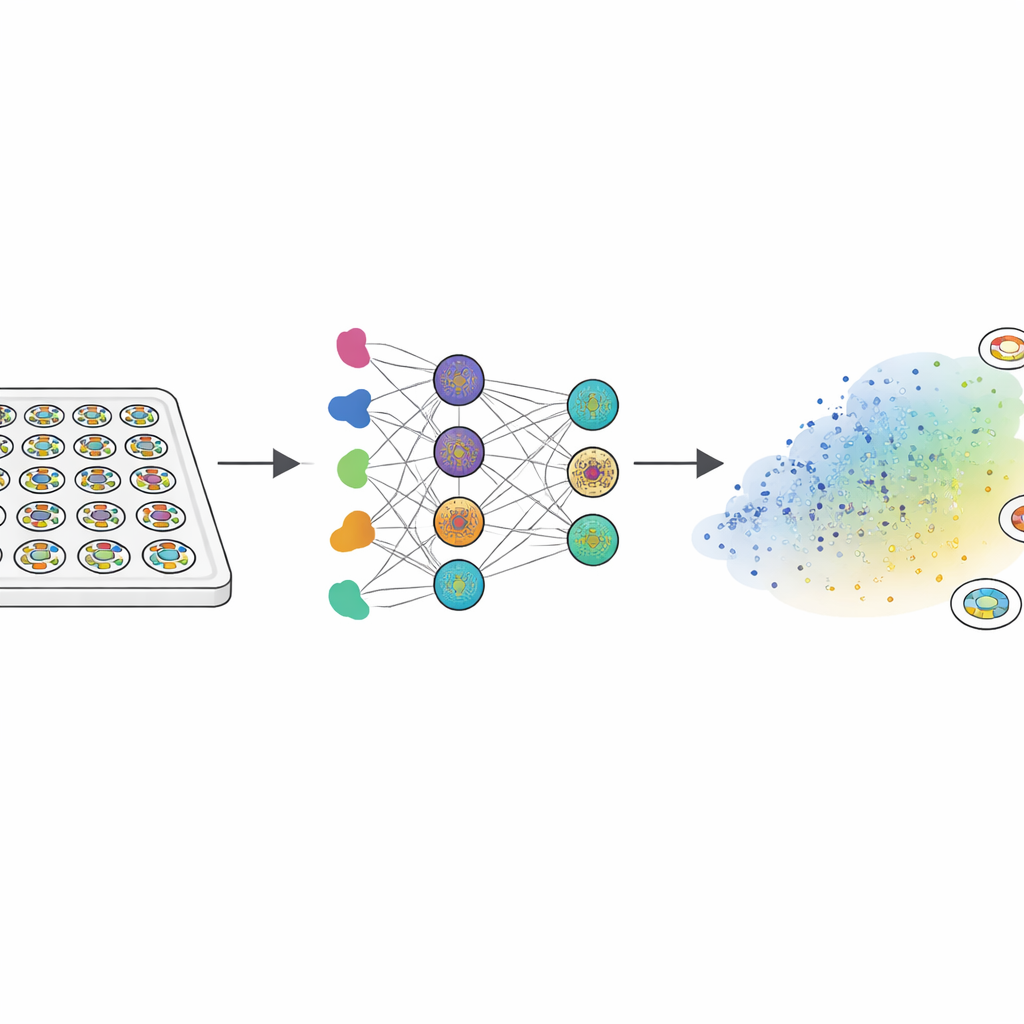
Aangezien echte menselijke embryo’s niet grondig bestudeerd kunnen worden, gebruikten de onderzoekers "gastruloïden" — kleine, platte schijfjes gekweekt uit menselijke embryonale stamcellen. Wanneer deze schijfjes worden blootgesteld aan een signaalproteïne genaamd BMP4, organiseren ze zichzelf in drie concentrische zones die vroege embryonale weefsels weerspiegelen: een binnenste regio die stamcelachtig blijft, een middelste band die mesoderm vormt (voorlopers van spier, bot en bloed), en een buitenste ring gerelateerd aan vroeg extra‑embryonaal weefsel. Het team behandelde ongeveer 2000 van deze kolonies met een bibliotheek van 210 geneesmiddelen die belangrijke groeipaden en signaalroutes targeten. Met fluorescentiemarkers en aangepaste beeldanalyse zetten ze het patroon van elke kolonie om in een vingerafdruk van 150 getallen die vastlegde hoe de drie weefseltypes van rand naar centrum waren gerangschikt.
Normale patronen en faalmodi in kaart brengen
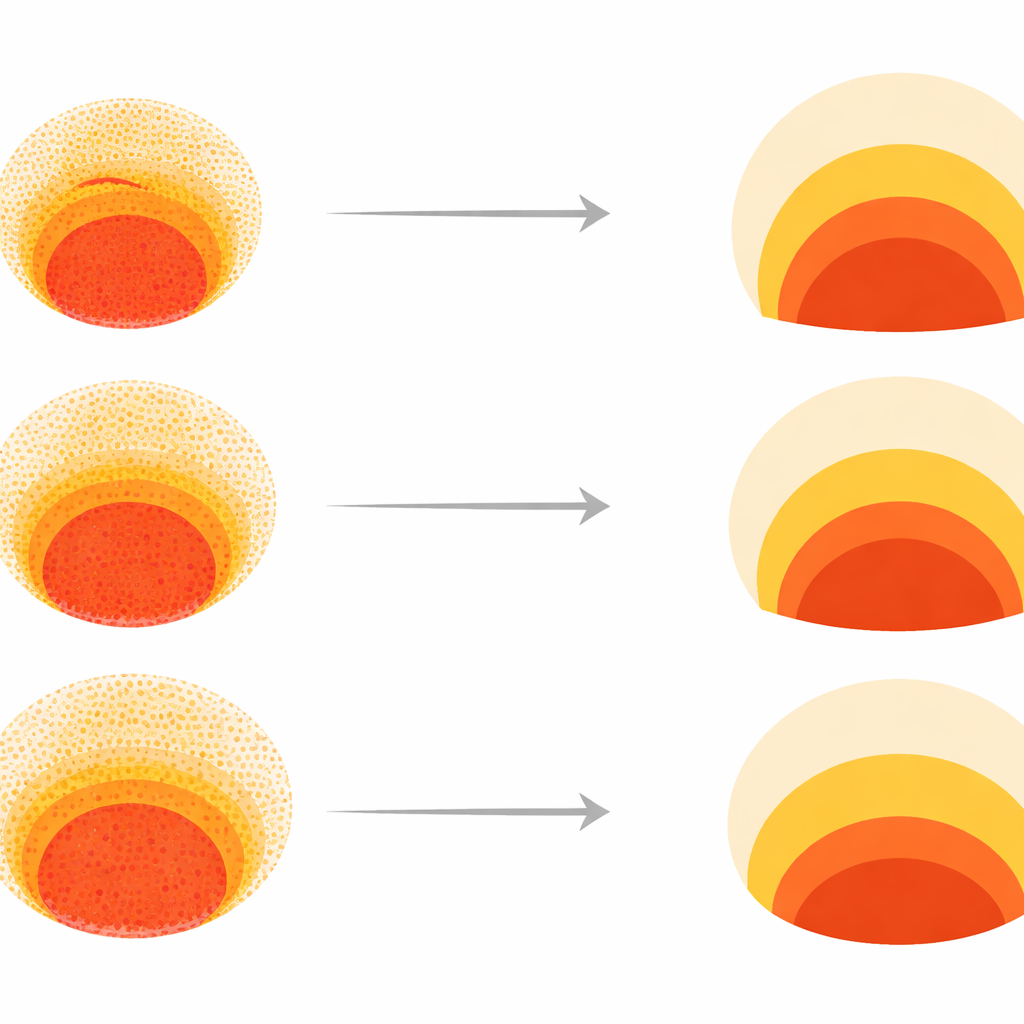
Om deze enorme dataset te begrijpen gebruikten de wetenschappers een techniek die vergelijkbare patronen dicht bij elkaar groepeert in een tweedimensionale "morforuimte." De meeste kolonies vielen in een brede regio waar alle drie de weefseltypes in de juiste radiale volgorde verschenen, zich voornamelijk onderscheidend in hoe breed elke ring was. Maar er doken meerdere duidelijke "faalmodi" op: sommige patronen misten de centrale stamcelachtige regio, andere verloren de mesodermband, en sommige braken de radiale symmetrie volledig. Omdat zulke defecten waarschijnlijk de correcte vorming van het lichaamsplan zouden verhinderen, beschouwde het team deze clusters als ontwikkelingsfouten in plaats van onschuldige variatie. Deze kaart werd de referentie waarmee zowel experimentele data als computermodellen vergeleken konden worden.
Computers leren risicovolle verbindingen te voorspellen
De volgende stap was nagaan of een computer kon voorspellen waar een nieuwe verbinding in deze morforuimte terecht zou komen enkel op basis van zijn chemische formule. De auteurs gebruikten een transformer‑model — een deep‑learningbenadering oorspronkelijk ontwikkeld voor taal — om de SMILES‑string van elk molecuul om te zetten in een hoogdimensionale numerieke representatie. Een neuraal netwerk leerde deze representaties vervolgens te koppelen aan de 150‑cijferige kolonievingerafdrukken, en een tweede netwerk vertaalde die vingerafdrukken naar posities op de morforuimtekaart. Voor tientallen geneesmiddelen met bekende zwangerschapsuitkomsten kwamen FATE‑MAPs zuiver in silico‑voorspellingen overeen met of presteerden beter dan toonaangevende stamcel‑ en computationele teratogeniciteitstests bij het classificeren van verbindingen als risicovol of veilig. Opmerkelijk was dat meerdere bekende teratogenen allemaal convergeerden naar dezelfde faalcluster, gekenmerkt door verlies van mesoderm.
Uitleggen hoe mislukkingen ontstaan, niet alleen dat ze optreden
Zwarte‑doos AI kan op zichzelf niet verklaren waarom een kolonie faalt. Om mechanisme toe te voegen bouwde het team een wiskundig model van hoe drie belangrijke signaalmoleculen — BMP, Wnt en Nodal — zich over de kolonie verspreiden en cellen na verloop van tijd naar verschillende bestemmingen sturen. Door parameters aan te passen zoals de begindichtheid van cellen en hoe resistent de centrale stamcelachtige cellen zijn tegen differentiatie (vastgelegd in een grootheid die zij SOX2‑stabiliteit noemen), konden ze patronen simuleren en die projecteren in dezelfde morforuimte. Dit toonde dat het grootste deel van de normale variatie in patronen verklaard kon worden door twee bijna onafhankelijke assen: hoe dicht de cellen opeengepakt zijn en hoe gemakkelijk ze hun stamcelachtige identiteit opgeven. Lagere celdichtheid liet Wnt‑ en Nodal‑signalen verder naar binnen verspreiden, waarmee de mesodermband verbreedde, terwijl hogere SOX2‑stabiliteit de centrale regio meer primitief hield ondanks differentiatiesignalen.
Van waarschuwingen naar veiligere medicijnen in de toekomst
Tenslotte gebruikte het team FATE‑MAP om twee geneesmiddelen in klinische fase die geen eerdere menselijke zwangerschapsgegevens hadden te markeren als potentiële teratogenen. Beide werden voorspeld — en vervolgens experimenteel bevestigd — hetzelfde mesoderm‑verlies faalpatroon te produceren dat gezien wordt bij klassieke retinoïde teratogenen, en ze veroorzaakten ook karakteristieke defecten in zebravis‑embryo’s. Breder bekeken toont het werk hoe het combineren van realistische stamcelmodellen, machine learning en mechanistische vergelijkingen vroege menselijke ontwikkeling kan omzetten in een in kaart te brengen landschap. Op de lange termijn zouden platforms zoals FATE‑MAP farmaceutische ontwikkelaars kunnen helpen enorme aantallen verbindingen te screenen op subtiele ontwikkelingsrisico’s voordat ze patiënten bereiken, terwijl ze tegelijkertijd de fundamentele regels verhelderen die een embryo van een eenvoudige celplaat naar een volledig gevormd lichaam sturen.
Bronvermelding: Rufo, J., Qiu, C., Han, D. et al. FATE-MAP predicts teratogenicity and human gastrulation failure modes by integrating deep learning and mechanistic modeling. Nat Commun 17, 3327 (2026). https://doi.org/10.1038/s41467-026-69596-6
Trefwoorden: teratogeniciteit, gastrulatie, stamcelmodellen, deep learning, ontwikkelings‑toxicity