Clear Sky Science · es
FATE-MAP predice teratogenicidad y modos de fallo de la gastrulación humana integrando aprendizaje profundo y modelado mecanicista
Por qué importan los errores en el embrión temprano
Muchas gestaciones no superan las primeras semanas, a menudo por razones que permanecen invisibles tanto para los progenitores como para los médicos. Un obstáculo crítico es una etapa llamada gastrulación, cuando una simple bola de células se reorganiza en las capas básicas que formarán todos los órganos del cuerpo. Si este paso falla, el resultado puede ser pérdida del embarazo o malformaciones congénitas. Sin embargo, los científicos han dispuesto de pocas herramientas específicas humanas para ver cómo medicamentos y químicos podrían desbaratar este proceso frágil. Este estudio presenta FATE-MAP, una nueva plataforma que combina modelos con células madre, microscopía avanzada e inteligencia artificial para predecir qué compuestos pueden dañar el desarrollo humano temprano y para revelar cómo surgen esos fallos.
Construir un sustituto de laboratorio del embrión temprano
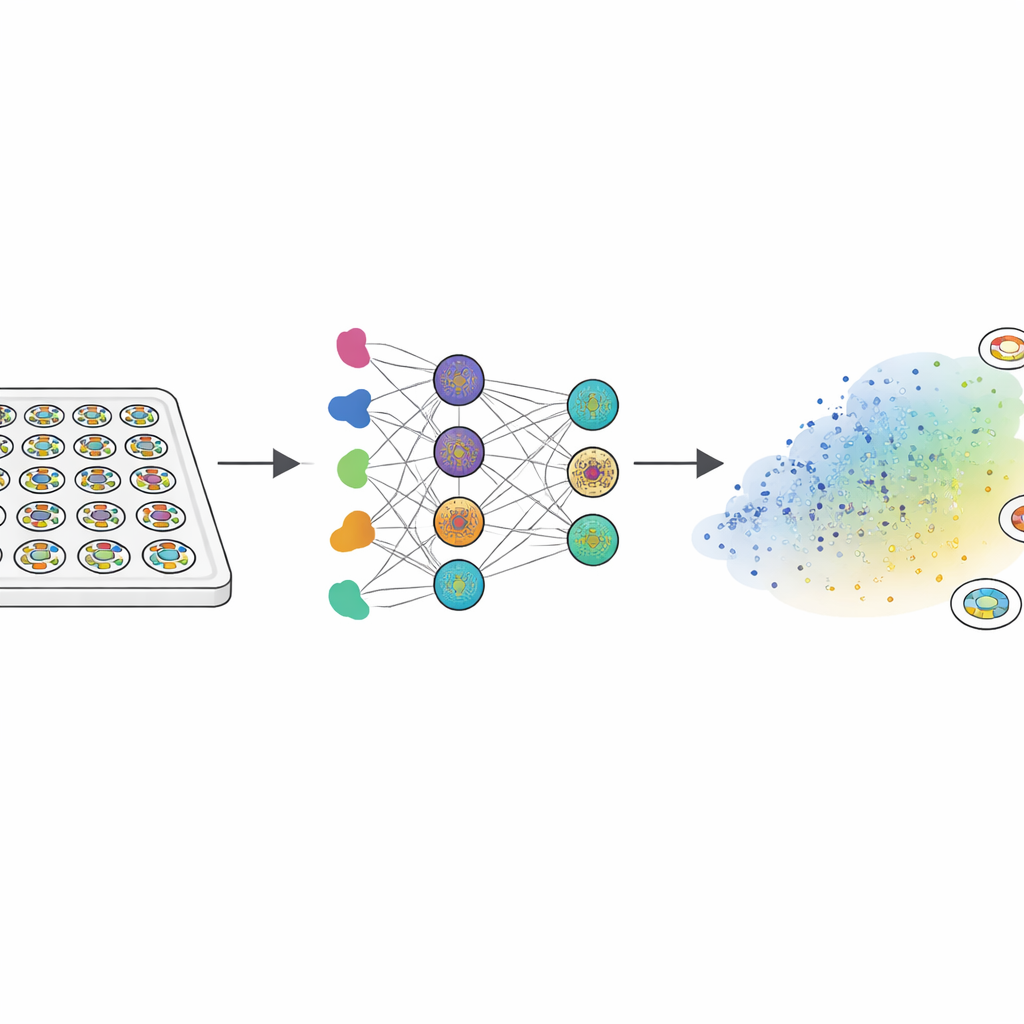
Dado que los embriones humanos reales no pueden estudiarse en profundidad, los investigadores recurrieron a “gastruloides”: pequeños discos planos cultivados a partir de células madre embrionarias humanas. Cuando se exponen a una proteína señal llamada BMP4, estos discos se autoorganizan en tres zonas concéntricas que reflejan los tejidos del embrión temprano: una región interna que mantiene rasgos de célula madre, una banda intermedia que se convierte en mesodermo (precursores de músculo, hueso y sangre) y un anillo exterior relacionado con tejido extraembrionario temprano. El equipo trató alrededor de 2000 de estas colonias con una biblioteca de 210 fármacos que apuntan a vías clave de crecimiento y señalización. Usando marcadores fluorescentes y análisis de imagen personalizado, convirtieron el patrón de cada colonia en una huella de 150 números que capturaba cómo se disponían los tres tipos de tejido del borde al centro.
Mapear patrones normales y modos de fallo
Para dar sentido a este enorme conjunto de datos, los científicos emplearon una técnica que agrupa patrones similares cerca unos de otros en un “morfospacio” bidimensional. La mayoría de las colonias se ubicaron en una región amplia donde los tres tipos de tejido aparecían en el orden radial correcto, diferenciándose principalmente en el ancho de cada anillo. Pero surgieron varios “modos de fallo” distintos: algunos patrones carecían de la región central con rasgos de célula madre, otros perdían la banda de mesodermo y algunos rompían la simetría radial por completo. Dado que tales defectos probablemente impedirían la formación adecuada del plan corporal, el equipo trató estos agrupamientos como modos de fallo del desarrollo más que como variación inocua. Este mapa se convirtió en la referencia con la que se podían comparar tanto los datos experimentales como los modelos computacionales.
Enseñar a las máquinas a predecir compuestos riesgosos
El siguiente paso fue comprobar si un ordenador podía predecir dónde caería un nuevo compuesto en ese morfospacio usando solo su fórmula química. Los autores emplearon un modelo transformer, un enfoque de aprendizaje profundo desarrollado originalmente para lenguaje, para convertir la cadena SMILES de cada molécula en una descripción numérica de alta dimensión. Una red neuronal aprendió entonces a mapear esas descripciones a las huellas de 150 números de las colonias, y una segunda red tradujo esas huellas en posiciones en el mapa del morfospacio. Para decenas de fármacos con resultados conocidos en embarazo, las predicciones puramente in silico de FATE-MAP igualaron o superaron a las principales pruebas de teratogenicidad basadas en células madre y enfoques computacionales al clasificar compuestos como riesgosos o seguros. De manera llamativa, varios teratógenos bien conocidos convergieron en el mismo conglomerado de fallo caracterizado por la pérdida de mesodermo.
Revelar cómo ocurren los fallos, no solo que ocurren
La IA de caja negra por sí sola no puede explicar por qué una colonia falla. Para añadir mecanismo, el equipo construyó un modelo matemático de cómo tres moléculas de señalización principales —BMP, Wnt y Nodal— se difunden a través de la colonia y empujan a las células hacia distintos destinos a lo largo del tiempo. Al ajustar parámetros como la densidad celular inicial y cuán resistentes son las células centrales con rasgos de célula madre a la diferenciación (capturado por una cantidad que denominan estabilidad de SOX2), pudieron simular patrones y proyectarlos en el mismo morfospacio. Esto reveló que la mayor parte de la variación normal en los patrones podía explicarse por dos ejes casi independientes: cuán compactas están las células y con qué facilidad renuncian a su identidad de célula madre. Una densidad celular menor permitió que las señales Wnt y Nodal se propagaran más hacia el interior, ensanchando la banda de mesodermo, mientras que una mayor estabilidad de SOX2 mantenía la región central en un estado más primitivo pese a las señales de diferenciación.
De las advertencias a futuros medicamentos más seguros
Finalmente, los investigadores usaron FATE-MAP para señalar dos fármacos en fase clínica sin datos humanos previos sobre embarazo como posibles teratógenos. Ambos fueron predichos, y luego confirmados experimentalmente, para producir el mismo modo de fallo por pérdida de mesodermo observado con teratógenos clásicos como los retinoides, y también causaron defectos característicos en embriones de pez cebra. En términos más generales, el trabajo muestra cómo la combinación de modelos realistas con células madre, aprendizaje automático y ecuaciones mecanicistas puede convertir el desarrollo humano temprano en un paisaje mapeable. A largo plazo, plataformas como FATE-MAP podrían ayudar a los desarrolladores de fármacos a cribar un gran número de compuestos en busca de riesgos sutiles para el desarrollo antes de que lleguen a los pacientes, al tiempo que iluminan las reglas fundamentales que guían a un embrión desde una hoja simple de células hasta un cuerpo completamente formado.
Cita: Rufo, J., Qiu, C., Han, D. et al. FATE-MAP predicts teratogenicity and human gastrulation failure modes by integrating deep learning and mechanistic modeling. Nat Commun 17, 3327 (2026). https://doi.org/10.1038/s41467-026-69596-6
Palabras clave: teratogenicidad, gastrulación, modelos con células madre, aprendizaje profundo, toxicidad del desarrollo