Clear Sky Science · pl
FATE-MAP przewiduje teratogenność i tryby niepowodzeń gastrulacji u ludzi, łącząc uczenie głębokie z modelowaniem mechanistycznym
Dlaczego błędy we wczesnym embrionie mają znaczenie
Wiele ciąż nie przechodzi przez najwcześniejsze tygodnie, często z powodów niewidocznych zarówno dla rodziców, jak i lekarzy. Jedną z krytycznych przeszkód jest etap zwany gastrulacją, kiedy prosta kula komórek reorganizuje się w podstawowe warstwy, z których powstaną wszystkie narządy. Jeśli ten etap zawiedzie, skutkiem może być utrata ciąży lub wady wrodzone. Naukowcy dysponowali niewieloma narzędziami specyficznymi dla człowieka, pozwalającymi zobaczyć, jak leki i chemikalia mogą zaburzyć ten delikatny proces. W tym badaniu przedstawiono FATE-MAP — nową platformę łączącą modele komórek macierzystych, zaawansowane obrazowanie i sztuczną inteligencję, aby prognozować, które związki mogą szkodzić wczesnemu rozwojowi człowieka i ujawniać mechanizmy tych niepowodzeń.
Tworzenie laboratoryjnego zamiennika wczesnego embrionu
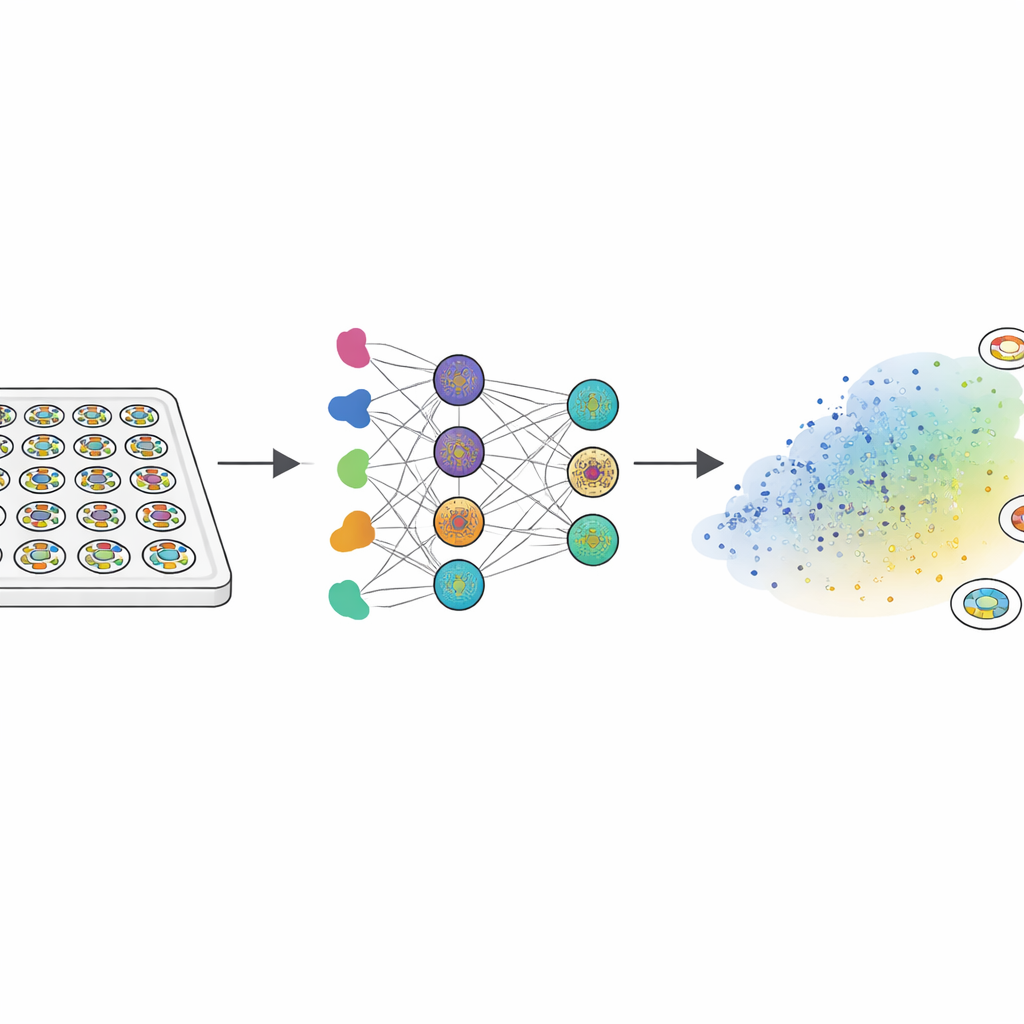
Ponieważ prawdziwych ludzkich embrionów nie można badać dogłębnie, badacze sięgnęli po „gastruloidy” — niewielkie, płaskie dyski hodowane z ludzkich embrionalnych komórek macierzystych. Po ekspozycji na białko sygnałowe BMP4 te dyski samoorganizują się w trzy koncentryczne strefy odpowiadające tkankom wczesnego embrionu: wewnętrzny obszar zachowujący cechy komórek macierzystych, środkowy pas różnicujący się w mezodermę (prekursory mięśni, kości i krwi) oraz zewnętrzny pierścień związany z wczesną tkanką pozazarodkową. Zespół poddał około 2000 takich kolonii bibliotece 210 leków celujących w kluczowe szlaki wzrostu i sygnalizacji. Dzięki znacznikom fluorescencyjnym i autorskim analizom obrazu przekształcili wzór każdej kolonii w 150‑liczbowy odcisk palca, który uchwycił rozmieszczenie trzech typów tkanek od krawędzi ku środkowi.
Mapowanie normalnych wzorców i trybów niepowodzeń
Aby zrozumieć ten ogromny zbiór danych, naukowcy wykorzystali technikę grupowania podobnych wzorców w dwuwymiarowej „morfoprzestrzeni”. Większość kolonii znalazła się w szerokim obszarze, gdzie wszystkie trzy typy tkanek pojawiały się w poprawnej kolejności radialnej, różniąc się głównie szerokością poszczególnych pierścieni. Jednak wyłoniło się kilka odrębnych „trybów niepowodzeń”: niektóre wzory pozbawione były centralnej strefy przypominającej komórki macierzyste, inne utraciły pas mezodermy, a niektóre straciły symetrię radialną. Ponieważ takie defekty prawdopodobnie uniemożliwiłyby prawidłowe uformowanie planu ciała, zespół potraktował te klastry jako tryby niepowodzeń rozwojowych, a nie nieszkodliwą zmienność. Ta mapa stała się punktem odniesienia, względem którego porównywano dane eksperymentalne i modele komputerowe.
Uczenie komputerów przewidywania ryzykownych związków
Następnym krokiem było sprawdzenie, czy komputer potrafi przewidzieć, gdzie nowy związek znajdzie się w tej morfoprzestrzeni, używając jedynie jego wzoru chemicznego. Autorzy zastosowali model transformer — podejście uczenia głębokiego opracowane pierwotnie do języka — aby przekształcić ciąg SMILES każdej cząsteczki w wysokowymiarowy opis numeryczny. Sieć neuronowa nauczyła się mapować te opisy na 150‑liczbowe odciski koloni, a druga sieć tłumaczyła te odciski na pozycje w mapie morfoprzestrzeni. Dla dziesiątek leków o znanych wynikach w ciąży, czysto in silico przewidywania FATE‑MAP porównały się z najlepszymi testami teratogenności opartymi na komórkach macierzystych i modelach obliczeniowych i często je przewyższały w klasyfikowaniu związków jako ryzykowne lub bezpieczne. Co istotne, kilka dobrze znanych teratogenów zbiegało się w tym samym klastrze niepowodzeń charakteryzującym się utratą mezodermy.
Ujawnianie, jak zachodzą niepowodzenia, a nie tylko że zachodzą
Sama „czarna skrzynka” AI nie wyjaśnia, dlaczego kolonia zawodzi. Aby dodać warstwę mechanistyczną, zespół zbudował model matematyczny opisujący, jak trzy główne cząsteczki sygnałowe — BMP, Wnt i Nodal — rozprzestrzeniają się po kolonii i kierują komórki ku różnym losom w czasie. Poprzez dostosowanie parametrów takich jak początkowa gęstość komórek oraz jak odporne na różnicowanie są centralne komórki o cechach macierzystych (opisane wielkością, którą nazwali stabilnością SOX2), mogli symulować wzory i projektować je do tej samej morfoprzestrzeni. Wyjawiło to, że większość normalnej zmienności wzorców można wytłumaczyć dwoma niemal niezależnymi osiami: gęstością komórek i tym, jak łatwo komórki porzucają swoją macierzystą tożsamość. Niższa gęstość komórek pozwalała sygnałom Wnt i Nodal rozprzestrzeniać się dalej do wnętrza, poszerzając pas mezodermy, podczas gdy wyższa stabilność SOX2 utrzymywała centralny obszar w bardziej prymitywnym stanie pomimo sygnałów różnicujących.
Od ostrzeżeń do bezpieczniejszych leków w przyszłości
Na koniec badacze użyli FATE‑MAP, aby oznaczyć dwa leki na etapie klinicznym, dla których brakowało wcześniejszych danych z ciąż ludzkich, jako potencjalne teratogeny. Oba zostały przewidziane, a następnie eksperymentalnie potwierdzone, że wywołują ten sam tryb utraty mezodermy obserwowany przy klasycznych teratogenach retinoidowych, i powodowały charakterystyczne defekty u embrionów zebrafish. Szerzej rzecz biorąc, praca pokazuje, jak połączenie realistycznych modeli komórek macierzystych, uczenia maszynowego i równań mechanistycznych może zmienić wczesny rozwój człowieka w mappable krajobraz. W długiej perspektywie platformy takie jak FATE‑MAP mogą pomóc producentom leków przesiewać ogromne liczby związków pod kątem subtelnych ryzyk rozwojowych, zanim dotrą one do pacjentów, jednocześnie oświetlając fundamentalne zasady, które prowadzą embrion od prostej warstwy komórek do w pełni ukształtowanego ciała.
Cytowanie: Rufo, J., Qiu, C., Han, D. et al. FATE-MAP predicts teratogenicity and human gastrulation failure modes by integrating deep learning and mechanistic modeling. Nat Commun 17, 3327 (2026). https://doi.org/10.1038/s41467-026-69596-6
Słowa kluczowe: teratogenność, gastrulacja, modele komórek macierzystych, uczenie głębokie, toksyczność rozwojowa