Clear Sky Science · it
FATE-MAP prevede la teratogenicità e le modalità di fallimento della gastrulazione umana integrando deep learning e modellizzazione meccanicistica
Perché gli errori nell’embrione precoce contano
Molte gravidanze non superano le prime settimane, spesso per ragioni che rimangono invisibili sia ai genitori sia ai medici. Una tappa critica è la gastrulazione, quando una semplice sfera di cellule si riorganizza nei livelli fondamentali che daranno origine a tutti gli organi del corpo. Se questo passaggio fallisce, il risultato può essere una perdita della gravidanza o malformazioni congenite. Tuttavia, gli scienziati hanno avuto pochi strumenti specifici per l’uomo in grado di mostrare come farmaci e agenti chimici possano compromettere questo processo fragile. Questo studio presenta FATE-MAP, una nuova piattaforma che combina modelli di cellule staminali, imaging avanzato e intelligenza artificiale per prevedere quali composti possono danneggiare lo sviluppo umano precoce e per rivelare come si manifestano questi fallimenti.
Costruire un sostituto di laboratorio per l’embrione precoce
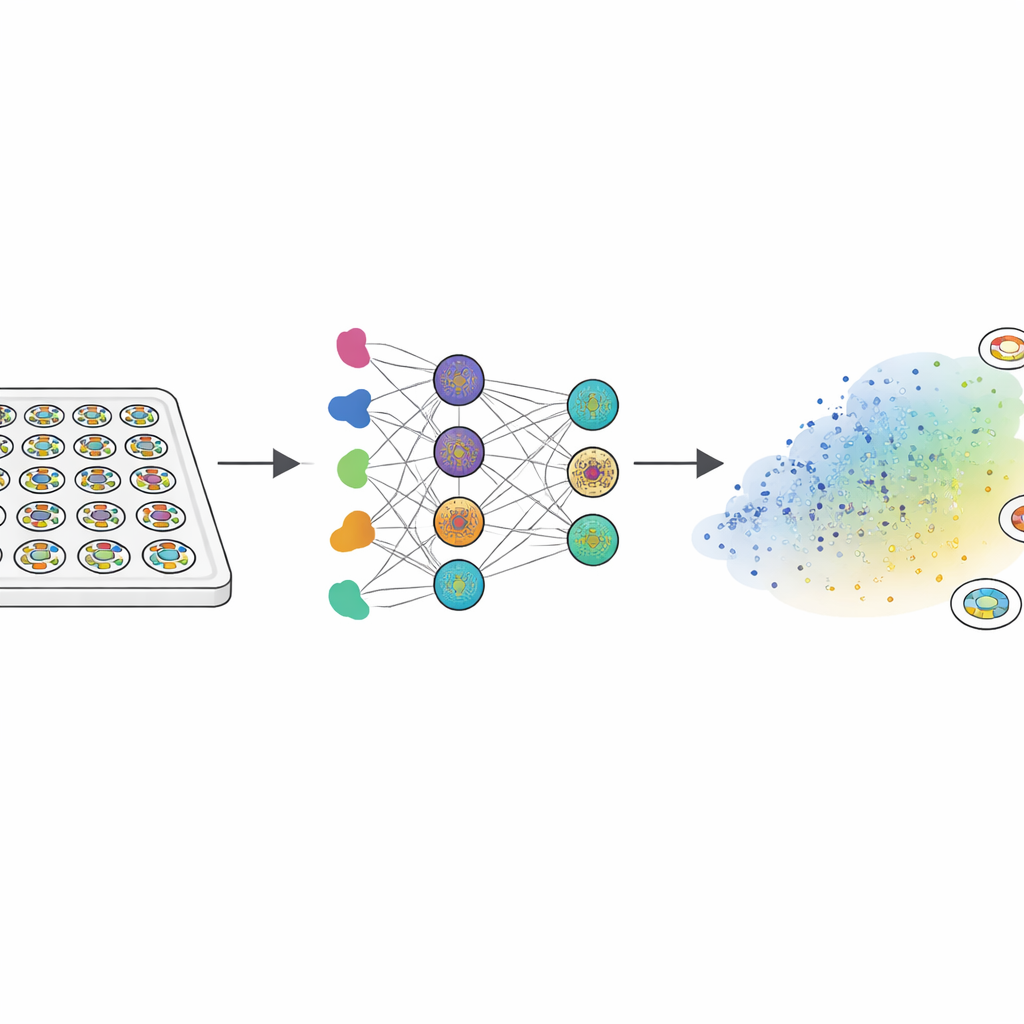
Poiché gli embrioni umani reali non possono essere studiati in profondità, i ricercatori si sono rivolti ai “gastruloidi”: piccoli dischi piatti ottenuti da cellule staminali embrionali umane. Quando esposti a una proteina di segnalazione chiamata BMP4, questi dischi si auto-organizzano in tre zone concentriche che riflettono i tessuti embrionali precoci: una regione interna che rimane staminale, una fascia intermedia che diventa mesoderma (precursori di muscoli, ossa e sangue) e un anello esterno correlato ai tessuti extra‑embrionali precoci. Il team ha trattato circa 2000 di queste colonie con una libreria di 210 farmaci che prendono di mira vie chiave di crescita e segnalazione. Usando marcatori fluorescenti e analisi d’immagine personalizzate, hanno trasformato il pattern di ciascuna colonia in un’impronta a 150 numeri che catturava come i tre tipi di tessuto erano disposti dal bordo al centro.
Mappare i pattern normali e le modalità di fallimento
Per interpretare questo enorme set di dati, gli scienziati hanno usato una tecnica che raggruppa pattern simili vicini in uno “spazio morfologico” bidimensionale. La maggior parte delle colonie ricadeva in una vasta regione in cui i tre tipi di tessuto apparivano nell’ordine radiale corretto, differendo principalmente nella larghezza di ciascun anello. Ma sono emerse diverse «modalità di fallimento» distinte: alcuni pattern mancavano della regione centrale staminale, altri perdevano la fascia del mesoderma e alcuni rompevano del tutto la simmetria radiale. Poiché tali difetti probabilmente impedirebbero la corretta formazione del piano corporeo, il team ha trattato questi cluster come modalità di fallimento dello sviluppo piuttosto che come variazione innocua. Questa mappa è diventata il riferimento rispetto al quale sono stati confrontati sia i dati sperimentali sia i modelli computazionali.
Addestrare i computer a prevedere composti rischiosi
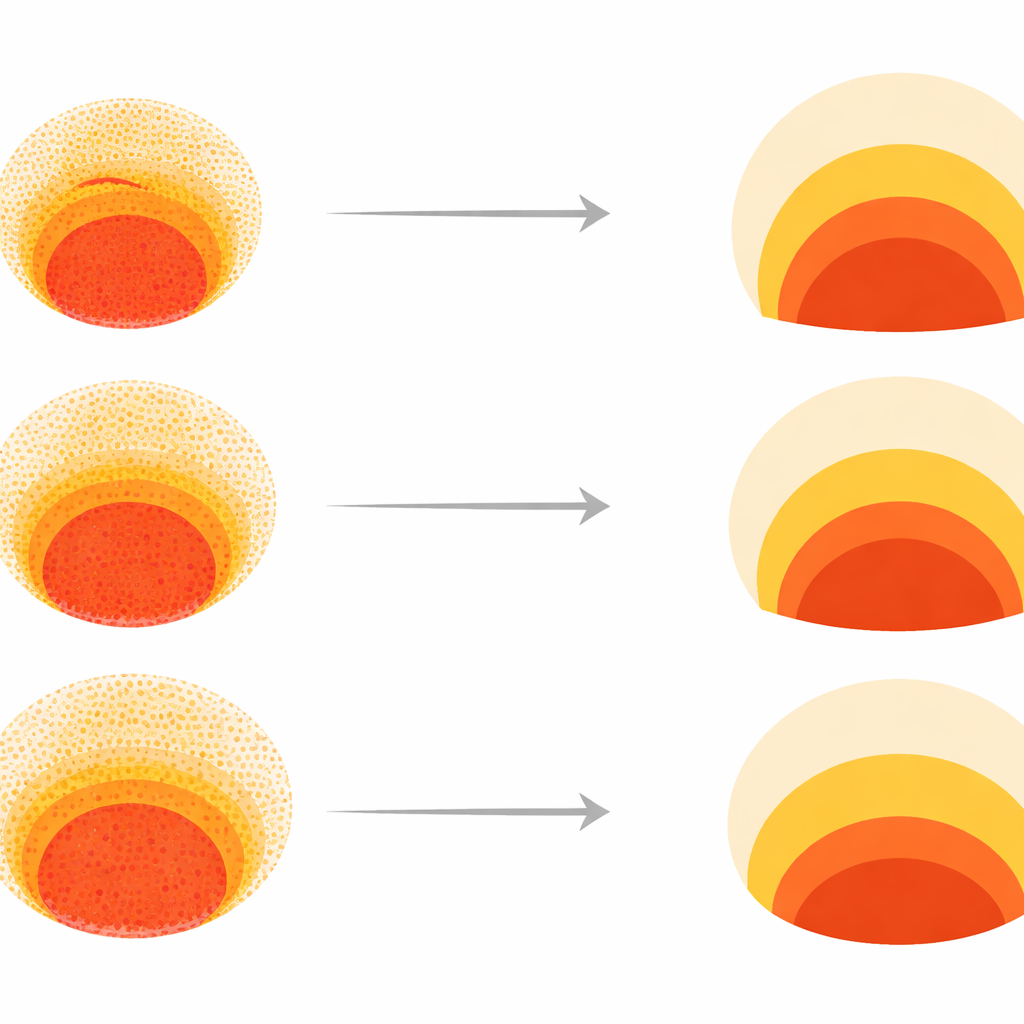
Il passo successivo è stato verificare se un computer potesse predire dove si sarebbe collocato un nuovo composto in questo spazio morfologico usando solo la sua formula chimica. Gli autori hanno impiegato un modello transformer — un approccio di deep learning originariamente sviluppato per il linguaggio — per convertire la stringa SMILES di ogni molecola in una descrizione numerica ad alta dimensionalità. Una rete neurale ha poi imparato a mappare queste descrizioni sulle impronte a 150 numeri delle colonie, e una seconda rete ha tradotto quelle impronte in posizioni sulla mappa dello spazio morfologico. Per dozzine di farmaci con esiti di gravidanza noti, le previsioni puramente in silico di FATE-MAP hanno eguagliato o superato i principali test teratogenicità basati su cellule staminali e modelli computazionali nel classificare i composti come rischiosi o sicuri. Sorprendentemente, diversi teratogeni ben noti convergevano tutti sullo stesso cluster di fallimento caratterizzato dalla perdita del mesoderma.
Rivelare come avvengono i fallimenti, non solo che avvengano
L’intelligenza artificiale a scatola nera da sola non può spiegare perché una colonia fallisca. Per aggiungere meccanismo, il team ha costruito un modello matematico di come tre principali molecole di segnalazione — BMP, Wnt e Nodal — si diffondono nella colonia e indirizzano le cellule verso destini differenti nel tempo. Modificando parametri come la densità cellulare iniziale e la resistenza delle cellule centrali staminali alla differenziazione (catturata da una quantità che chiamano stabilità di SOX2), hanno potuto simulare pattern e proiettarli nello stesso spazio morfologico. Ciò ha rivelato che la maggior parte della variazione normale nei pattern poteva essere spiegata da due assi quasi indipendenti: quanto sono fitte le cellule e quanto facilmente rinunciano alla loro identità staminale. Una densità cellulare più bassa permetteva ai segnali Wnt e Nodal di propagarsi più verso l’interno, allargando la fascia del mesoderma, mentre una maggiore stabilità di SOX2 manteneva la regione centrale in uno stato più primitivo nonostante i segnali di differenziazione.
Da avvisi a futuri farmaci più sicuri
Infine, i ricercatori hanno usato FATE-MAP per segnalare due farmaci in fase clinica, privi di dati precedenti su gravidanze umane, come potenziali teratogeni. Entrambi sono stati previsti, e poi confermati sperimentalmente, come in grado di produrre la stessa modalità di fallimento per perdita di mesoderma osservata con i classici teratogeni retinoidi, e hanno inoltre causato difetti caratteristici negli embrioni di zebrafish. Più in generale, il lavoro dimostra come la combinazione di modelli realistici di cellule staminali, apprendimento automatico ed equazioni meccanicistiche possa trasformare lo sviluppo umano precoce in un paesaggio mappabile. A lungo termine, piattaforme come FATE-MAP potrebbero aiutare gli sviluppatori di farmaci a screeningare un gran numero di composti per rischi sviluppativi sottili prima che raggiungano i pazienti, illuminando al contempo le regole fondamentali che guidano un embrione da un semplice strato di cellule verso un corpo completamente formato.
Citazione: Rufo, J., Qiu, C., Han, D. et al. FATE-MAP predicts teratogenicity and human gastrulation failure modes by integrating deep learning and mechanistic modeling. Nat Commun 17, 3327 (2026). https://doi.org/10.1038/s41467-026-69596-6
Parole chiave: teratogenicità, gastrulazione, modelli di cellule staminali, deep learning, tossicità dello sviluppo