Clear Sky Science · de
FATE-MAP sagt Teratogenität und Fehlformen der menschlichen Gastrulation voraus, indem es Deep Learning und mechanistische Modellierung integriert
Warum Fehler im frühen Embryo wichtig sind
Viele Schwangerschaften überstehen die ersten Wochen nicht, oft aus Gründen, die für Eltern und Ärztinnen/Ärzte unsichtbar bleiben. Eine entscheidende Hürde ist die Gastrulation, eine Phase, in der sich eine einfache Zellkugel in die Grundschichten umorganisiert, aus denen sich später alle Organe bilden. Misslingt dieser Schritt, kann das zu Schwangerschaftsverlust oder Geburtsfehlern führen. Wissenschaftlern standen jedoch nur wenige humanspezifische Werkzeuge zur Verfügung, um zu untersuchen, wie Medikamente und Chemikalien diesen empfindlichen Prozess stören könnten. Diese Studie stellt FATE-MAP vor, eine neue Plattform, die Stammzellmodelle, fortgeschrittene Bildgebung und künstliche Intelligenz kombiniert, um vorherzusagen, welche Verbindungen die frühe menschliche Entwicklung gefährden könnten, und um aufzuzeigen, wie diese Fehlentwicklungen entstehen.
Ein Labor‑Ersatz für den frühen Embryo
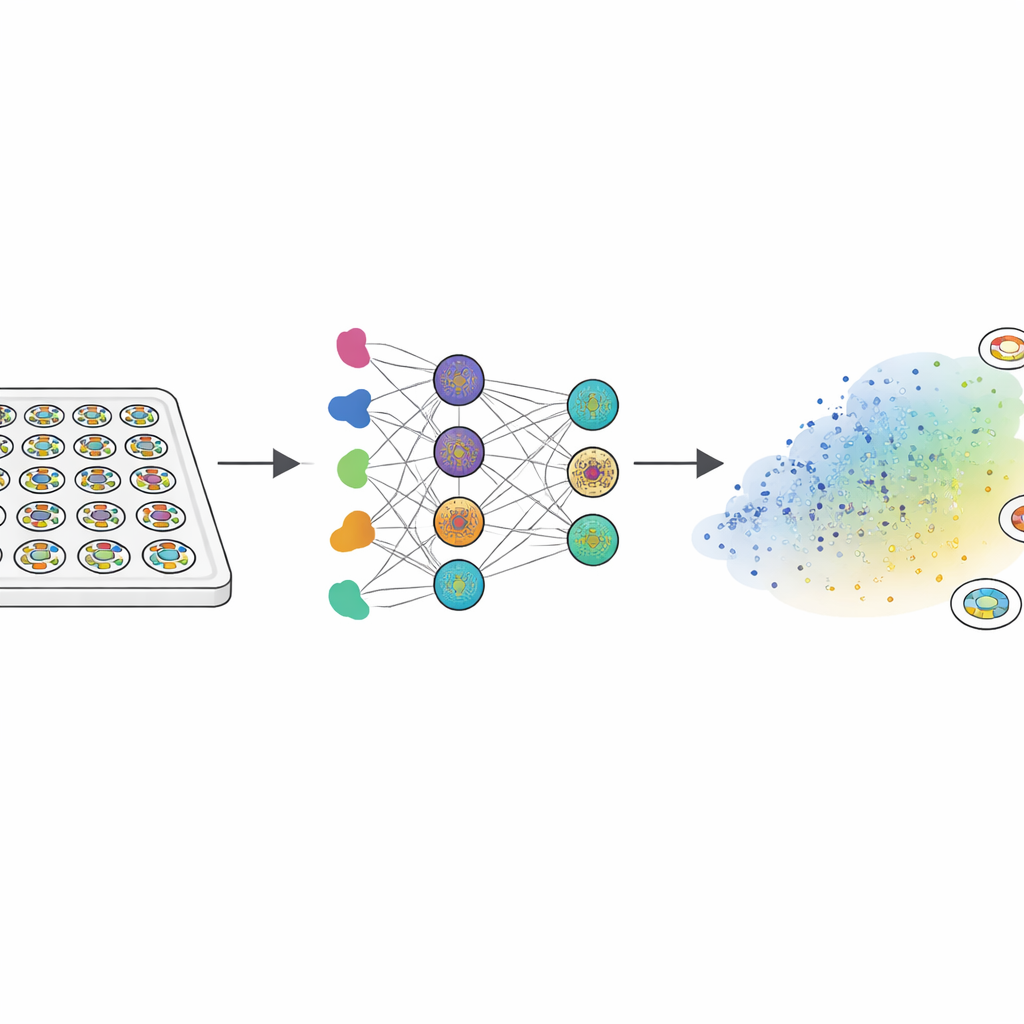
Da sich echte menschliche Embryonen nicht eingehend untersuchen lassen, nutzten die Forschenden sogenannte „Gastruloide“ — winzige, flache Scheiben, die aus humanen embryonalen Stammzellen gezüchtet werden. Bei Exposition gegenüber einem Signalprotein namens BMP4 organisieren sich diese Scheiben selbst und bilden drei konzentrische Zonen, die frühe embryonale Gewebe widerspiegeln: eine innere Region, die stammzellähnlich bleibt, einen mittleren Ring, der Mesoderm (Vorläufer von Muskeln, Knochen und Blut) bildet, und einen äußeren Ring, der frühem extraembryonalen Gewebe entspricht. Das Team behandelte etwa 2000 dieser Kolonien mit einer Bibliothek von 210 Wirkstoffen, die zentrale Wachstums- und Signalwege ansprechen. Mit Fluoreszenzmarkern und maßgeschneiderter Bildanalyse verwandelten sie das Muster jeder Kolonie in einen 150‑Zahlen starken Fingerabdruck, der erfasste, wie die drei Gewebetypen vom Rand zur Mitte angeordnet waren.
Normale Muster und Fehler‑Modi kartieren
Um dieses große Datenset zu strukturieren, verwendeten die Wissenschaftler eine Technik, die ähnliche Muster in einem zweidimensionalen „Morphoraum“ nahe zueinander gruppiert. Die meisten Kolonien lagen in einem breiten Bereich, in dem alle drei Gewebetypen in der korrekten radialen Reihenfolge auftauchten und sich hauptsächlich in der Breite der Ringe unterschieden. Es traten jedoch mehrere eindeutige „Fehlmodi“ auf: Einige Muster fehlten die zentrale stammzellähnliche Region, andere verloren den Mesoderm‑Streifen, und manche brachen die radiale Symmetrie völlig auf. Da solche Defekte die richtige Körperplanbildung wahrscheinlich verhindern würden, betrachtete das Team diese Cluster als Entwicklungsfehler und nicht als harmlose Variationen. Diese Karte wurde zur Referenz, anhand derer experimentelle Daten und Computermodelle verglichen werden konnten.
Computern beibringen, riskante Verbindungen vorherzusagen
Der nächste Schritt bestand darin zu prüfen, ob ein Computer vorhersagen kann, wo eine neue Verbindung in diesem Morphoraum landen würde, allein anhand ihrer chemischen Formel. Die Autorinnen und Autoren nutzten ein Transformer‑Modell — einen Deep‑Learning‑Ansatz, der ursprünglich für Sprache entwickelt wurde —, um die SMILES‑Strings jeder Verbindung in eine hochdimensionale numerische Beschreibung zu übersetzen. Ein neuronales Netzwerk lernte dann, diese Beschreibungen auf die 150‑Zahlen‑Koloniefingerabdrücke abzubilden, und ein zweites Netzwerk übersetzte diese Fingerabdrücke in Positionen im Morphoraum. Bei Dutzenden von Wirkstoffen mit bekannten Schwangerschaftsauswirkungen entsprachen FATE‑MAPs rein in silico‑Vorhersagen — oder übertrafen — führende Stammzell‑ und rechnerische Teratogenitätstests bei der Klassifizierung von Verbindungen als riskant oder sicher. Auffällig war, dass mehrere bekannte Teratogene alle in demselben Fehler‑Cluster zusammenliefen, das durch den Verlust des Mesoderms charakterisiert ist.
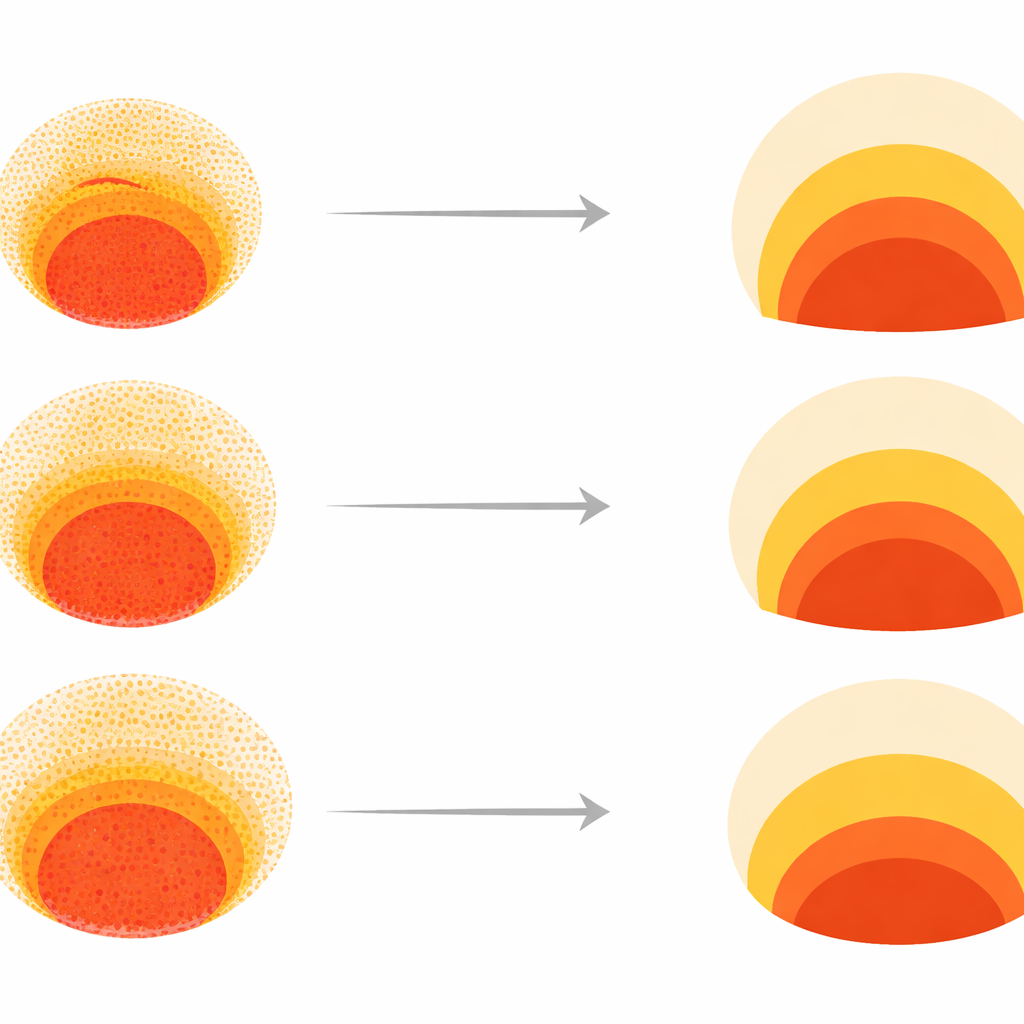
Aufdecken, wie Fehler entstehen, nicht nur dass sie auftreten
Black‑Box‑KI allein kann nicht erklären, warum eine Kolonie versagt. Um Mechanismen zu ergänzen, entwickelten die Forschenden ein mathematisches Modell, das beschreibt, wie drei wichtige Signalmoleküle — BMP, Wnt und Nodal — sich in der Kolonie ausbreiten und im Lauf der Zeit Zellen in unterschiedliche Schicksale treiben. Durch Anpassen von Parametern wie der Anfangszell‑Dichte und wie resistent die zentralen stammzellähnlichen Zellen gegen Differenzierung sind (erfasst durch eine Größe, die sie SOX2‑Stabilität nennen), konnten sie Muster simulieren und in denselben Morphoraum projizieren. Dies zeigte, dass die meiste normale Variation der Muster durch zwei nahezu unabhängige Achsen erklärt werden kann: wie dicht die Zellen sitzen und wie leicht sie ihre stammzellähnliche Identität aufgeben. Niedrigere Zelldichte erlaubte es Wnt‑ und Nodal‑Signalen, weiter nach innen zu reichen und den Mesoderm‑Streifen zu verbreitern, während höhere SOX2‑Stabilität die zentrale Region trotz Differenzierungsreizen in einem primitiveren Zustand hielt.
Von Warnungen zu künftig sichereren Medikamenten
Schließlich nutzten die Forschenden FATE‑MAP, um zwei klinisch entwickelte Wirkstoffe ohne vorherige Daten zur Anwendung in der menschlichen Schwangerschaft als potenzielle Teratogene zu markieren. Beide wurden vorhergesagt und anschließend experimentell bestätigt, denselben mesoderm‑verlustbedingten Fehlmodus zu erzeugen, wie er bei klassischen Retinoid‑Teratogenen beobachtet wird, und sie verursachten zudem charakteristische Defekte in Zebrafisch‑Embryonen. Allgemeiner zeigt die Arbeit, wie die Kombination realistischer Stammzellmodelle, maschinellem Lernen und mechanistischer Gleichungen die frühe menschliche Entwicklung in eine kartierbare Landschaft verwandeln kann. Langfristig könnten Plattformen wie FATE‑MAP Arzneimittelentwicklern helfen, große Mengen von Verbindungen auf subtile Entwicklungsrisiken zu screenen, bevor sie Patienten erreichen, und zugleich die grundlegenden Regeln zu beleuchten, die einen Embryo aus einem einfachen Zellblatt zu einem vollständig ausgebildeten Körper führen.
Zitation: Rufo, J., Qiu, C., Han, D. et al. FATE-MAP predicts teratogenicity and human gastrulation failure modes by integrating deep learning and mechanistic modeling. Nat Commun 17, 3327 (2026). https://doi.org/10.1038/s41467-026-69596-6
Schlüsselwörter: Teratogenität, Gastrulation, Stammzellmodelle, Deep Learning, Entwicklungstoxizität