Clear Sky Science · fr
FATE-MAP prédit la tératogénicité et les modes d’échec de la gastrulation humaine en intégrant apprentissage profond et modélisation mécaniste
Pourquoi les erreurs précoces de l’embryon comptent
De nombreuses grossesses ne dépassent jamais les premières semaines, souvent pour des raisons invisibles aux parents comme aux médecins. Un obstacle critique est une étape appelée gastrulation, lorsque une simple boule de cellules se réorganise en couches de base qui formeront tous les organes du corps. Si cette étape échoue, le résultat peut être une perte de grossesse ou des malformations congénitales. Pourtant, les scientifiques disposaient de peu d’outils spécifiquement humains pour voir comment des médicaments et des produits chimiques pourraient faire dérailler ce processus fragile. Cette étude présente FATE-MAP, une plateforme qui combine modèles de cellules souches, imagerie avancée et intelligence artificielle pour prévoir quels composés peuvent nuire au développement humain précoce et pour révéler comment ces échecs surviennent.
Construire un substitut de laboratoire de l’embryon précoce
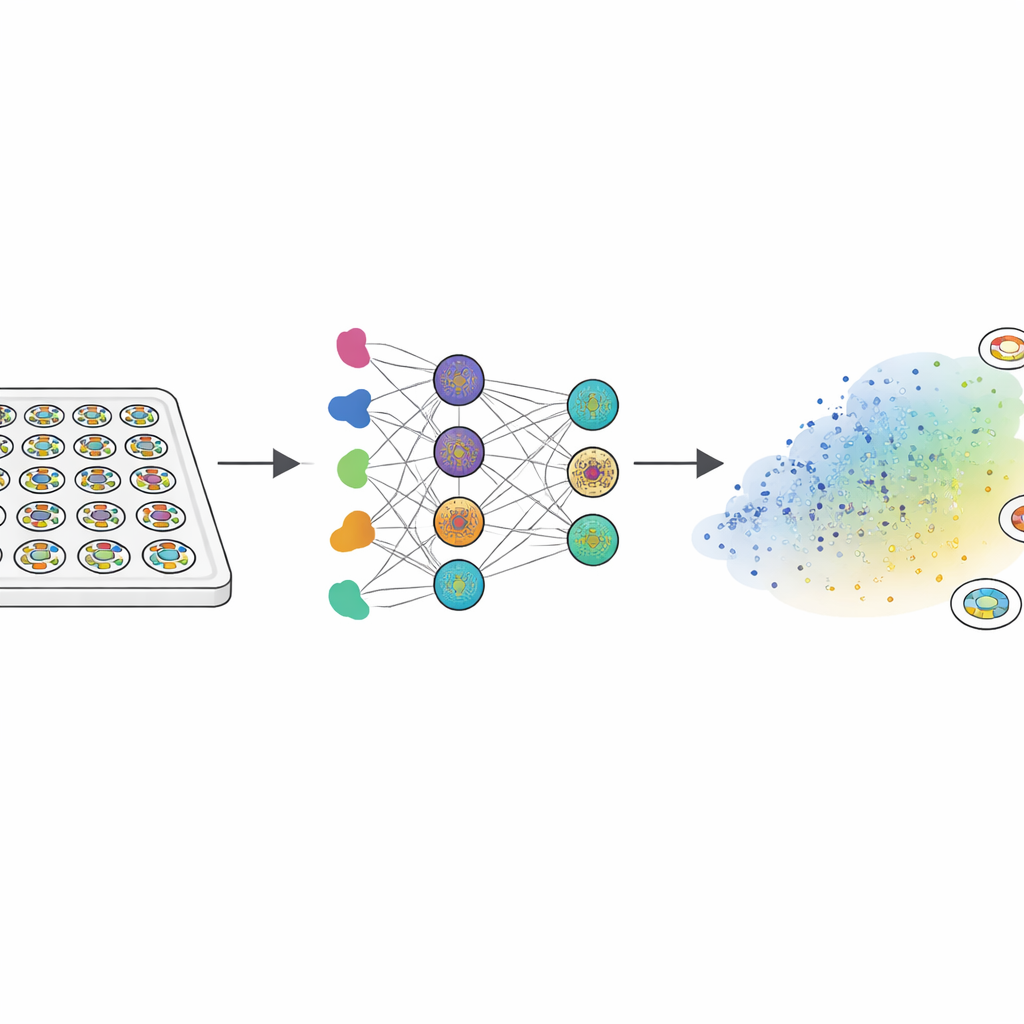
Comme les vrais embryons humains ne peuvent pas être étudiés en profondeur, les chercheurs ont recours aux « gastruloïdes » — de disques minuscules et plats cultivés à partir de cellules souches embryonnaires humaines. Lorsqu’on les expose à une protéine de signalisation appelée BMP4, ces disques s’auto‑organisent en trois zones concentriques qui reflètent les tissus de l’embryon précoce : une région centrale qui reste semblable à des cellules souches, une bande médiane qui devient mésoderme (précurseurs du muscle, des os et du sang), et un anneau externe lié aux tissus extra‑embryonnaires précoces. L’équipe a traité environ 2000 de ces colonies avec une bibliothèque de 210 médicaments ciblant des voies de croissance et de signalisation clés. À l’aide de marqueurs fluorescents et d’une analyse d’images sur mesure, ils ont transformé le motif de chaque colonie en une empreinte de 150 nombres capturant l’agencement des trois types tissulaires de la périphérie au centre.
Cartographier les motifs normaux et les modes d’échec
Pour donner du sens à cet énorme jeu de données, les scientifiques ont utilisé une technique regroupant des motifs similaires proches les uns des autres dans un « morphospaces » bidimensionnel. La plupart des colonies se situaient dans une vaste région où les trois types tissulaires apparaissaient dans le bon ordre radial, la variance principale portant sur la largeur de chaque anneau. Mais plusieurs « modes d’échec » distincts ont émergé : certains motifs manquaient de la région centrale stem‑like, d’autres perdaient la bande mésodermique, et certains brisaient complètement la symétrie radiale. Parce que de tels défauts empêcheraient probablement la formation correcte du plan corporel, l’équipe a considéré ces groupes comme des modes d’échec du développement plutôt que comme des variations bénignes. Cette carte est devenue la référence contre laquelle les données expérimentales et les modèles informatiques pouvaient être comparés.
Apprendre aux ordinateurs à prédire les composés à risque
L’étape suivante consistait à vérifier si un ordinateur pouvait prédire où un nouveau composé se placerait dans ce morphospaces en n’utilisant que sa formule chimique. Les auteurs ont utilisé un modèle Transformer — une approche d’apprentissage profond initialement développée pour le langage — pour convertir la chaîne SMILES de chaque molécule en une description numérique à haute dimension. Un réseau neuronal a ensuite appris à mapper ces descriptions sur les empreintes de 150 nombres des colonies, et un second réseau a traduit ces empreintes en positions sur la carte morphospaciale. Pour des dizaines de médicaments dont les effets pendant la grossesse sont connus, les prédictions purement in silico de FATE‑MAP égalent ou surpassent les meilleurs tests tératogènes basés sur cellules souches et les approches computationnelles pour classer les composés en risques ou sûrs. Fait remarquable, plusieurs tératogènes bien connus convergent tous vers le même groupe d’échec caractérisé par la perte de mésoderme.
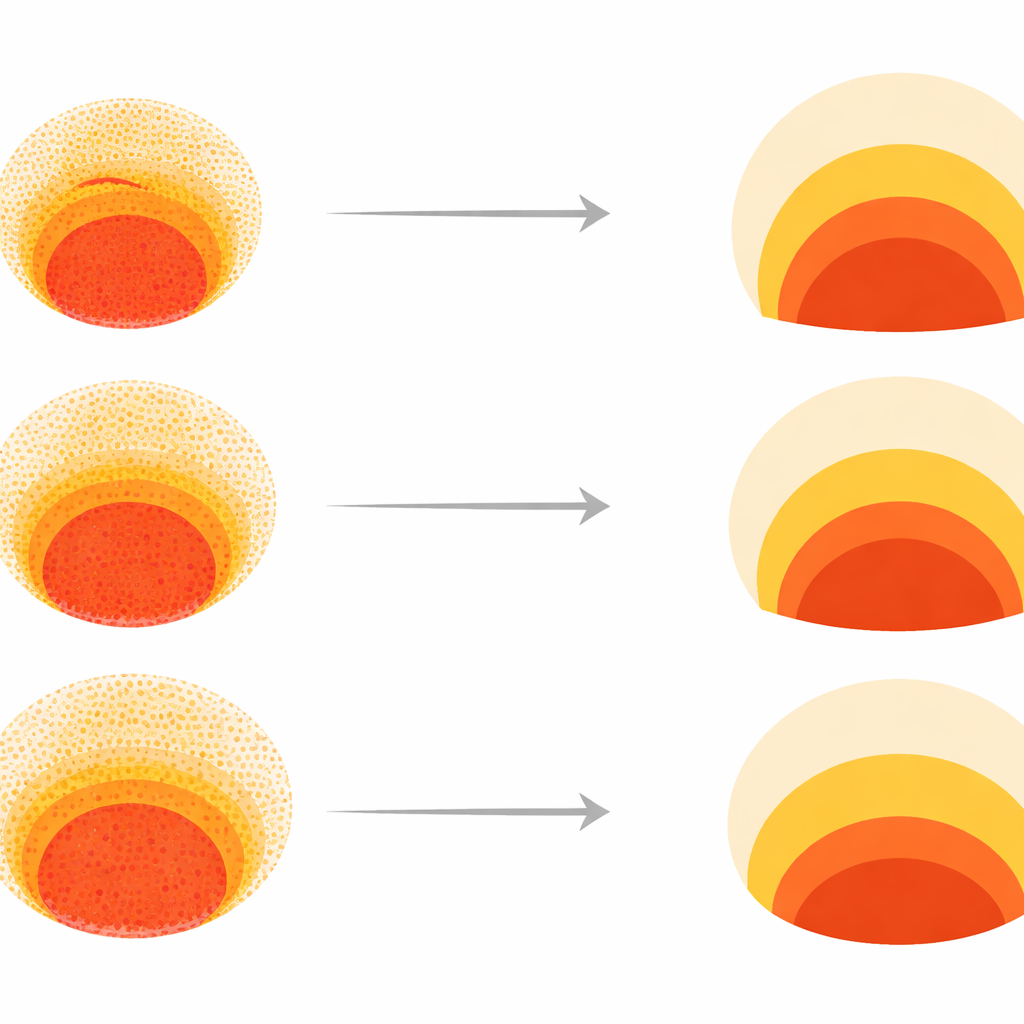
Révéler comment les échecs se produisent, pas seulement qu’ils existent
Une IA boîte noire ne peut pas, à elle seule, expliquer pourquoi une colonie échoue. Pour ajouter du mécanisme, l’équipe a construit un modèle mathématique de la façon dont trois molécules de signalisation majeures — BMP, Wnt et Nodal — se diffusent à travers la colonie et poussent les cellules vers différents destins au fil du temps. En ajustant des paramètres tels que la densité cellulaire initiale et la résistance des cellules centrales de type souche à la différenciation (capturée par une quantité qu’ils appellent stabilité de SOX2), ils ont pu simuler des motifs et les projeter dans le même morphospaces. Cela a révélé que la majorité de la variation normale des motifs pouvait s’expliquer par deux axes presque indépendants : à quel point les cellules sont denses et à quelle facilité elles renoncent à leur identité de cellules souches. Une densité cellulaire plus faible permettait aux signaux Wnt et Nodal de se propager plus loin vers l’intérieur, élargissant la bande mésodermique, tandis qu’une stabilité SOX2 élevée maintenait la région centrale dans un état plus primitif malgré les signaux de différenciation.
Des avertissements vers des médicaments futurs plus sûrs
Enfin, les chercheurs ont utilisé FATE‑MAP pour signaler deux médicaments en phase clinique sans données antérieures chez l’humain comme potentiels tératogènes. Les deux ont été prédits, puis confirmés expérimentalement, comme produisant le même mode d’échec par perte de mésoderme observé avec des tératogènes rétinoïdes classiques, et ils ont aussi provoqué des défauts caractéristiques chez des embryons de poisson zèbre. Plus largement, ce travail montre comment la combinaison de modèles réalistes de cellules souches, d’apprentissage automatique et d’équations mécanistes peut transformer le développement humain précoce en un paysage cartographiable. À terme, des plateformes comme FATE‑MAP pourraient aider les développeurs de médicaments à dépister d’énormes bibliothèques de composés pour des risques développementaux subtils avant qu’ils n’atteignent les patients, tout en éclairant les règles fondamentales qui guident un embryon, d’une simple feuille de cellules, vers un corps entièrement formé.
Citation: Rufo, J., Qiu, C., Han, D. et al. FATE-MAP predicts teratogenicity and human gastrulation failure modes by integrating deep learning and mechanistic modeling. Nat Commun 17, 3327 (2026). https://doi.org/10.1038/s41467-026-69596-6
Mots-clés: tératogénicité, gastrulation, modèles de cellules souches, apprentissage profond, toxicité développementale