Clear Sky Science · pt
FATE-MAP prevê teratogenicidade e modos de falha da gastrulação humana integrando aprendizado profundo e modelagem mecanicista
Por que os erros no embrião precoce importam
Muitas gestações não chegam a passar das primeiras semanas, frequentemente por razões que permanecem invisíveis tanto para os pais quanto para os médicos. Um obstáculo crítico é uma etapa chamada gastrulação, quando uma bola simples de células se reorganiza nas camadas básicas que formarão todos os órgãos do corpo. Se essa etapa falhar, o resultado pode ser perda da gravidez ou malformações congênitas. No entanto, os cientistas dispõem de poucas ferramentas específicas humanas para ver como medicamentos e produtos químicos podem desviar esse processo frágil. Este estudo apresenta o FATE-MAP, uma nova plataforma que combina modelos com células‑tronco, imagem avançada e inteligência artificial para prever quais compostos podem prejudicar o desenvolvimento humano precoce e revelar como essas falhas surgem.
Construindo um substituto de laboratório para o embrião precoce
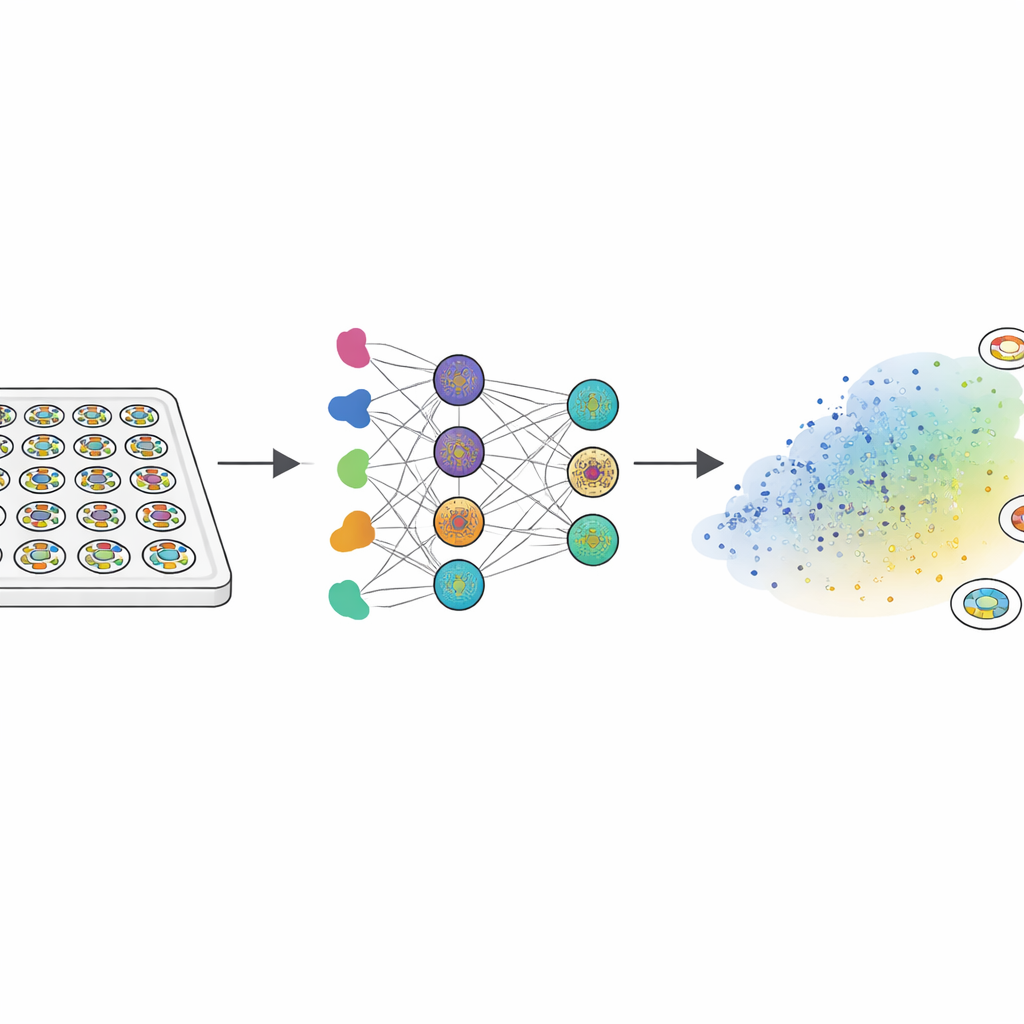
Como embriões humanos reais não podem ser estudados em profundidade, os pesquisadores recorreram a “gastruloides” — pequenos discos planos cultivados a partir de células‑tronco embrionárias humanas. Quando expostos a uma proteína sinalizadora chamada BMP4, esses discos se autoorganizavam em três zonas concêntricas que espelham os tecidos do embrião precoce: uma região interna que permanece semelhante a células‑tronco, uma faixa intermediária que se torna mesoderma (precursores de músculo, osso e sangue) e um anel externo relacionado ao tecido extraembrionário inicial. A equipe tratou cerca de 2000 dessas colônias com uma biblioteca de 210 fármacos que atingem vias-chave de crescimento e sinalização. Usando marcadores fluorescentes e análise de imagem personalizada, transformaram o padrão de cada colônia em uma impressão digital de 150 números que capturava como os três tipos de tecido estavam organizados do bordo ao centro.
Mapeando padrões normais e modos de falha
Para entender esse conjunto de dados enorme, os cientistas usaram uma técnica que agrupa padrões semelhantes próximos uns dos outros em um “morfoespaço” bidimensional. A maioria das colônias caiu em uma ampla região onde os três tipos de tecido apareciam na ordem radial correta, diferindo principalmente na largura de cada anel. Mas vários “modos de falha” distintos emergiram: alguns padrões careciam da região central semelhante a células‑tronco, outros perderam a faixa de mesoderma, e alguns quebraram a simetria radial por completo. Como tais defeitos provavelmente impediriam a formação correta do plano corporal, a equipe tratou esses agrupamentos como modos de falha do desenvolvimento em vez de variação inofensiva. Esse mapa tornou‑se a referência contra a qual tanto os dados experimentais quanto os modelos computacionais podiam ser comparados.
Ensinando computadores a prever compostos arriscados
O passo seguinte foi verificar se um computador poderia prever onde um novo composto cairia nesse morfoespaço usando apenas sua fórmula química. Os autores usaram um modelo transformer — uma abordagem de aprendizado profundo originalmente desenvolvida para linguagem — para converter a string SMILES de cada molécula em uma descrição numérica de alta dimensão. Uma rede neural então aprendeu a mapear essas descrições para as impressões digitais de 150 números das colônias, e uma segunda rede traduziu essas impressões em posições no mapa do morfoespaço. Para dezenas de fármacos com resultados gestacionais conhecidos, as previsões puramente in silico do FATE-MAP igualaram ou superaram testes líderes de teratogenicidade baseados em células‑tronco e computacionais na classificação de compostos como arriscados ou seguros. De forma notável, vários teratógenos bem conhecidos convergiram para o mesmo agrupamento de falha caracterizado pela perda do mesoderma.
Revelando como as falhas ocorrem, não apenas que ocorrem
A IA de caixa preta sozinha não consegue explicar por que uma colônia falha. Para adicionar mecanismo, a equipe construiu um modelo matemático de como três grandes moléculas sinalizadoras — BMP, Wnt e Nodal — se difundem pela colônia e conduzem as células a diferentes destinos ao longo do tempo. Ao ajustar parâmetros como densidade celular inicial e o quão resistentes as células centrais semelhantes a células‑tronco são à diferenciação (capturado por uma quantidade que chamam de estabilidade de SOX2), eles puderam simular padrões e projetá‑los no mesmo morfoespaço. Isso revelou que a maior parte da variação normal nos padrões podia ser explicada por dois eixos quase independentes: quão compactas estão as células e quão facilmente elas abandonam sua identidade semelhante a células‑tronco. Menor densidade celular permitiu que sinais Wnt e Nodal se espalhassem mais para dentro, alargando a faixa de mesoderma, enquanto maior estabilidade de SOX2 mantinha a região central em um estado mais primitivo apesar dos sinais de diferenciação.
De alertas a futuros medicamentos mais seguros
Finalmente, os pesquisadores usaram o FATE-MAP para sinalizar dois fármacos em estágio clínico sem dados prévios em gravidez humana como potenciais teratógenos. Ambos foram previstos, e então confirmados experimentalmente, como produtores do mesmo modo de falha por perda de mesoderma visto com teratógenos clássicos retinoides, e também causaram defeitos característicos em embriões de zebrafish. Mais amplamente, o trabalho mostra como combinar modelos realistas com células‑tronco, aprendizado de máquina e equações mecanicistas pode transformar o desenvolvimento humano precoce em uma paisagem mapeável. A longo prazo, plataformas como o FATE-MAP poderiam ajudar desenvolvedores de fármacos a triagem de enorme número de compostos quanto a riscos sutis de desenvolvimento antes que eles cheguem aos pacientes, ao mesmo tempo em que iluminam as regras fundamentais que guiam um embrião de uma folha simples de células rumo a um corpo totalmente formado.
Citação: Rufo, J., Qiu, C., Han, D. et al. FATE-MAP predicts teratogenicity and human gastrulation failure modes by integrating deep learning and mechanistic modeling. Nat Commun 17, 3327 (2026). https://doi.org/10.1038/s41467-026-69596-6
Palavras-chave: teratogenicidade, gastrulação, modelos com células-tronco, aprendizado profundo, toxicidade do desenvolvimento