Clear Sky Science · sv
FATE‑MAP förutser teratogenicitet och fel i mänsklig gastrulation genom att integrera djupinlärning och mekanistisk modellering
Varför tidiga embryofel spelar roll
Många graviditeter tar aldrig sig förbi de allra första veckorna, ofta av orsaker som förblir osynliga för både föräldrar och läkare. Ett kritiskt hinder är ett stadium som kallas gastrulation, då en enkel cellboll omorganiseras till de grundläggande lager som kommer att bilda varje organ i kroppen. Om detta steg går fel kan resultatet bli förlust av graviditet eller medfödda missbildningar. Trots det har forskare haft få människospecifika verktyg för att se hur läkemedel och kemikalier kan stjälpa denna sköra process. Denna studie presenterar FATE‑MAP, en ny plattform som kombinerar stamcellsmodeller, avancerad bildtagning och artificiell intelligens för att förutsäga vilka kemikalier som kan skada tidig mänsklig utveckling och för att avslöja hur dessa fel uppstår.
Bygga ett laboratoriumsersättare för det tidiga embryot
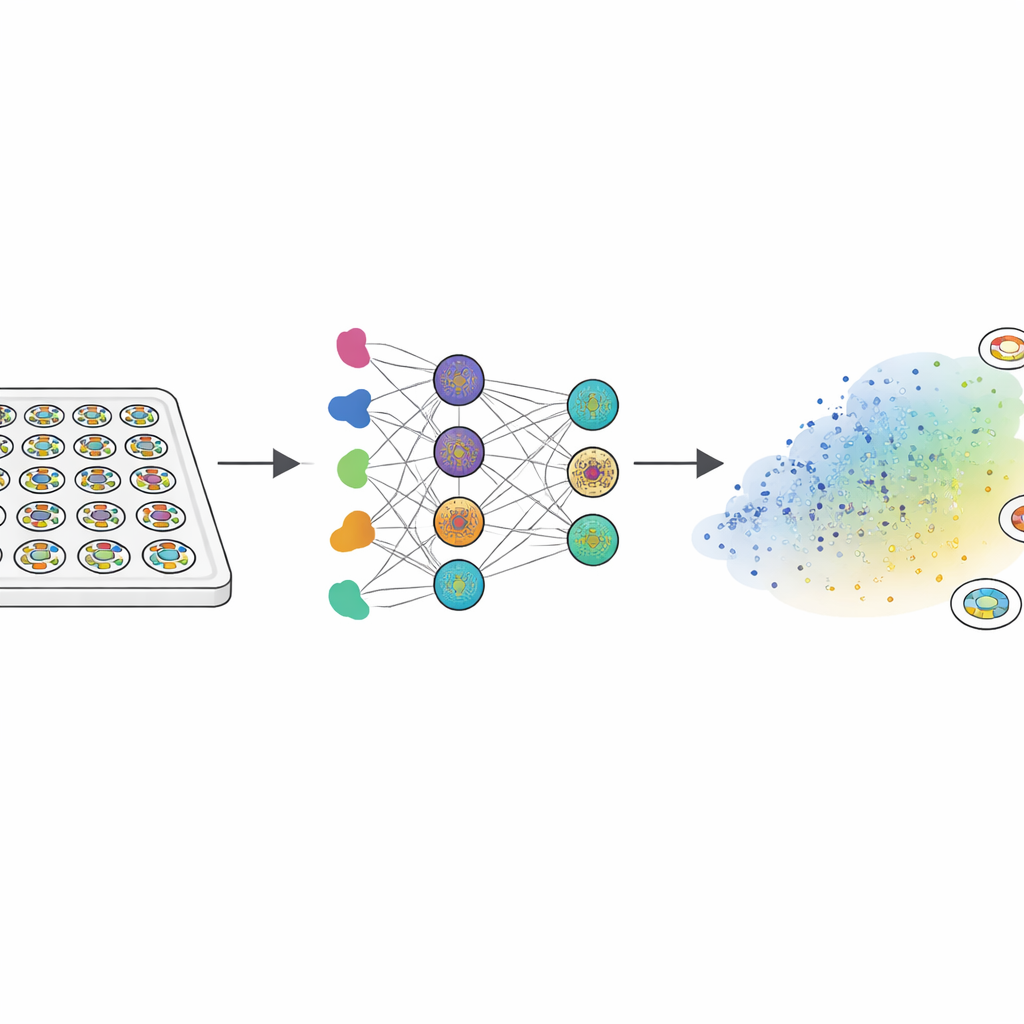
Eftersom riktiga mänskliga embryon inte kan studeras på djupet vände sig forskarna till »gastruloider«—små, platta skivor odlade från humana embryonala stamceller. När dessa skivor exponeras för ett signalprotein kallat BMP4 självorganiserar de sig till tre koncentriska zoner som speglar tidiga embryovävnader: en innerst som förblir stamcellslik, ett mittersta band som blir mesoderm (föregångare till muskel, ben och blod) och en yttre ring som är relaterad till tidig extra‑embryonal vävnad. Teamet behandlade omkring 2000 av dessa kolonier med ett bibliotek på 210 läkemedel som riktar in sig på viktiga tillväxt‑ och signalsystem. Med fluorescerande markörer och anpassad bildanalys förvandlade de varje kolonis mönster till ett 150‑tals fingeravtryck som fångade hur de tre vävnadstyperna var ordnade från kant till centrum.
Kartlägga normala mönster och felmodi
För att förstå denna enorma datamängd använde forskarna en teknik som klustrar liknande mönster nära varandra i ett tvådimensionellt »morfospace«. De flesta kolonier hamnade i ett brett område där alla tre vävnadstyperna uppträdde i rätt radiell ordning och skilde sig mest i hur breda de olika ringarna var. Men flera distinkta »felmodi« framträdde: vissa mönster saknade den centrala stamcellslika regionen, andra förlorade mesodermbandet, och några bröt radial symmetri helt. Eftersom sådana defekter sannolikt skulle förhindra korrekt kroppslayout behandlade teamet dessa kluster som utvecklingsfelmodi snarare än ofarlig variation. Denna karta blev referensen mot vilken både experimentella data och datorbaserade modeller kunde jämföras.
Lära datorer att förutsäga riskfyllda föreningar
Nästa steg var att undersöka om en dator kunde förutsäga var en ny förening skulle landa i detta morfospace enbart utifrån dess kemiska formel. Författarna använde en transformer‑modell—en djupinlärningsmetod ursprungligen utvecklad för språk—för att omvandla varje molekyls SMILES‑sträng till en högdimensionell numerisk beskrivning. Ett neuralt nätverk lärde sig sedan att mappa dessa beskrivningar till de 150‑siffriga koloni‑fingeravtrycken, och ett andra nätverk översatte dessa fingeravtryck till positioner på morfospace‑kartan. För flera dussin läkemedel med kända graviditetsutfall motsvarade FATE‑MAPs rent in silico‑förutsägelser eller överträffade ledande stamcells‑ och datorbaserade tester för teratogenicitet vad gäller att klassificera föreningar som riskfyllda eller säkra. Slående nog konvergerade flera välkända teratogener till samma felkluster som karakteriserades av förlust av mesoderm.
Avslöja hur fel uppstår, inte bara att de gör det
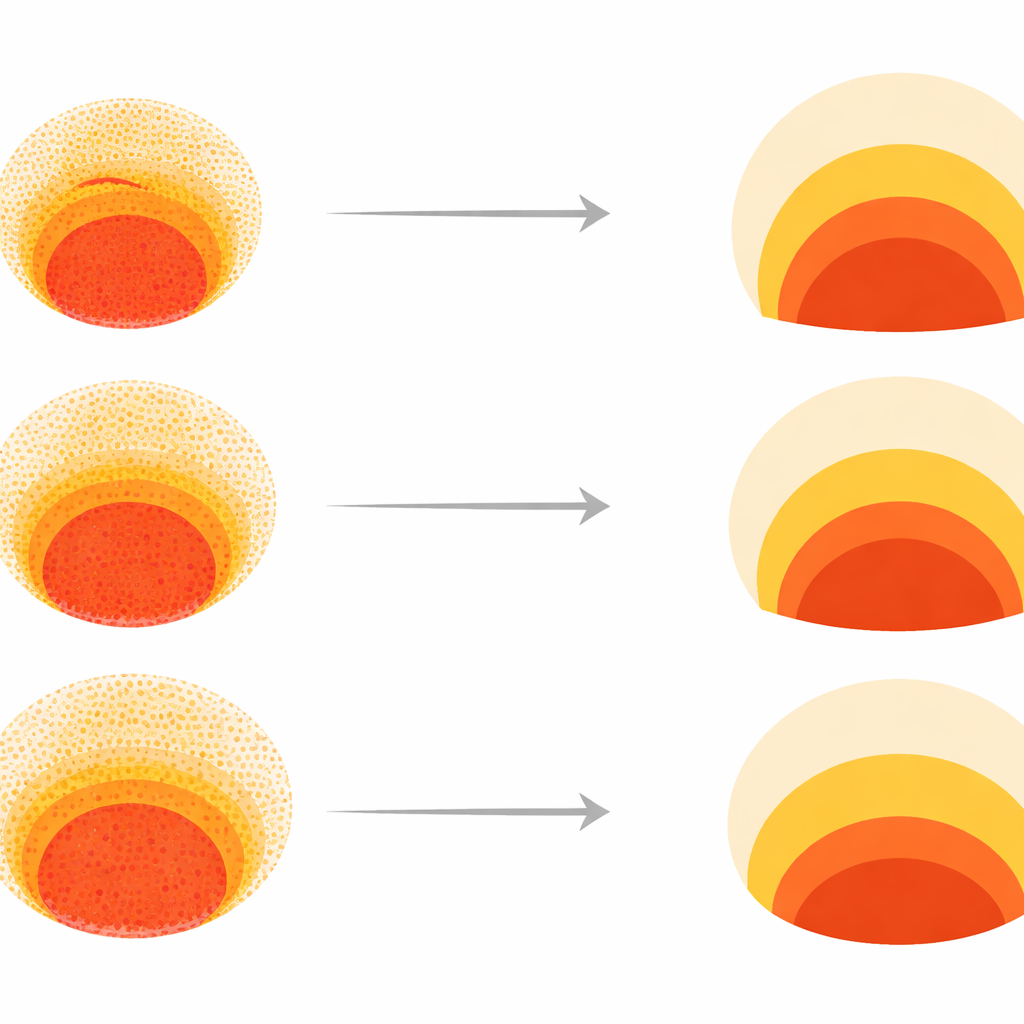
Svart‑låds‑AI ensam kan inte förklara varför en koloni misslyckas. För att lägga till mekanism byggde teamet en matematisk modell av hur tre stora signalsubstanser—BMP, Wnt och Nodal—sprids över kolonin och driver celler mot olika öden över tid. Genom att justera parametrar såsom initial celltäthet och hur motståndskraftiga de centrala stamcellslika cellerna är mot differentiering (fångat av en kvantitet de kallar SOX2‑stabilitet) kunde de simulera mönster och projicera dem in i samma morfospace. Detta visade att den mesta normala variationen i mönster kunde förklaras av två nästan oberoende axlar: hur tätpackade cellerna är och hur lätt de ger upp sin stamcellslika identitet. Lägre celltäthet tillät Wnt‑ och Nodal‑signaler att sprida sig längre inåt och bredda mesodermbandet, medan högre SOX2‑stabilitet höll den centrala regionen i ett mer primitivt tillstånd trots differentieringssignaler.
Från varningar till framtida säkrare läkemedel
Slutligen använde forskarna FATE‑MAP för att flagga två läkemedel i klinisk fas utan tidigare mänskliga graviditetsdata som potentiella teratogener. Båda förutsades, och bekräftades experimentellt, att ge samma mesoderm‑bortfallsfelmod som ses med klassiska retinoida teratogener, och de orsakade också karakteristiska defekter i zebrafiskembryon. Mer allmänt visar arbetet hur kombinationen av realistiska stamcellsmodeller, maskininlärning och mekanistiska ekvationer kan göra tidig mänsklig utveckling till ett kartlagt landskap. På lång sikt skulle plattformar som FATE‑MAP kunna hjälpa läkemedelsutvecklare att screena ett stort antal föreningar för subtila utvecklingsrisker innan de når patienter, samtidigt som de belyser de grundläggande regler som styr hur ett embryo förvandlas från ett enkelt cellskikt till en fullt bildad kropp.
Citering: Rufo, J., Qiu, C., Han, D. et al. FATE-MAP predicts teratogenicity and human gastrulation failure modes by integrating deep learning and mechanistic modeling. Nat Commun 17, 3327 (2026). https://doi.org/10.1038/s41467-026-69596-6
Nyckelord: teratogenicitet, gastrulation, stamcellsmodeller, djupinlärning, utvecklingstoxicitet