Clear Sky Science · tr
FATE-MAP, derin öğrenme ve mekanistik modellemeyi birleştirerek teratojenisiteyi ve insan gastrulasyonunda başarısızlık modlarını öngörür
Erken embriyo hatalarının önemi
Birçok gebelik en erken haftaları aşamaz; bunun sebeplerinin çoğu hem ebeveynler hem de doktorlar için görünmez kalır. Kritik engellerden biri, basit bir hücre küresinin vücutta her organı oluşturacak temel katmanlara yeniden düzenlendiği gastrulasyon evresidir. Bu adım yanlış giderse gebelik kaybı veya doğumsal kusurlar ortaya çıkabilir. Ancak bilim insanlarının ilaçların ve kimyasalların bu hassas süreci nasıl bozabileceğini görmelerine olanak tanıyan insan-a özgü az sayıda aracı vardı. Bu çalışma, kök hücre modelleri, gelişmiş görüntüleme ve yapay zekâyı birleştiren yeni bir platform olan FATE-MAP’i tanıtarak hangi bileşiklerin erken insan gelişimine zarar verebileceğini ve bu başarısızlıkların nasıl ortaya çıktığını öngörmeyi amaçlıyor.
Erken embriyoya laboratuvarda benzer bir yapı oluşturmak
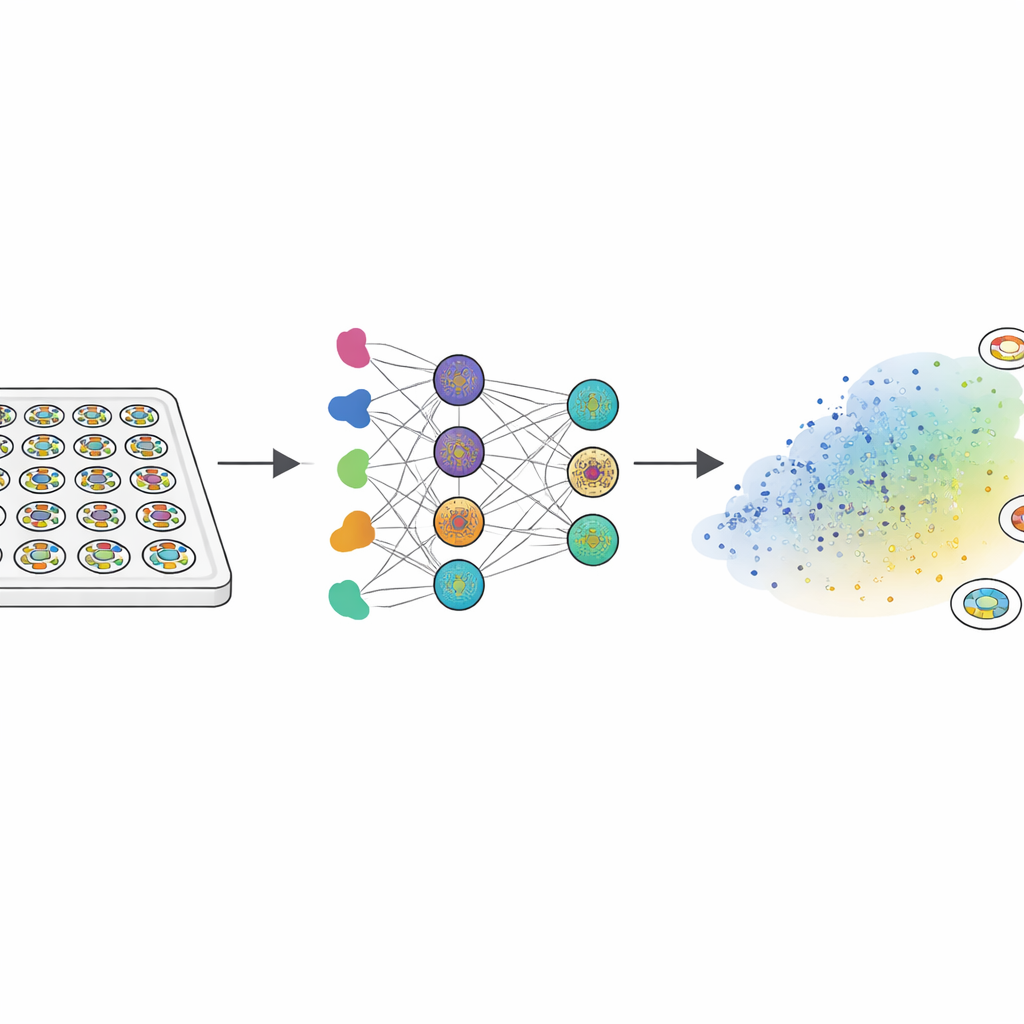
Gerçek insan embriyoları derinlemesine incelenemediğinden, araştırmacılar "gastruloidler"e yöneldi—insan embriyonik kök hücrelerinden yetiştirilen küçük, düz diskler. BMP4 adlı bir sinyal proteinine maruz kaldıklarında bu diskler, içten dışa doğru erken embriyo dokularını yansıtan üç konsantrik bölgeye kendiliğinden organize olur: kök hücre benzeri kalan iç bölge, kas, kemik ve kanın öncülleri olan mezoderm haline gelen orta band ve erken ekstra-embriyonik dokuya ilişkili dış halka. Ekip, bu koloni türlerinden yaklaşık 2000 tanesini büyüme ve sinyal yolaklarını hedefleyen 210 ilaçlık bir kütüphane ile muamele etti. Floresan belirteçler ve özel görüntü analizi kullanarak her koloni desenini, üç doku türünün kenardan merkeze nasıl düzenlendiğini yakalayan 150 sayılık bir parmak izine dönüştürdüler.
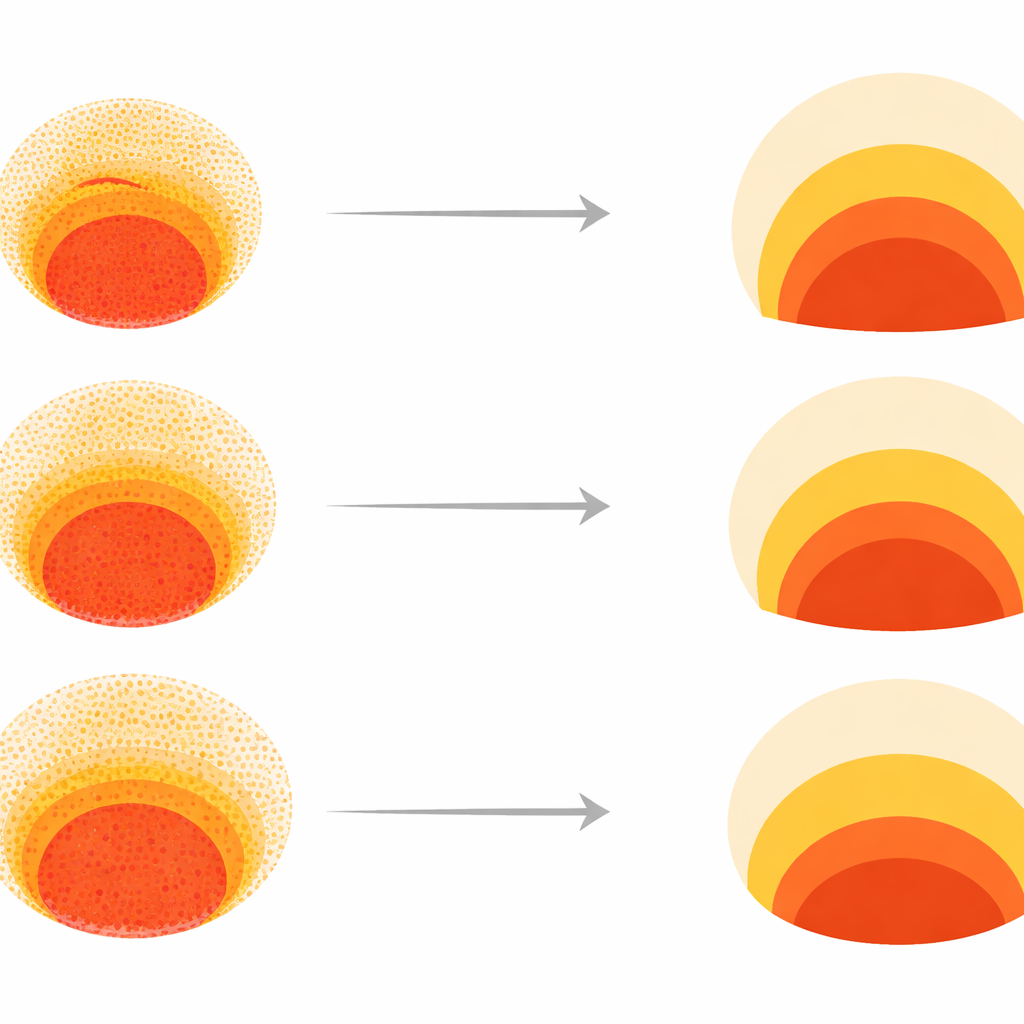
Normal desenleri ve başarısızlık modlarını haritalamak
Bu devasa veri kümesini anlamlandırmak için bilim insanları benzer desenleri iki boyutlu bir "morfosantrum"da birbirine yakın kümelere ayıran bir teknik kullandı. Kolonilerin çoğu, üç doku türünün doğru radyal sırada göründüğü geniş bir bölgeye düştü; aralarındaki farklar esas olarak her halkanın genişliğindeydi. Ancak birkaç belirgin "başarısızlık modu" ortaya çıktı: bazı desenlerde merkezi kök hücre benzeri bölge yoktu, bazılarında mezoderm bandı kayboldu ve bazıları radyal simetriyi tamamen yitirdi. Bu tür kusurlar muhtemelen doğru vücut planı oluşumunu engelleyeceği için ekip bu kümeleri zararsız varyasyonlar yerine gelişimsel başarısızlık modları olarak değerlendirdi. Bu harita, deneysel verilerin ve bilgisayar modellerinin karşılaştırılabileceği referans haline geldi.
Bilgisayarlara riskli bileşikleri tahmin etmeyi öğretmek
Bir sonraki adım, yeni bir bileşiğin yalnızca kimyasal formülünden bu morfosantrumda nereye düşeceğini bir bilgisayarın tahmin edip edemeyeceğini görmekti. Yazarlar, başlangıçta dil için geliştirilen derin öğrenme yaklaşımı olan bir transformer model kullandı ve her molekülün SMILES dizisini yüksek boyutlu sayısal bir betimlemeye dönüştürdü. Ardından bir sinir ağı bu betimlemeleri 150 sayılık koloni parmak izlerine eşlemeyi öğrendi ve ikinci bir ağ bu parmak izlerini morfosantrumdaki konumlara çevirdi. Bilinen gebelik sonuçlarına sahip düzinelerce ilaç için FATE-MAP’in sadece sayısal ortamda yapılan öngörüleri, bileşikleri riskli veya güvenli olarak sınıflandırmada önde gelen kök hücre ve hesaplamalı teratojenisite testlerine eşit ya da daha iyi performans gösterdi. Dikkat çekici şekilde, birkaç iyi bilinen teratojen aynı mezoderm kaybı ile karakterize edilen aynı başarısızlık kümesine toplandı.
Sadece başarısızlık olduğunu söylemek değil, nasıl olduğunu açığa çıkarmak
Siyah kutu yapay zekâ tek başına bir koloninin neden başarısız olduğunu açıklayamaz. Mekanizmayı eklemek için ekip, BMP, Wnt ve Nodal olmak üzere üç ana sinyal molekülünün koloni boyunca nasıl yayıldığını ve zaman içinde hücreleri farklı kaderlere nasıl yönlendirdiğini matematiksel olarak modelledi. Başlangıç hücre yoğunluğu ve merkezi kök hücre benzeri hücrelerin farklılaşmaya karşı ne kadar dirençli olduğu (SOX2 kararlılığı olarak adlandırdıkları bir nicelikle yakalanan) gibi parametreleri ayarlayarak desenleri simüle edebildiler ve bunları aynı morfosantruma projekte ettiler. Bu, desenlerdeki çoğu normal varyasyonun iki neredeyse bağımsız eksenle açıklanabileceğini ortaya koydu: hücrelerin ne kadar sıkışık olduğu ve kök hücre kimliğini ne kadar kolay bıraktıkları. Daha düşük hücre yoğunluğu Wnt ve Nodal sinyallerinin içe doğru daha fazla yayılmasına izin vererek mezoderm bandını genişletirken, daha yüksek SOX2 kararlılığı merkezin farklılaşma uyaranlarına rağmen daha ilkel bir durumda kalmasını sağladı.
Uyarılardan daha güvenli ilaçlara doğru
Son olarak araştırmacılar, daha önce insan gebelik verisi olmayan iki klinik aşama ilacı FATE-MAP ile potansiyel teratojenler olarak işaretledi. Her ikisi de klasik retinoid teratojenlerinde görülen aynı mezoderm-kaybı başarısızlık modunu üretmesi öngörüldü ve ardından deneysel olarak doğrulandı; ayrıca zebrafish embriyolarında karakteristik kusurlara yol açtılar. Daha geniş açıdan bakıldığında, çalışma gerçekçi kök hücre modellerini, makine öğrenmesini ve mekanistik denklemleri bir araya getirmenin erken insan gelişimini haritalanabilir bir manzaraya dönüştürebileceğini gösteriyor. Uzun vadede FATE-MAP benzeri platformlar, ilaç geliştiricilerin hastalara ulaşmadan önce çok sayıda bileşiği saptanamayan gelişimsel risklere karşı taramasına yardımcı olurken, aynı zamanda embriyonun basit bir hücre tabakasından tam oluşmuş bir vücuda dönüşümünü yönlendiren temel kuralları aydınlatabilir.
Atıf: Rufo, J., Qiu, C., Han, D. et al. FATE-MAP predicts teratogenicity and human gastrulation failure modes by integrating deep learning and mechanistic modeling. Nat Commun 17, 3327 (2026). https://doi.org/10.1038/s41467-026-69596-6
Anahtar kelimeler: teratojenisite, gastrulasyon, kök hücre modelleri, derin öğrenme, gelişim toksisitesi