Clear Sky Science · zh
配体依赖的Wnt信号通过微环境中的透明质酸表达促进胃癌转移
这项研究为何重要
胃癌是世界上致死率很高的癌症之一,主要原因在于它常常扩散到远处器官如肝脏。许多药物侧重于杀死癌细胞本身,但本研究表明,包围癌细胞的“土壤”——支持性组织和胶状物质——可能同样关键。通过揭示胃肿瘤如何重塑其环境以在肝脏中存活和繁衍,这项工作为阻断转移(而不仅仅缩小原发肿瘤)指明了新的方向。
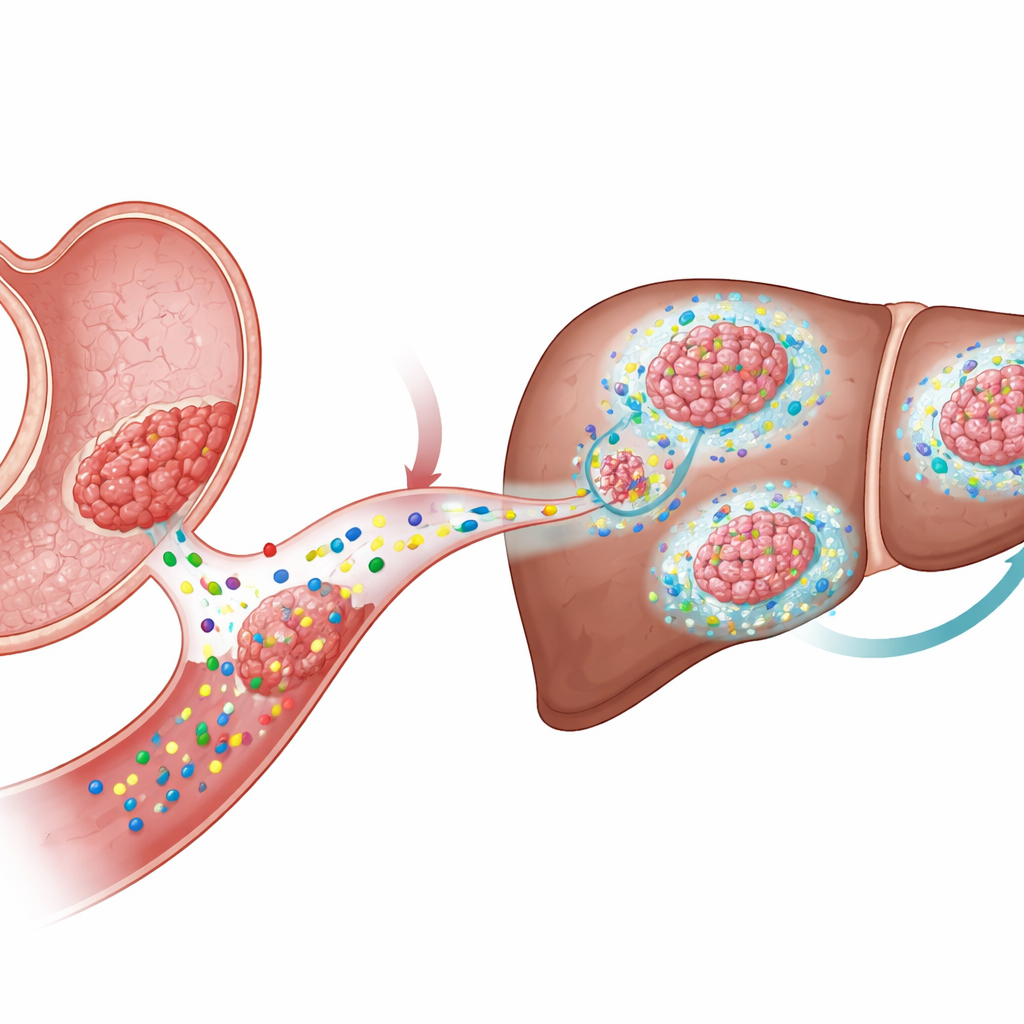
驱动肿瘤生长的信号
研究者关注一类名为Wnt的分子信号家族,这些信号在健康组织中帮助调控干细胞,但常常被癌症劫持。在结肠癌中,Wnt活性通常由癌细胞内部的突变驱动。然而在胃癌中,此类突变较少见,但Wnt活性仍然很高。这提示许多胃肿瘤可能依赖于Wnt配体——由细胞分泌的信号分子——而非永久性的基因开关,从而提出了这些外源信号如何影响肿瘤生长与扩散的问题。
模拟人类疾病的基因工程小鼠
为探讨这一点,团队构建了复杂的小鼠模型,携带三种常见胃癌突变(基因Kras、Tgfbr2和Trp53,合称KTP)的组合。有些小鼠还在胃部特异性产生额外的Wnt1配体(WKTP)。仅有驱动基因突变的小鼠出现胃黏膜增厚和异常细胞类型,但加入Wnt1后这些变化更为明显,产生了明显的上皮异常——从癌前到癌性病变。当科学家从这些小鼠培养迷你肿瘤(类器官)并移植到受体动物体内时,KTP和WKTP细胞都在原位形成了可见肿瘤,表明这组三个驱动突变足以导致局部肿瘤形成。
何时何地发生肝转移
关键差异在研究者观察转移时显现。他们将KTP或WKTP类器官注入脾脏,该途径将细胞直接输送到肝脏。只有产生Wnt1的WKTP细胞在肝脏形成了大且纤维化的转移肿瘤,尽管两种细胞类型最初到达肝脏的数量相似。阻断Wnt配体释放的药物显著减少了肝转移,并使残存肿瘤表现出更分化、增殖性更低的特点。有趣的是,通过破坏门控基因(Apc)来强制KTP细胞维持持续的Wnt活性并不能可靠地产生转移。这表明Wnt在传播疾病中的作用取决于其对周围非癌细胞的影响,而不仅仅是肿瘤细胞内的作用。
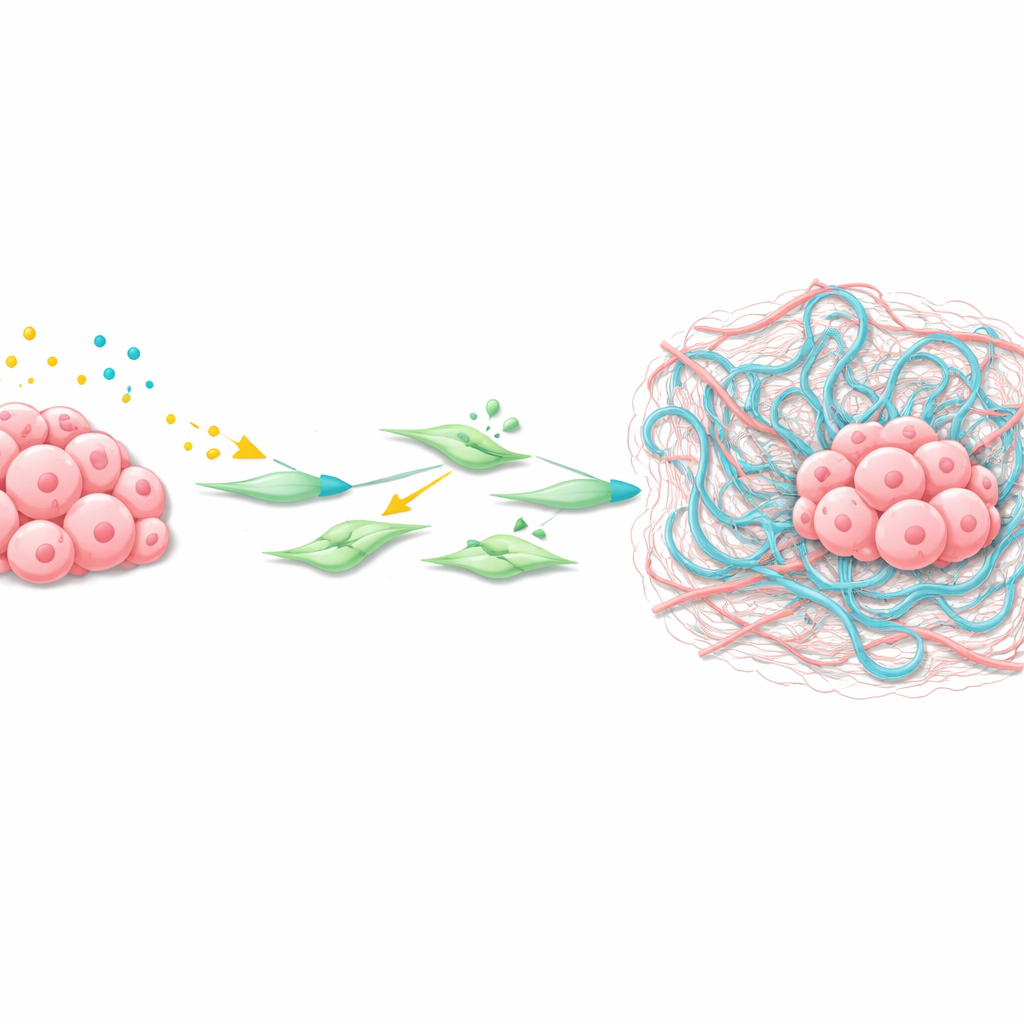
肿瘤如何重塑其邻域
利用空间转录组学——一种在薄组织切片上绘制基因活性分布的技术——团队放大观察了肝转移的微环境。他们发现包绕肿瘤的一簇癌相关成纤维细胞(CAF)显示出强烈的Wnt和TGFβ信号活性。这些CAF高表达Has2,Has2是一种合成透明质酸的酶,透明质酸是一种在组织中以粘稠网状累积的长链糖聚合物。对分离的肝星状细胞和CAF的实验显示,Wnt配体与TGFβ协同作用,开启Wnt靶基因、激活成纤维细胞,并大幅提升Has2水平,导致周围基质强烈收缩和重塑。
有助于癌细胞落脚的粘性网络
研究者进一步证明透明质酸本身是关键帮凶。在小鼠和人类的胃癌肝转移样本中,肿瘤巢周围从非常早期阶段就富含透明质酸。当将WKTP癌细胞工程化为产生透明质酸酶(分解透明质酸的酶)时,它们仍能在注射部位形成肿瘤,但在肝脏产生的转移显著减少。这表明,由激活的成纤维细胞形成的富含透明质酸的粘性基质,构成了一个保护性、滋养性的生态位,帮助播散的胃癌细胞在肝脏中存活、增殖并组织成完整的转移肿瘤。
对未来治疗的意义
综上所述,该研究揭示了一系列事件:胃肿瘤分泌Wnt信号;这些信号与TGFβ协同激活成纤维细胞;成纤维细胞大量合成透明质酸,在肝脏中构建出有利于转移生长的纤维化、凝胶样微环境。对患者而言,这提示了不只针对癌细胞的新策略。阻断Wnt配体产生或接受、干扰TGFβ驱动的成纤维细胞激活,或防止透明质酸积聚的疗法,可能使远处器官对游走的胃癌细胞变得不那么适宜,从而有望将一种快速致命的疾病转变为更可控的状态。
引用: Furutani, Y., Oshima, H., Hong, C.P. et al. Ligand-dependent Wnt signaling promotes gastric cancer metastasis through hyaluronan expression in microenvironment. Nat Commun 17, 2777 (2026). https://doi.org/10.1038/s41467-026-69470-5
关键词: 胃癌, 转移, Wnt信号, 肿瘤微环境, 透明质酸