Clear Sky Science · pt
Sinalização Wnt dependente de ligante promove metástase do câncer gástrico por meio da expressão de ácido hialurônico no microambiente
Por que esta pesquisa importa
O câncer gástrico está entre os cânceres mais letais do mundo, em grande parte porque costuma se espalhar para órgãos distantes, como o fígado. Muitos medicamentos focam em matar as próprias células cancerígenas, mas este estudo mostra que o “solo” ao redor das células — o tecido de suporte e a substância gelatinosa que as envolve — pode ser igualmente importante. Ao revelar como tumores gástricos remodelam seu ambiente para prosperar no fígado, este trabalho aponta para novas maneiras de bloquear a metástase em vez de apenas reduzir o tumor primário.
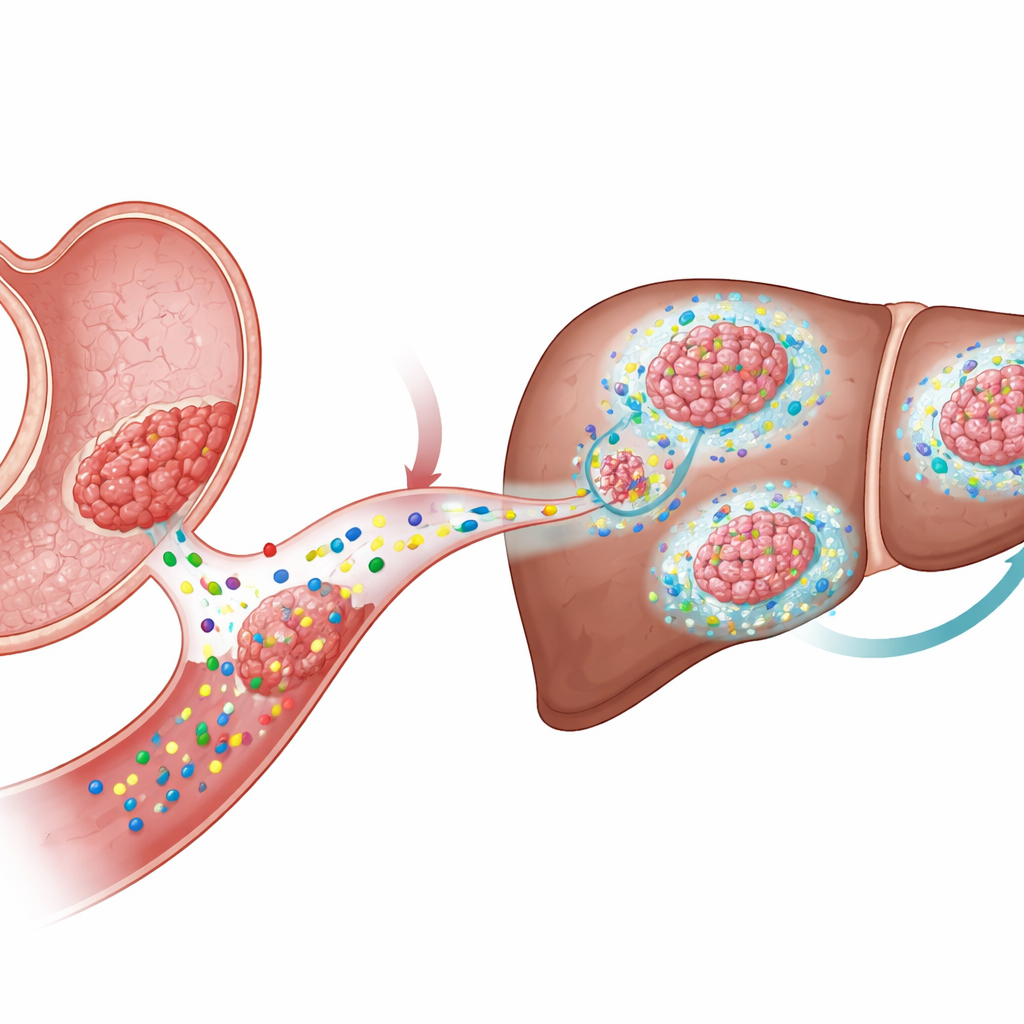
Sinais que impulsionam o crescimento tumoral
Os pesquisadores se concentraram em uma família de sinais moleculares chamada Wnt, que ajuda a regular células-tronco em tecidos saudáveis, mas é frequentemente sequestrada por cânceres. No câncer colorretal, a atividade Wnt costuma ser conduzida por mutações dentro das próprias células tumorais. No câncer gástrico, porém, tais mutações são menos comuns, ainda que a atividade Wnt permaneça elevada. Isso sugeriu que muitos tumores estomacais podem depender de ligantes Wnt — moléculas sinalizadoras secretadas pelas células — ao invés de interruptores genéticos permanentes, levantando a questão de como esses sinais externos influenciam o crescimento e a disseminação tumoral.
Camundongos modificados que imitam a doença humana
Para investigar, a equipe criou modelos murinos sofisticados carregando combinações de três mutações comuns no câncer gástrico (nos genes Kras, Tgfbr2 e Trp53, agrupados como KTP). Alguns camundongos também produziram ligante Wnt1 extra especificamente no estômago (WKTP). Camundongos com apenas as mutações motoras do câncer desenvolveram espessamento da mucosa gástrica e tipos celulares anormais, mas a adição de Wnt1 intensificou essas alterações, produzindo tumores claramente displásicos — do estágio pré-canceroso ao canceroso. Quando os cientistas cultivaram mini-tumores (organoides) desses camundongos e os transplantaram em animais receptores, tanto células KTP quanto WKTP formaram tumores de tamanho considerável no local de origem, mostrando que o conjunto das três mutações era suficiente para a formação tumoral local.
Quando e onde ocorre a disseminação para o fígado
A diferença crucial surgiu ao examinarem a metástase. Eles injetaram organoides KTP ou WKTP no baço, via que direciona as células diretamente ao fígado. Apenas as células produtoras de Wnt1 (WKTP) formaram grandes metástases hepáticas fibróticas, embora ambos os tipos de células tenham chegado inicialmente ao fígado em números semelhantes. Medicamentos que bloqueiam a liberação de ligantes Wnt reduziram fortemente as metástases hepáticas e fizeram com que os tumores remanescentes aparentassem maior diferenciação e menor proliferação. Curiosamente, forçar atividade Wnt constante dentro de células KTP ao desabilitar um gene guardião (Apc) não produziu metástases de forma confiável. Isso indicou que o papel da Wnt na disseminação depende de sua ação em células não cancerosas do entorno, e não apenas dentro das próprias células tumorais.
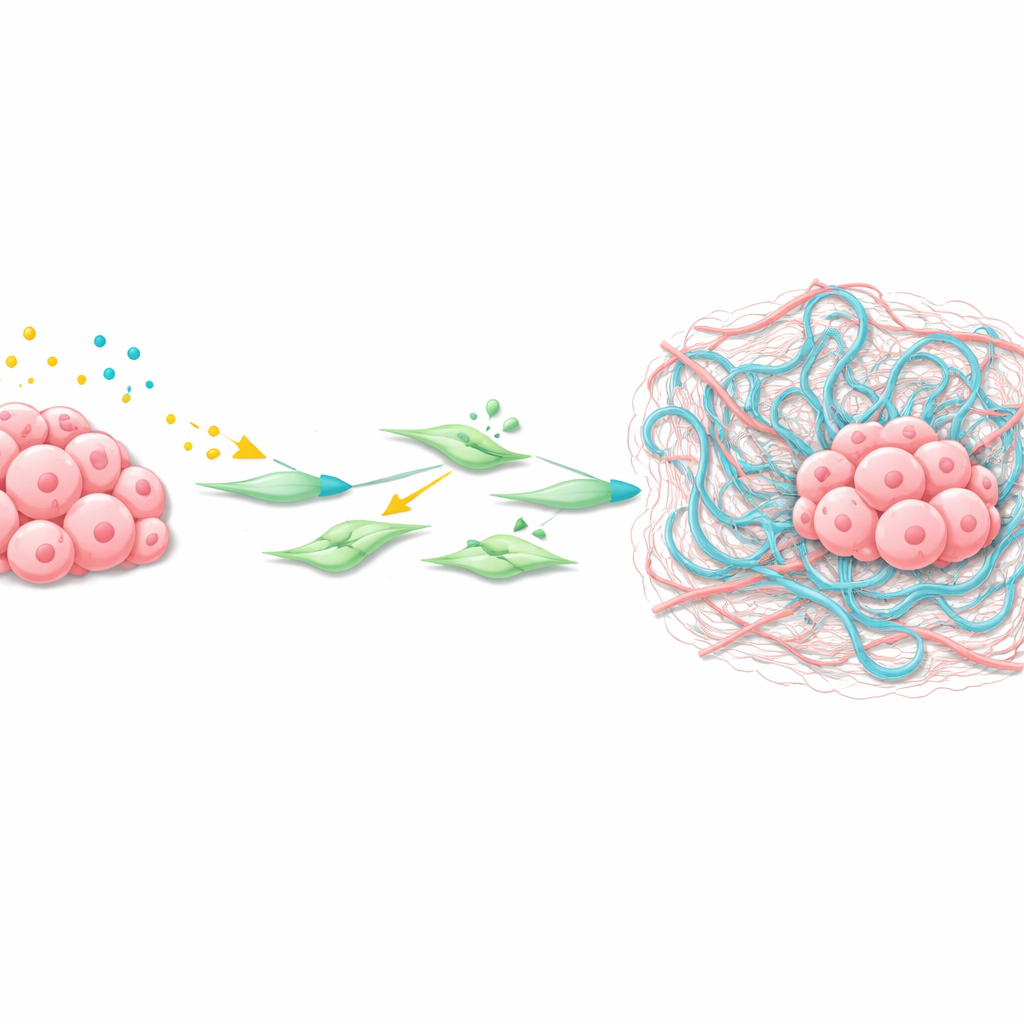
Como o tumor remodela seu bairro
Usando transcriptômica espacial — uma técnica que mapeia a atividade gênica em fatias finas de tecido — a equipe investigou o microambiente das metástases hepáticas. Eles identificaram um aglomerado de fibroblastos associados ao câncer (CAFs) ao redor dos tumores com forte atividade das vias Wnt e TGFβ. Esses CAFs produziram altos níveis de Has2, uma enzima que sintetiza ácido hialurônico, um polímero de açúcar longo que se acumula como uma malha viscosa nos tecidos. Experimentos com células estreladas hepáticas isoladas e CAFs mostraram que ligantes Wnt e TGFβ agem em conjunto para ativar genes-alvo de Wnt, ativar os fibroblastos e aumentar muito os níveis de Has2, provocando forte contração e remodelamento da matriz circundante.
Uma teia pegajosa que ajuda o câncer a se instalar
Os pesquisadores então demonstraram que o ácido hialurônico em si é um cúmplice chave. Tanto em metástases hepáticas de câncer gástrico de camundongo quanto humanas, o ácido hialurônico era abundante ao redor dos ninhos tumorais desde estágios muito iniciais. Quando células WKTP foram geneticamente modificadas para produzir hialuronidases — enzimas que degradam o ácido hialurônico — elas ainda formaram tumores no local de injeção, mas geraram muito menos metástases no fígado. Isso sugere que a matriz pegajosa, rica em ácido hialurônico, produzida por fibroblastos ativados forma um nicho protetor e nutritivo que ajuda células gástricas disseminadas a sobreviver, proliferar e organizar-se em metástases completas.
O que isso significa para tratamentos futuros
Em conjunto, o estudo revela uma sequência de eventos: tumores gástricos secretam sinais Wnt; esses cooperam com TGFβ para ativar fibroblastos; os fibroblastos produzem grandes quantidades de ácido hialurônico, construindo um microambiente fibrótico e em forma de gel no fígado que favorece o crescimento metastático. Para os pacientes, isso aponta para novas estratégias que não atacam apenas as células tumorais. Terapias que bloqueiem a produção ou recepção de ligantes Wnt, interfiram na ativação de fibroblastos mediada por TGFβ ou evitem o acúmulo de ácido hialurônico poderiam tornar órgãos distantes menos hospitaleiros para células de câncer gástrico disseminadas, potencialmente transformando uma doença rapidamente letal em uma condição mais controlável.
Citação: Furutani, Y., Oshima, H., Hong, C.P. et al. Ligand-dependent Wnt signaling promotes gastric cancer metastasis through hyaluronan expression in microenvironment. Nat Commun 17, 2777 (2026). https://doi.org/10.1038/s41467-026-69470-5
Palavras-chave: câncer gástrico, metástase, sinalização Wnt, microambiente tumoral, ácido hialurônico