Clear Sky Science · it
La segnalazione Wnt dipendente da ligando favorisce la metastasi del cancro gastrico attraverso l’espressione di ialuronano nel microambiente
Perché questa ricerca è importante
Il cancro gastrico è uno dei tumori più letali al mondo, in gran parte perché si diffonde spesso a organi distanti come il fegato. Molti farmaci mirano a uccidere direttamente le cellule tumorali, ma questo studio dimostra che anche il “terreno” circostante in cui crescono le cellule — il tessuto di supporto e la sostanza gelatinosa intorno a esse — può essere altrettanto rilevante. Scoprendo come i tumori gastrici rimodellano il loro ambiente per prosperare nel fegato, questo lavoro indica nuove strategie per bloccare le metastasi anziché limitarsi a ridurre il tumore primario.
Segnali che guidano la crescita tumorale
I ricercatori si sono concentrati su una famiglia di segnali molecolari chiamata Wnt, che regola le cellule staminali nei tessuti sani ma viene frequentemente dirottata dai tumori. Nel cancro del colon, l’attività Wnt è solitamente guidata da mutazioni all’interno delle cellule tumorali stesse. Nel cancro gastrico, invece, tali mutazioni sono meno comuni, eppure l’attività Wnt rimane elevata. Ciò ha suggerito che molti tumori gastrici potrebbero dipendere dai ligandi Wnt — molecole segnale secrete dalle cellule — piuttosto che da interruttori genetici permanenti, sollevando la questione di come questi segnali esterni influenzino la crescita e la diffusione del tumore.
Topi ingegnerizzati che imitano la malattia umana
Per indagare, il team ha creato modelli murini sofisticati che portano combinazioni di tre mutazioni comuni nel cancro gastrico (nei geni Kras, Tgfbr2 e Trp53, raggruppate come KTP). Alcuni topi producevano inoltre un eccesso del ligando Wnt1 specificamente nello stomaco (WKTP). I topi con solo le mutazioni oncogeniche sviluppavano un ispessimento della mucosa gastrica e tipi cellulari anomali, ma l’aggiunta di Wnt1 accentuava questi cambiamenti, producendo tumori chiaramente displastici — da precancerosi a cancerosi. Quando gli scienziati hanno coltivato mini-tumori (organoidi) da questi topi e li hanno trapiantati in animali riceventi, sia le cellule KTP sia WKTP hanno formato tumori di dimensioni rilevanti nel sito originario, mostrando che il set di tre mutazioni era sufficiente per la formazione tumorale locale.
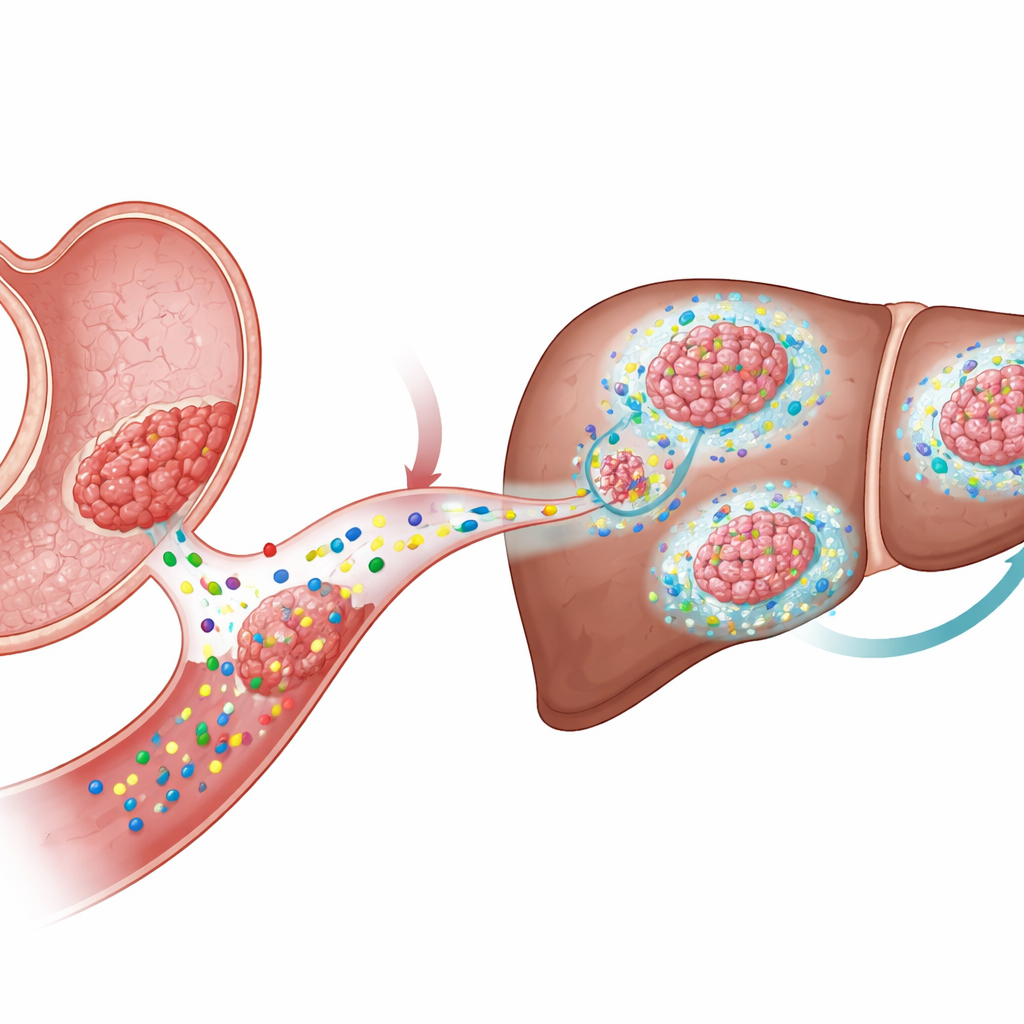
Quando e dove avviene la diffusione al fegato
La differenza chiave è emersa nell’analisi delle metastasi. I ricercatori hanno iniettato organoidi KTP o WKTP nella milza, una via che invia le cellule direttamente al fegato. Solo le cellule WKTP produttrici di Wnt1 hanno formato grandi metastasi epatiche fibrotiche, nonostante entrambi i tipi di cellule fossero giunti inizialmente al fegato in numeri simili. Farmaci che bloccano il rilascio dei ligandi Wnt hanno ridotto nettamente le metastasi epatiche e hanno fatto apparire i tumori residui più differenziati e meno proliferativi. È interessante che forzare un’attività Wnt costitutiva all’interno delle cellule KTP disabilitando un gene regolatore (Apc) non abbia prodotto in modo affidabile metastasi. Ciò indica che il ruolo di Wnt nella diffusione della malattia dipende dalla sua azione nelle cellule non tumorali circostanti, non solo all’interno delle cellule tumorali stesse.
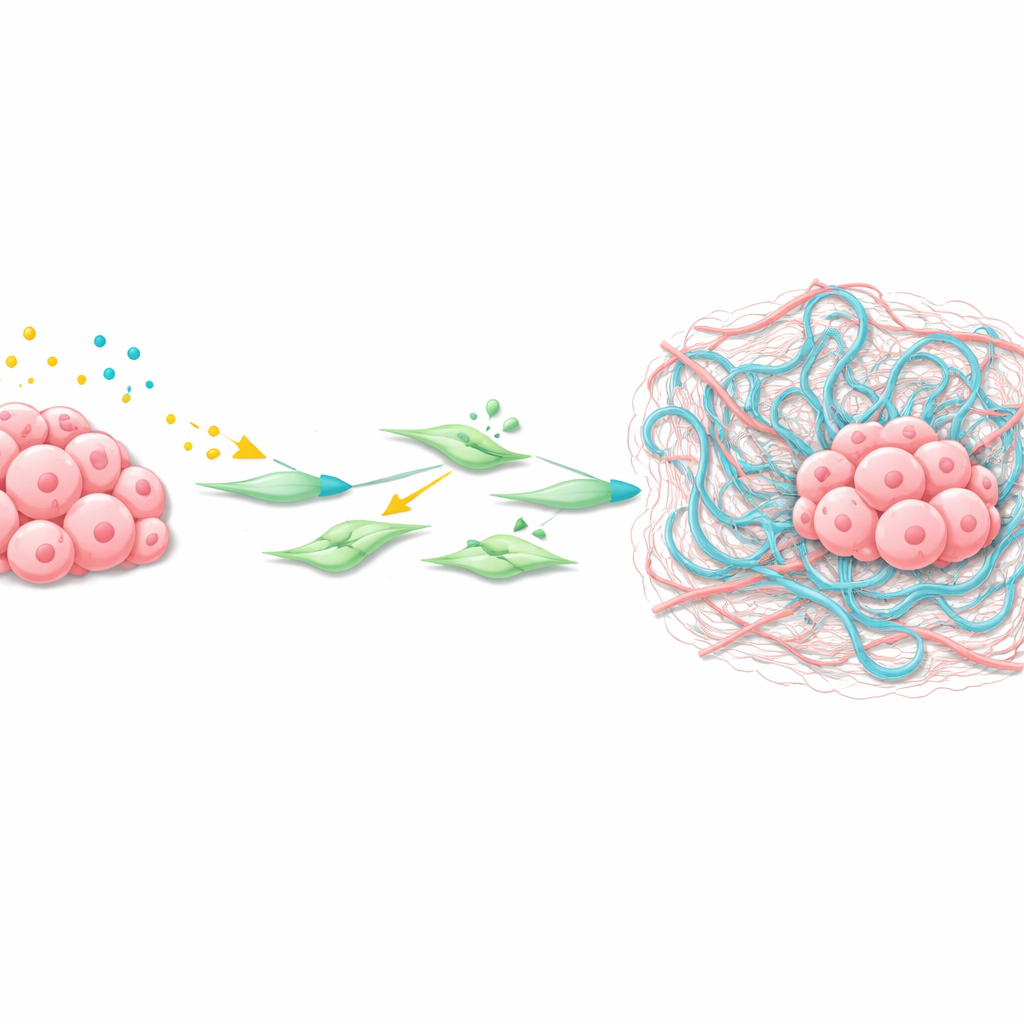
Come il tumore rimodella il suo quartiere
Usando la trascrittomica spaziale — una tecnica che mappa l’attività genica attraverso sezioni tissutali — il team ha analizzato nel dettaglio il microambiente delle metastasi epatiche. Hanno identificato un gruppo di fibroblasti associati al tumore (CAF) che circondavano i tumori con una forte attività dei segnali Wnt e TGFβ. Questi CAF esprimevano elevati livelli di Has2, un enzima che sintetizza l’ialuronano, un lungo polimero zuccherino che si accumula come una rete viscosa nei tessuti. Esperimenti con cellule stellate epatiche isolate e CAF hanno mostrato che i ligandi Wnt e il TGFβ agiscono insieme per attivare i geni bersaglio Wnt, attivare i fibroblasti e aumentare notevolmente i livelli di Has2, provocando una marcata contrazione e rimodellamento della matrice circostante.
Una rete appiccicosa che aiuta il tumore a stabilirsi
I ricercatori hanno quindi dimostrato che l’ialuronano stesso è un complice chiave. Sia nelle metastasi epatiche di topo sia in quelle umane del cancro gastrico, l’ialuronano risultava abbondante intorno agli aggregati tumorali fin dalle prime fasi. Quando le cellule cancerose WKTP sono state ingegnerizzate per produrre ialuronidasi — enzimi che degradano l’ialuronano — hanno comunque formato tumori nel sito di iniezione ma hanno dato origine a molte meno metastasi epatiche. Questo suggerisce che la matrice viscosa ricca di ialuronano creata dai fibroblasti attivati costituisce un nicchia protettiva e nutritiva che aiuta le cellule tumorali gastriche disseminate a sopravvivere, proliferare e organizzarsi in metastasi complete.
Cosa significa per i trattamenti futuri
Nel complesso, lo studio rivela una catena di eventi: i tumori gastrici secernono segnali Wnt; questi cooperano con il TGFβ per attivare i fibroblasti; i fibroblasti producono grandi quantità di ialuronano, costruendo un microambiente fibrotico e gelatinoso nel fegato che favorisce la crescita metastatica. Per i pazienti, ciò indica nuove strategie che non mirano solo alle cellule tumorali. Terapie che bloccano la produzione o la ricezione dei ligandi Wnt, interferiscono con l’attivazione dei fibroblasti guidata da TGFβ o impediscono l’accumulo di ialuronano potrebbero rendere gli organi distanti meno ospitali per le cellule tumorali gastriche in dispersione, trasformando potenzialmente una malattia rapidamente letale in una più controllabile.
Citazione: Furutani, Y., Oshima, H., Hong, C.P. et al. Ligand-dependent Wnt signaling promotes gastric cancer metastasis through hyaluronan expression in microenvironment. Nat Commun 17, 2777 (2026). https://doi.org/10.1038/s41467-026-69470-5
Parole chiave: cancro gastrico, metastasi, segnalazione Wnt, microambiente tumorale, ialuronano