Clear Sky Science · de
Ligandabhängige Wnt-Signalübertragung fördert die Metastasierung von Magenkrebs durch Hyaluronan-Expression im Mikroenvironment
Warum diese Forschung wichtig ist
Magenkrebs gehört zu den weltweit tödlichsten Krebserkrankungen, vor allem weil er häufig in entfernte Organe wie die Leber streut. Viele Medikamente zielen darauf ab, Krebszellen direkt zu töten, doch diese Studie zeigt, dass der umgebende „Boden“, in dem Krebszellen wachsen — also das stützende Gewebe und die gelartige Matrix — genauso entscheidend sein kann. Indem sie aufdeckt, wie Magen-Tumoren ihre Umgebung so umgestalten, dass sie in der Leber gedeihen, weist diese Arbeit auf neue Wege hin, Metastasen zu verhindern statt nur Primärtumoren zu verkleinern.
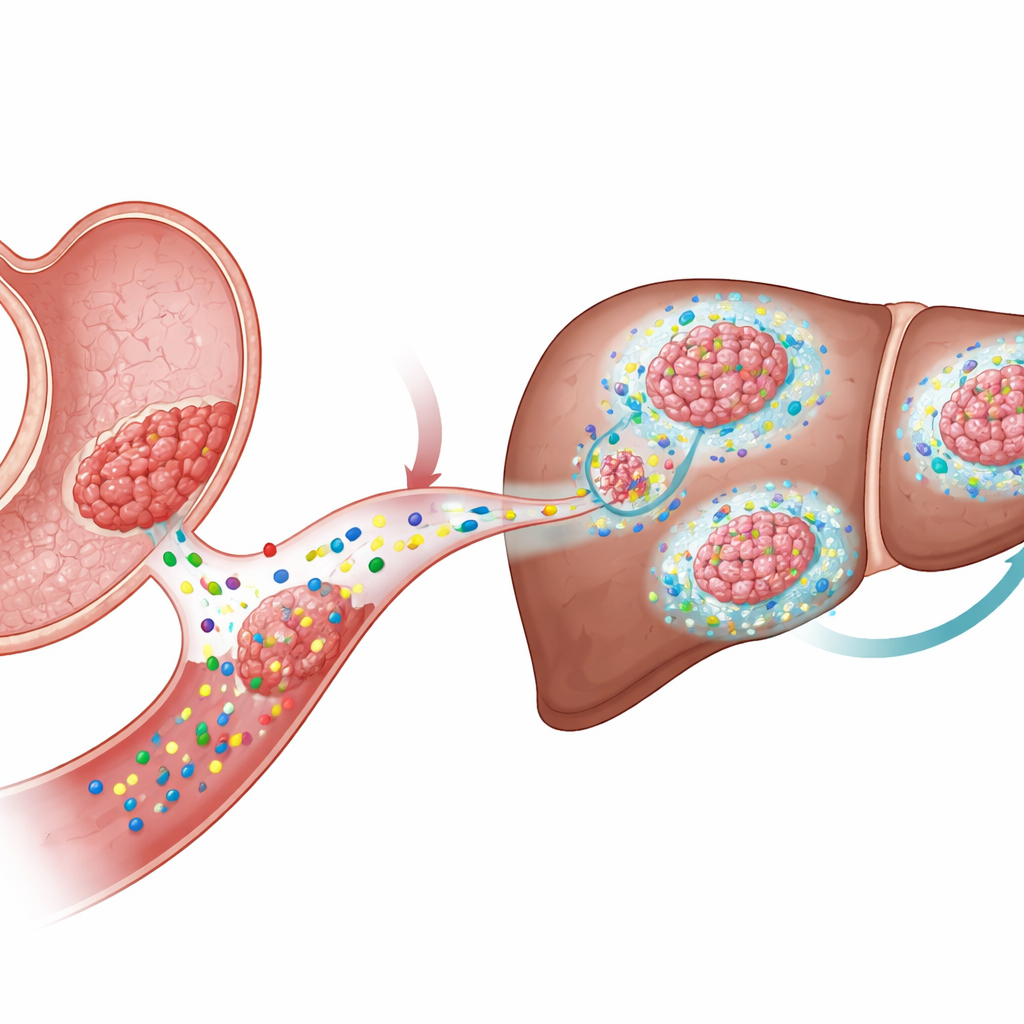
Signale, die Tumorwachstum antreiben
Die Forschenden konzentrierten sich auf eine Familie molekularer Signale namens Wnt, die in gesunden Geweben Stammzellen regulieren, in Krebs jedoch häufig missbraucht werden. Beim Darmkrebs wird die Wnt-Aktivität meist durch Mutationen innerhalb der Krebszellen selbst getrieben. Beim Magenkrebs sind solche Mutationen seltener, trotzdem ist die Wnt-Aktivität hoch. Das deutete darauf hin, dass viele Magen-Tumoren eher von Wnt-Liganden — von Zellen ausgeschütteten Signalstoffen — abhängig sein könnten als von dauerhaften genetischen Schaltern. Es stellte sich die Frage, wie diese externen Signale das Tumorwachstum und die Ausbreitung beeinflussen.
Genetisch veränderte Mäuse, die die menschliche Krankheit nachahmen
Um das zu untersuchen, erzeugte das Team ausgefeilte Mausmodelle mit Kombinationen aus drei häufigen Magenkrebs-Mutationen (in den Genen Kras, Tgfbr2 und Trp53, zusammengefasst als KTP). Einige Mäuse produzierten zusätzlich gezielt mehr Wnt1-Ligand im Magen (WKTP). Mäuse mit nur den Krebs-Treiber-Mutationen entwickelten verdickte Magenschleimhäute und abnorme Zelltypen, doch durch Hinzufügen von Wnt1 wurden diese Veränderungen stärker und führten zu deutlich dysplastischen — also von präkanzerös bis krebsartig reichen — Tumoren. Als die Wissenschaftler Organoide (Mini-Tumoren) aus diesen Mäusen züchteten und in Empfängertiere transplantierten, bildeten sowohl KTP- als auch WKTP-Zellen am Entstehungsort große Tumoren, was zeigt, dass die Drei-Treiber-Mutation ausreichend für lokale Tumorbildung ist.
Wann und wo die Ausbreitung in die Leber auftritt
Der entscheidende Unterschied zeigte sich bei der Metastasierung. Die Forschenden injizierten KTP- oder WKTP-Organoide in die Milz, einen Weg, der Zellen direkt in die Leber leitet. Nur die Wnt1-produzierenden WKTP-Zellen bildeten große, fibröse metastatische Tumoren in der Leber, obwohl beide Zelltypen anfangs in ähnlicher Zahl dort ankamen. Medikamente, die die Freisetzung von Wnt-Liganden blockieren, verringerten die Lebermetastasen stark und bewirkten, dass die verbleibenden Tumoren differenzierter und weniger proliferativ erschienen. Interessanterweise führte das Erzwingen konstanter Wnt-Aktivität innerhalb von KTP-Zellen durch Deaktivierung eines Kontrollgens (Apc) nicht zuverlässig zu Metastasen. Das deutet darauf hin, dass die Rolle von Wnt bei der Ausbreitung davon abhängt, wie es in den umliegenden, nicht-krebsartigen Zellen wirkt, nicht nur innerhalb der Tumorzellen selbst.
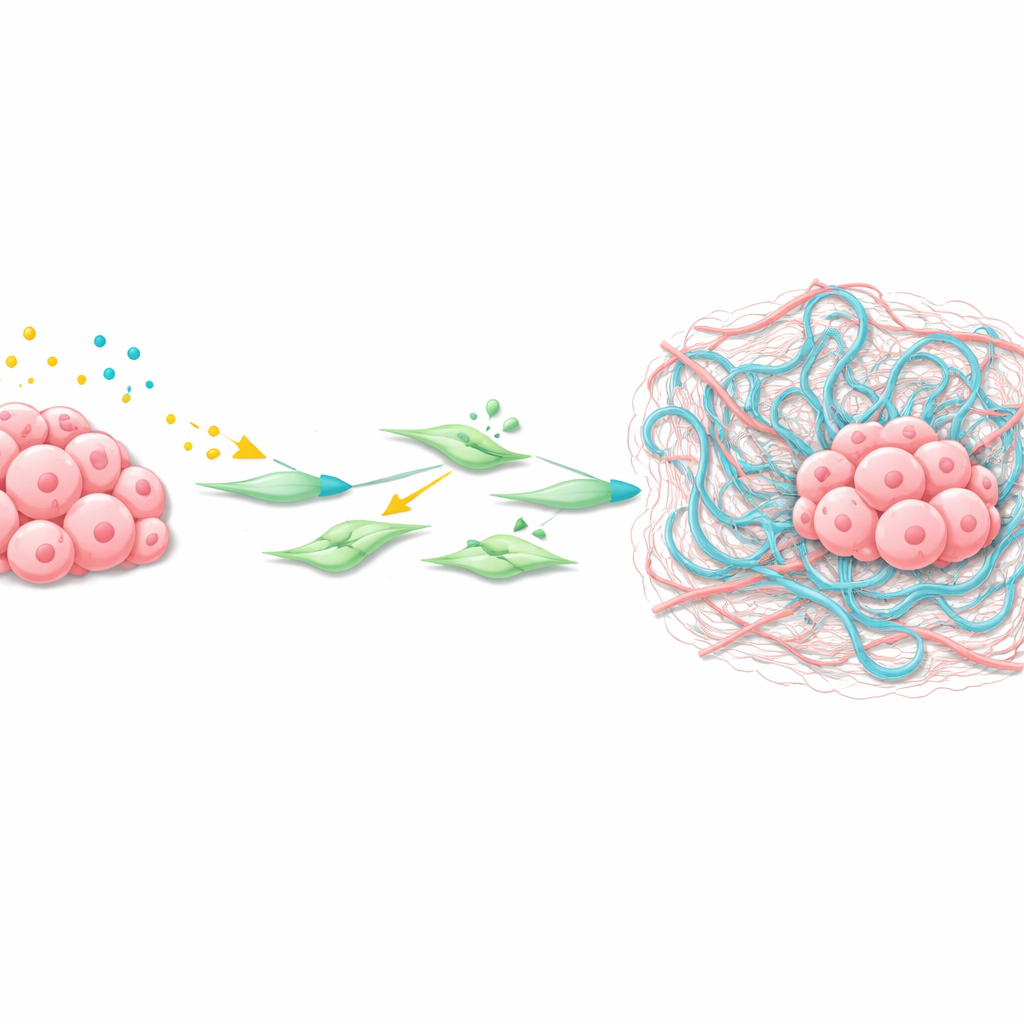
Wie der Tumor seine Nachbarschaft umgestaltet
Mithilfe räumlicher Transkriptomik — einer Technik, die Genaktivität über dünne Gewebeschnitte kartiert — untersuchte das Team das Mikroenvironment der Lebermetastasen. Sie fanden einen Cluster von krebsassoziierten Fibroblasten (CAFs) um die Tumoren mit stark aktiver Wnt- und TGFβ-Signalgebung. Diese CAFs produzierten hohe Mengen von Has2, einem Enzym, das Hyaluronan synthetisiert, ein langes Zuckerpolymer, das sich als viskoses Netz im Gewebe ansammelt. Experimente mit isolierten Lebersternzellen und CAFs zeigten, dass Wnt-Liganden und TGFβ zusammenwirken, um Wnt-Zielgene einzuschalten, die Fibroblasten zu aktivieren und Has2 stark zu erhöhen, was zu ausgeprägter Kontraktion und Umgestaltung der umliegenden Matrix führt.
Ein klebriges Netz, das dem Krebs beim Ansiedeln hilft
Die Forschenden zeigten dann, dass Hyaluronan selbst ein entscheidender Komplize ist. Sowohl in Maus- als auch in menschlichen Magenkrebs-Lebermetastasen war Hyaluronan bereits in sehr frühen Stadien um Tumornester herum reichlich vorhanden. Als WKTP-Krebszellen so verändert wurden, dass sie Hyaluronidasen — Enzyme, die Hyaluronan abbauen — produzierten, bildeten sie zwar weiterhin Tumoren an der Injektionsstelle, erzeugten in der Leber jedoch deutlich weniger Metastasen. Das legt nahe, dass die klebrige, hyaluronanreiche Matrix, die von aktivierten Fibroblasten geschaffen wird, eine schützende, nährende Nische bildet, die disseminierten Magenkrebszellen hilft, zu überleben, zu proliferieren und sich zu vollständigen metastatischen Tumoren zu organisieren.
Was das für zukünftige Behandlungen bedeutet
Insgesamt zeigt die Studie eine Abfolge von Ereignissen: Magen-Tumoren sekretieren Wnt-Signale; diese kooperieren mit TGFβ, um Fibroblasten zu aktivieren; die Fibroblasten produzieren große Mengen Hyaluronan und bauen so in der Leber ein fibröses, gelartiges Mikroenvironment auf, das das metastatische Wachstum begünstigt. Für Patientinnen und Patienten deutet das auf neue Strategien hin, die nicht nur die Krebszellen selbst angreifen. Therapien, die die Produktion oder Wahrnehmung von Wnt-Liganden blockieren, die TGFβ-getriebene Aktivierung von Fibroblasten stören oder die Ansammlung von Hyaluronan verhindern, könnten entfernte Organe für wandernde Magenkrebszellen weniger gastlich machen und so eine rasch tödliche Erkrankung in eine besser kontrollierbare verwandeln.
Zitation: Furutani, Y., Oshima, H., Hong, C.P. et al. Ligand-dependent Wnt signaling promotes gastric cancer metastasis through hyaluronan expression in microenvironment. Nat Commun 17, 2777 (2026). https://doi.org/10.1038/s41467-026-69470-5
Schlüsselwörter: Magenkrebs, Metastasen, Wnt-Signalgebung, Tumormikroumgebung, Hyaluronan