Clear Sky Science · ru
Зависимая от лигандов Wnt‑сигнализация способствует метастазированию рака желудка через экспрессию гиалуронана в микроокружении
Почему это исследование важно
Рак желудка — один из самых смертельных видов рака в мире, во многом потому, что он часто даёт метастазы в отдалённые органы, такие как печень. Многие лекарства направлены на уничтожение самих раковых клеток, но в этом исследовании показано, что окружающая «почва», в которой растут опухолевые клетки — поддерживающая ткань и гелеобразное межклеточное вещество — может быть не менее важной. Раскрыв, как желудочные опухоли перестраивают своё окружение, чтобы успешно оседать в печени, работа указывает на новые подходы, направленные на блокирование метастазирования, а не только на уменьшение первичных опухолей.
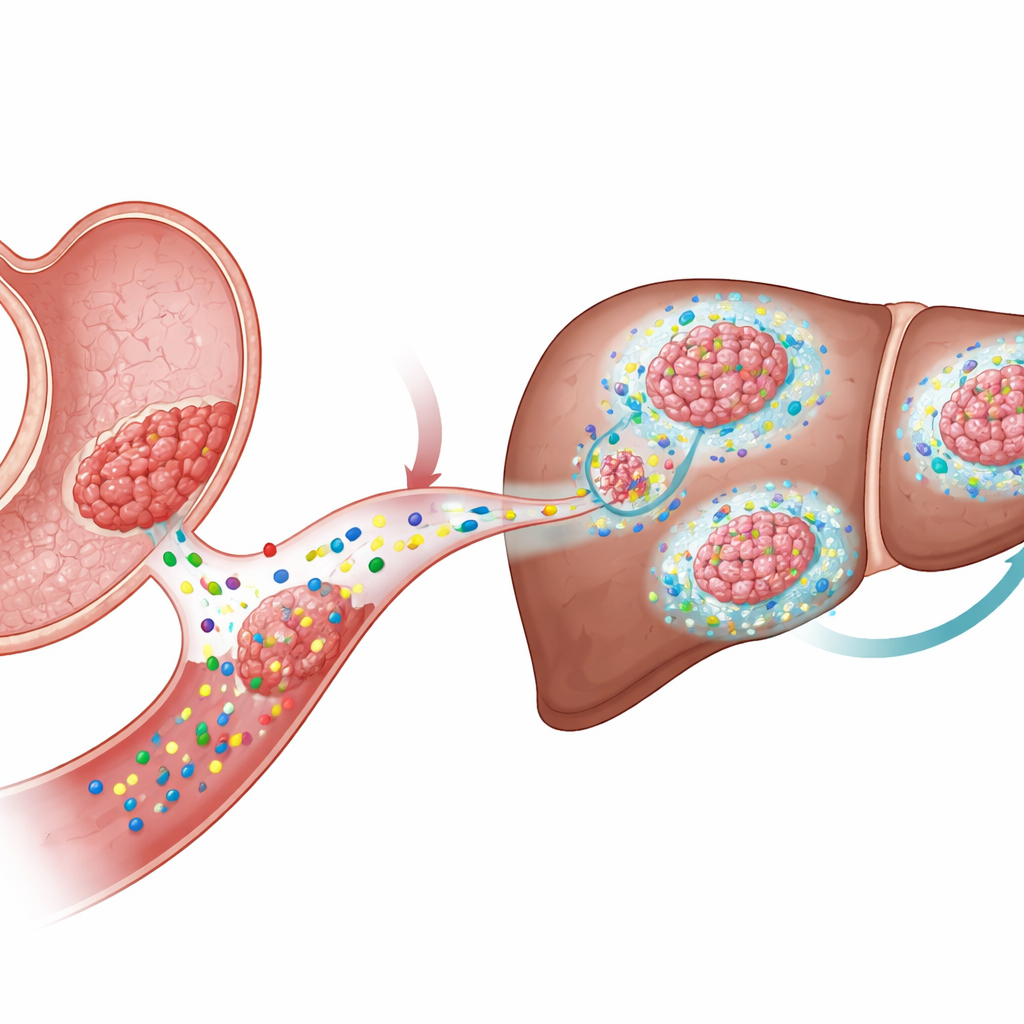
Сигналы, стимулирующие рост опухоли
Исследователи сосредоточились на семействе молекулярных сигналов Wnt, которые регулируют стволовые клетки в здоровых тканях, но часто захватываются опухолями. В колоректальном раке активность Wnt обычно обусловлена мутациями внутри самих раковых клеток. В раке желудка такие мутации встречаются реже, но активность Wnt остаётся высокой. Это наводило на мысль, что многие опухоли желудка могут зависеть от Wnt‑лигандов — сигнальных молекул, секретируемых клетками — а не от постоянных генетических переключателей, что ставит вопрос о том, как внешние сигналы влияют на рост и распространение опухоли.
Генноинженерные мыши, имитирующие человеческое заболевание
Для изучения этого явления команда создала продвинутые мышиные модели с комбинациями трёх распространённых мутаций при раке желудка (в генах Kras, Tgfbr2 и Trp53, объединённых как KTP). У части мышей дополнительно в желудке экспрессировался лишний лиганд Wnt1 (WKTP). Мыши только с драйверными мутациями развивали утолщение слизистой желудка и атипию клеток, но добавление Wnt1 усиливало эти изменения и приводило к явным диспластическим — предопухолевым и опухолевым — изменениям. Когда учёные вырастили мини‑опухоли (органоиды) из этих мышей и пересадили их реципиентам, как KTP, так и WKTP клетки формировали крупные опухоли в исходном месте, что показывает: набор из трёх драйверных мутаций достаточен для локального формирования опухоли.
Когда и где возникает распространение в печень
Ключевое различие проявилось при изучении метастазирования. Исследователи вводили органоиды KTP или WKTP в селезёнку — путь, по которому клетки напрямую попадают в печень. Только WKTP‑клетки, продуцирующие Wnt1, образовывали крупные фиброзные метастатические опухоли в печени, хотя оба типа клеток первоначально попадали туда в сходных количествах. Препараты, блокирующие выделение Wnt‑лигандов, резко сокращали число метастаз в печени и делали оставшиеся опухоли более дифференцированными и менее пролиферирующими. Интересно, что принудительное постоянное включение Wnt внутри KTP‑клеток путём отключения контрольного гена (Apc) не вызывало надёжного образования метастаз. Это указывает на то, что роль Wnt в распространении заболевания зависит от его действия в окружающих нераковых клетках, а не только внутри самих опухолевых клеток.
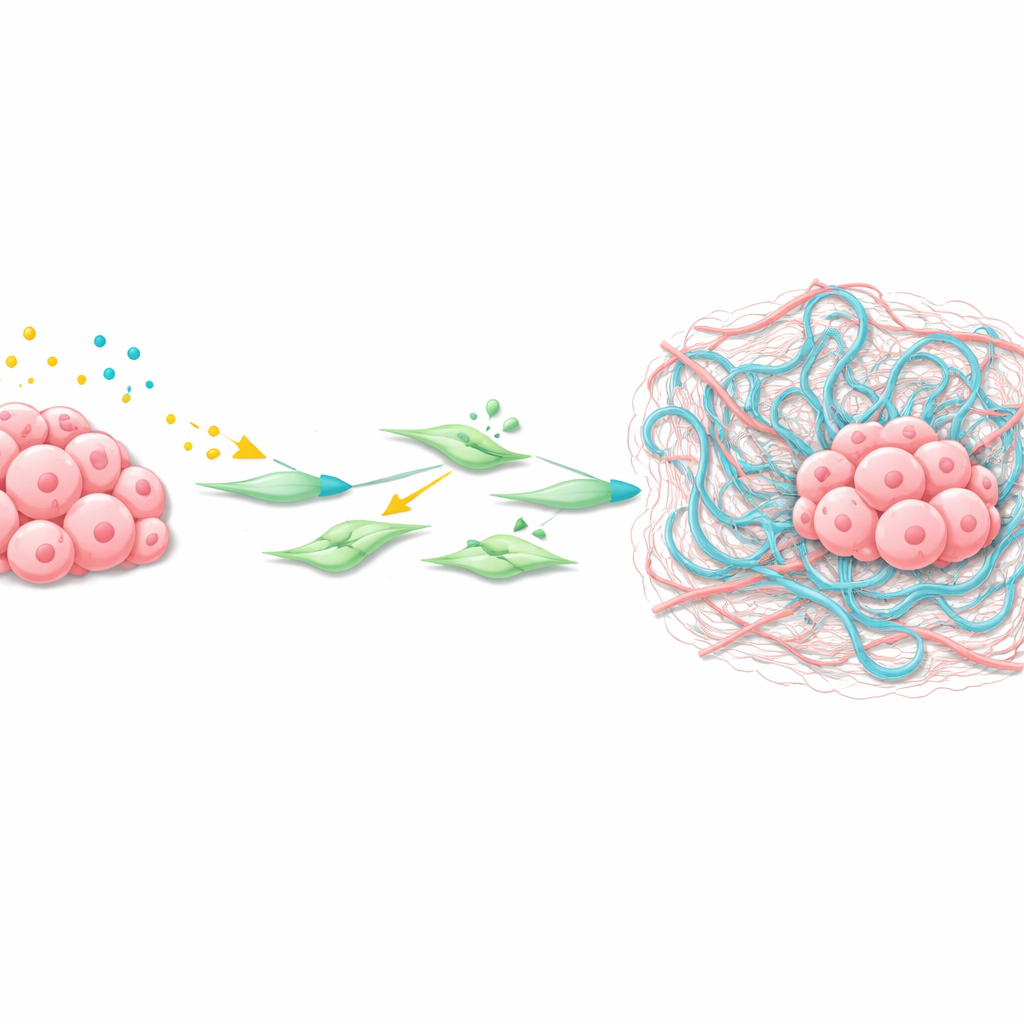
Как опухоль перестраивает своё окружение
С помощью пространственной транскриптомики — метода, картирующего активность генов в тонких срезах ткани — команда подробно изучила микроокружение печёночных метастаз. Они обнаружили скопление ассоциированных с раком фибробластов (CAF), окружающих опухоли, с выраженной активностью Wnt и сигнального пути TGFβ. Эти CAF экспрессировали высокий уровень Has2 — фермента, синтезирующего гиалуронан, длинный полисахарид, накапливающийся в тканях в виде вязкой сетки. Эксперименты с изолированными печёночными звездчатыми клетками и CAF показали, что Wnt‑лиганд и TGFβ совместно включают Wnt‑таргетные гены, активируют фибробласты и значительно повышают уровень Has2, приводя к сильному сокращению и ремоделированию внеклеточного матрикса.
Липкая сеть, помогающая раку укорениться
Далее исследователи показали, что сам гиалуронан является ключевым соучастником. В метастазах рака желудка в печени у мышей и у людей гиалуронан был обилен вокруг опухолевых гнёзд уже на ранних стадиях. Когда WKTP‑клетки были модифицированы так, чтобы продуцировать гиалуронидазы — ферменты, разрушающие гиалуронан — они по‑прежнему формировали опухоли в месте инъекции, но давали значительно меньше метастаз в печени. Это свидетельствует о том, что липкая матрица, богатая гиалуронаном и созданная активированными фибробластами, формирует защитную, питательную нишу, которая помогает диссеминированным клеткам рака желудка выживать, пролиферировать и организовываться в полноценные метастатические опухоли.
Что это значит для будущих терапий
В совокупности исследование выявляет цепочку событий: желудочные опухоли секретируют Wnt‑сигналы; эти сигналы в сотрудничестве с TGFβ активируют фибробласты; фибробласты синтезируют большие количества гиалуронана, создавая фиброзное гелеобразное микроокружение в печени, благоприятное для роста метастаз. Для пациентов это указывает на новые стратегии, не ограничивающиеся прямой атакой на раковые клетки. Терапии, блокирующие продукцию или восприятие Wnt‑лигандов, вмешивающиеся в TGFβ‑опосредованную активацию фибробластов или предотвращающие накопление гиалуронана, могут сделать отдалённые органы менее пригодными для оседания клеток рака желудка, потенциально превращая быстро фатальное заболевание в более контролируемое.
Цитирование: Furutani, Y., Oshima, H., Hong, C.P. et al. Ligand-dependent Wnt signaling promotes gastric cancer metastasis through hyaluronan expression in microenvironment. Nat Commun 17, 2777 (2026). https://doi.org/10.1038/s41467-026-69470-5
Ключевые слова: рак желудка, метастазирование, Wnt‑сигнализация, опухолевое микроокружение, гиалуронан