Clear Sky Science · nl
Ligand-afhankelijke Wnt‑signalering bevordert uitzaaiing van maagkanker via hyaluronaan-expressie in de micro‑omgeving
Waarom dit onderzoek ertoe doet
Maagkanker behoort tot de dodelijkste vormen van kanker wereldwijd, grotendeels omdat het vaak uitzaait naar verre organen zoals de lever. Veel geneesmiddelen richten zich op het doden van kankercellen zelf, maar deze studie laat zien dat de omliggende "bodem" waarin kankercellen groeien — het steunweefsel en de gelachtige stof eromheen — net zo belangrijk kan zijn. Door te achterhalen hoe maagtumoren hun omgeving herschikken om in de lever te gedijen, wijst dit werk op nieuwe mogelijkheden om metastasen te blokkeren in plaats van alleen primaire tumoren te verkleinen.
Signalen die tumorgroei aandrijven
De onderzoekers richtten zich op een familie van moleculaire signalen genaamd Wnt, die helpen bij het reguleren van stamcellen in gezonde weefsels maar vaak door kankers worden gekaapt. Bij darmkanker wordt Wnt‑activiteit doorgaans aangestuurd door mutaties binnen de kankercellen zelf. Bij maagkanker zijn dergelijke mutaties minder gebruikelijk, maar is Wnt‑activiteit toch hoog. Dat suggereerde dat veel maagtumoren mogelijk afhankelijk zijn van Wnt‑liganden — signaalmoleculen die door cellen worden uitgescheiden — in plaats van permanente genetische schakelaars, wat de vraag oproept hoe deze externe signalen tumorgroei en verspreiding beïnvloeden.
Gemanipuleerde muismodellen die menselijke ziekte nabootsen
Om dit te onderzoeken creëerde het team geraffineerde muismodellen met combinaties van drie veelvoorkomende maagkankermutaties (in de genen Kras, Tgfbr2 en Trp53, gegroepeerd als KTP). Sommige muizen produceerden bovendien extra Wnt1‑ligand specifiek in de maag (WKTP). Muizen met alleen de kankerveroorzakende mutaties ontwikkelden verdikte maagbekledingen en abnormale celtypen, maar het toevoegen van Wnt1 versterkte deze veranderingen en leidde tot duidelijk dysplastische — precancereuze tot cancerogene — tumoren. Toen de wetenschappers mini‑tumoren (organoïden) van deze muizen groeiden en in ontvangers dieren transplanteerden, vormden zowel KTP‑ als WKTP‑cellen omvangrijke tumoren op de oorspronkelijke locatie, wat aantoont dat de set van drie driver‑mutaties voldoende was voor lokale tumorvorming.
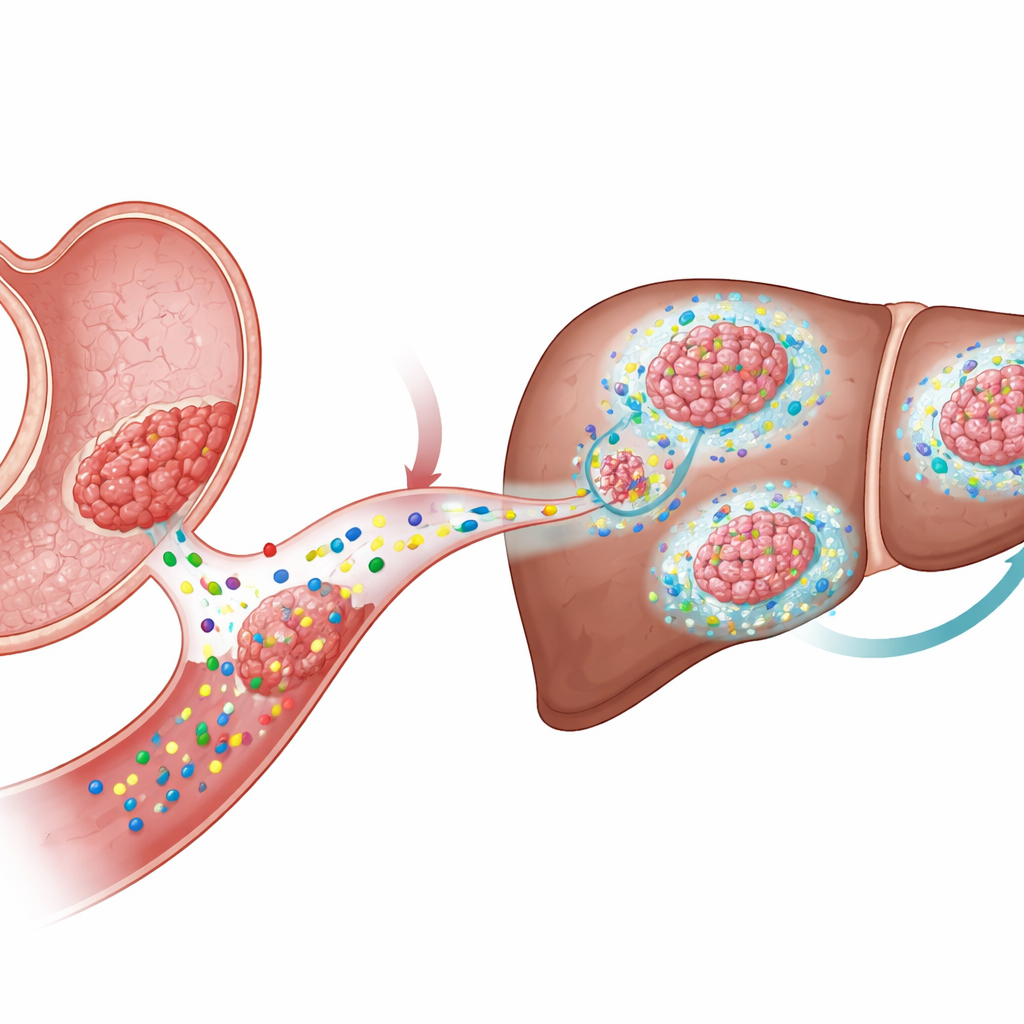
Wanneer en waar uitzaaiing naar de lever optreedt
Het belangrijkste verschil werd duidelijk toen de onderzoekers naar metastasen keken. Ze injecteerden KTP‑ of WKTP‑organoïden in de milt, een route die cellen rechtstreeks naar de lever voert. Alleen de Wnt1‑producerende WKTP‑cellen vormden grote, fibrotische metastatische tumoren in de lever, ook al arriveerden beide celtypen aanvankelijk in vergelijkbare aantallen. Middelen die de afgifte van Wnt‑liganden blokkeren verminderden levermetastasen sterk en zorgden ervoor dat de resterende tumoren gedifferentieerder en minder proliferatief leken. Interessant genoeg leidde het afdwingen van constante Wnt‑activiteit binnen KTP‑cellen door een poortwachtergen (Apc) uit te schakelen niet betrouwbaar tot metastasen. Dit geeft aan dat de rol van Wnt bij ziekteverspreiding afhangt van zijn werking in de omliggende niet‑kankercellen, en niet alleen binnen de tumorcellen zelf.
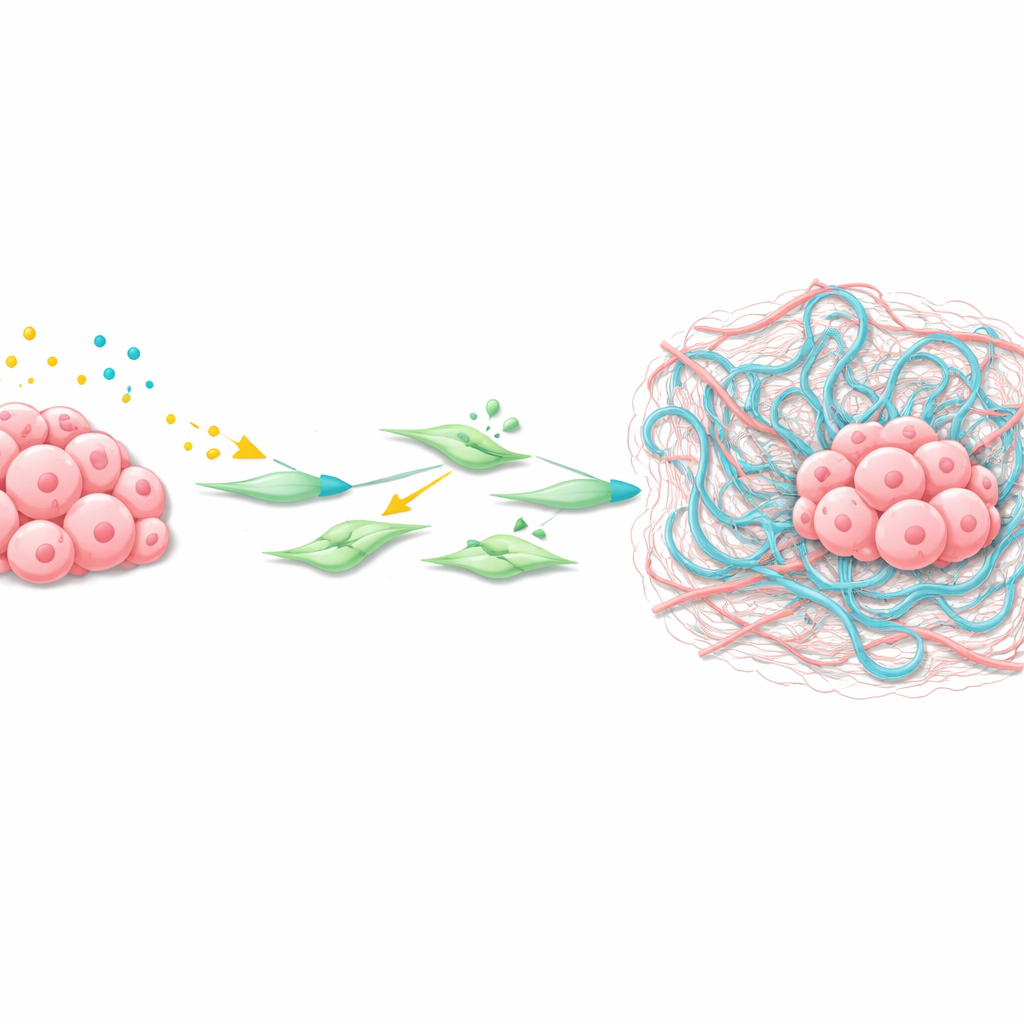
Hoe de tumor zijn omgeving hervormt
Met behulp van spatial transcriptomics — een techniek die genactiviteit over dunne weefselplakjes in kaart brengt — zocht het team dieper in de micro‑omgeving van levermetastasen. Ze vonden een groep kankergeassocieerde fibroblasten (CAF's) die de tumoren omringden en sterke Wnt‑ en TGFβ‑signalering vertoonden. Deze CAF's produceerden hoge niveaus van Has2, een enzym dat hyaluronaan synthetiseert, een lange suikerpolymeer die zich ophoopt als een viskeus netwerk in weefsels. Experimenten met geïsoleerde leverstellaatcellen en CAF's toonden dat Wnt‑liganden en TGFβ samenwerkten om Wnt‑doelgenen aan te zetten, de fibroblasten te activeren en Has2‑niveaus sterk te verhogen, wat leidde tot krachtige contractie en hermodellering van de omliggende matrix.
Een kleverig netwerk dat kanker helpt vestigen
De onderzoekers toonden vervolgens aan dat hyaluronaan zelf een sleutelmedeplichtige is. Zowel in muis‑ als in humane maagkankerlevermetastasen was hyaluronaan vanaf zeer vroege stadia overvloedig aanwezig rond tumor‑nestjes. Toen WKTP‑kankercellen zo werden gemodificeerd dat ze hyaluronidases — enzymen die hyaluronaan afbreken — produceerden, vormden ze nog steeds tumoren op de injectieplaats maar produceerden ze veel minder metastasen in de lever. Dit suggereert dat het kleverige, hyaluronaan‑rijke netwerk dat door geactiveerde fibroblasten wordt opgebouwd een beschermende, voedende niche vormt die uitgezette maagkankercellen helpt te overleven, te prolifereren en zich te organiseren tot volwaardige metastatische tumoren.
Wat dit betekent voor toekomstige behandelingen
Samen onthult de studie een keten van gebeurtenissen: maagtumoren scheiden Wnt‑signalen uit; deze werken samen met TGFβ om fibroblasten te activeren; de fibroblasten produceren grote hoeveelheden hyaluronaan en bouwen daarmee een fibrotische, gelachtige micro‑omgeving in de lever die metastatische uitgroei bevordert. Voor patiënten wijst dit op nieuwe strategieën die niet alleen op kankercellen gericht zijn. Therapieën die de productie of ontvangst van Wnt‑liganden blokkeren, die interfereren met TGFβ‑gedreven fibroblastactivatie, of die de ophoping van hyaluronaan voorkomen, zouden verre organen minder gastvrij kunnen maken voor rondzwervende maagkankercellen en zo een snel dodelijke ziekte mogelijk beter beheersbaar maken.
Bronvermelding: Furutani, Y., Oshima, H., Hong, C.P. et al. Ligand-dependent Wnt signaling promotes gastric cancer metastasis through hyaluronan expression in microenvironment. Nat Commun 17, 2777 (2026). https://doi.org/10.1038/s41467-026-69470-5
Trefwoorden: maagkanker, uitzaaiing, Wnt‑signaleringspad, tumormicro‑omgeving, hyaluronaan