Clear Sky Science · fr
La signalisation Wnt dépendante des ligands favorise les métastases du cancer gastrique via l’expression d’hyaluronane dans le microenvironnement
Pourquoi cette recherche importe
Le cancer gastrique figure parmi les cancers les plus meurtriers au monde, en grande partie parce qu’il se propage souvent vers des organes distants tels que le foie. Nombre de traitements visent à tuer directement les cellules cancéreuses, mais cette étude montre que le « sol » environnant dans lequel les cellules tumorales évoluent — le tissu de soutien et la matrice gélatineuse qui les entourent — peut être tout aussi déterminant. En révélant comment les tumeurs gastriques remodelent leur environnement pour prospérer dans le foie, ce travail ouvre la voie à de nouvelles approches visant à bloquer les métastases plutôt qu’à réduire uniquement la taille des tumeurs primaires.
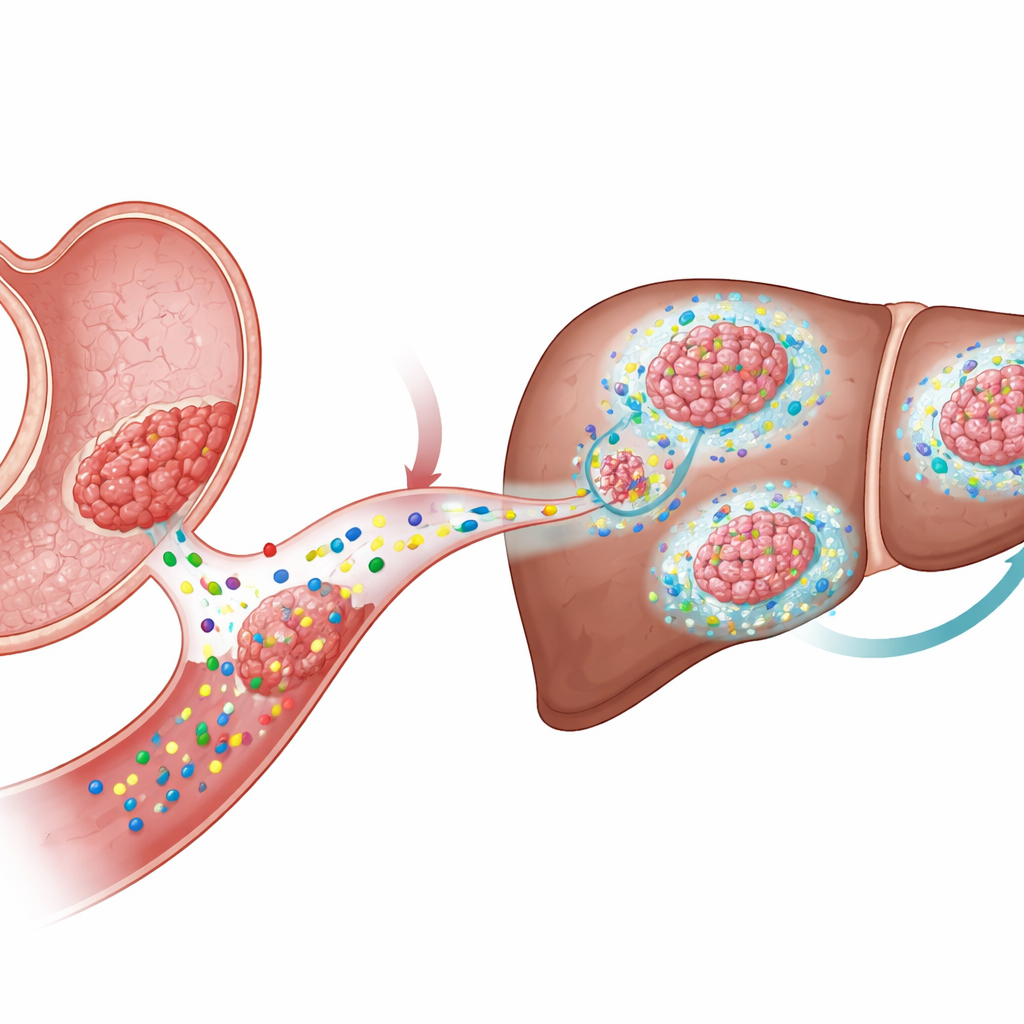
Les signaux qui stimulent la croissance tumorale
Les chercheurs se sont concentrés sur une famille de signaux moléculaires appelée Wnt, qui régule les cellules souches dans les tissus sains mais est fréquemment détournée par les cancers. Dans le cancer colorectal, l’activité Wnt est généralement portée par des mutations intrinsèques aux cellules tumorales. Dans le cancer gastrique, en revanche, ces mutations sont moins courantes, et pourtant l’activité Wnt reste élevée. Cela suggérait que de nombreuses tumeurs de l’estomac pourraient dépendre des ligands Wnt — des molécules de signalisation sécrétées par des cellules — plutôt que de commutateurs génétiques permanents, soulevant la question de savoir comment ces signaux externes influencent la croissance et la dissémination tumorales.
Souris modifiées qui reproduisent la maladie humaine
Pour explorer cette hypothèse, l’équipe a développé des modèles murins sophistiqués portant des combinaisons de trois mutations courantes du cancer gastrique (dans les gènes Kras, Tgfbr2 et Trp53, regroupées sous l’acronyme KTP). Certaines souris produisaient aussi un excès du ligand Wnt1 spécifiquement dans l’estomac (WKTP). Les souris ne portant que les mutations oncogènes développaient un épaississement de la muqueuse gastrique et des types cellulaires anormaux, tandis que l’addition de Wnt1 amplifiait ces altérations, produisant des tumeurs nettement dysplasiques — du stade précancéreux au stade cancéreux. Lorsque les scientifiques ont cultivé des mini-tumeurs (organoïdes) issues de ces souris et les ont transplantées dans des animaux receveurs, les cellules KTP et WKTP ont toutes deux formé de volumineuses tumeurs au site d’origine, montrant que l’ensemble des trois mutations suffisait à la formation tumorale locale.
Quand et où la dissémination vers le foie se produit
La différence clé est apparue lors de l’examen des métastases. Les chercheurs ont injecté des organoïdes KTP ou WKTP dans la rate, une voie qui dirige les cellules directement vers le foie. Seules les cellules WKTP productrices de Wnt1 ont formé de grandes métastases hépatiques fibreuses, bien que les deux types de cellules soient arrivées initialement en nombres similaires. Des médicaments bloquant la libération des ligands Wnt ont fortement réduit les métastases hépatiques et rendu les tumeurs restantes plus différenciées et moins prolifératives. Fait intéressant, forcer une activité Wnt constitutive à l’intérieur des cellules KTP en désactivant un gène régulateur (Apc) n’a pas produit de métastases de manière fiable. Cela indique que le rôle de Wnt dans la dissémination dépend de son action sur les cellules non tumorales environnantes, et pas seulement au sein des cellules tumorales elles‑mêmes.
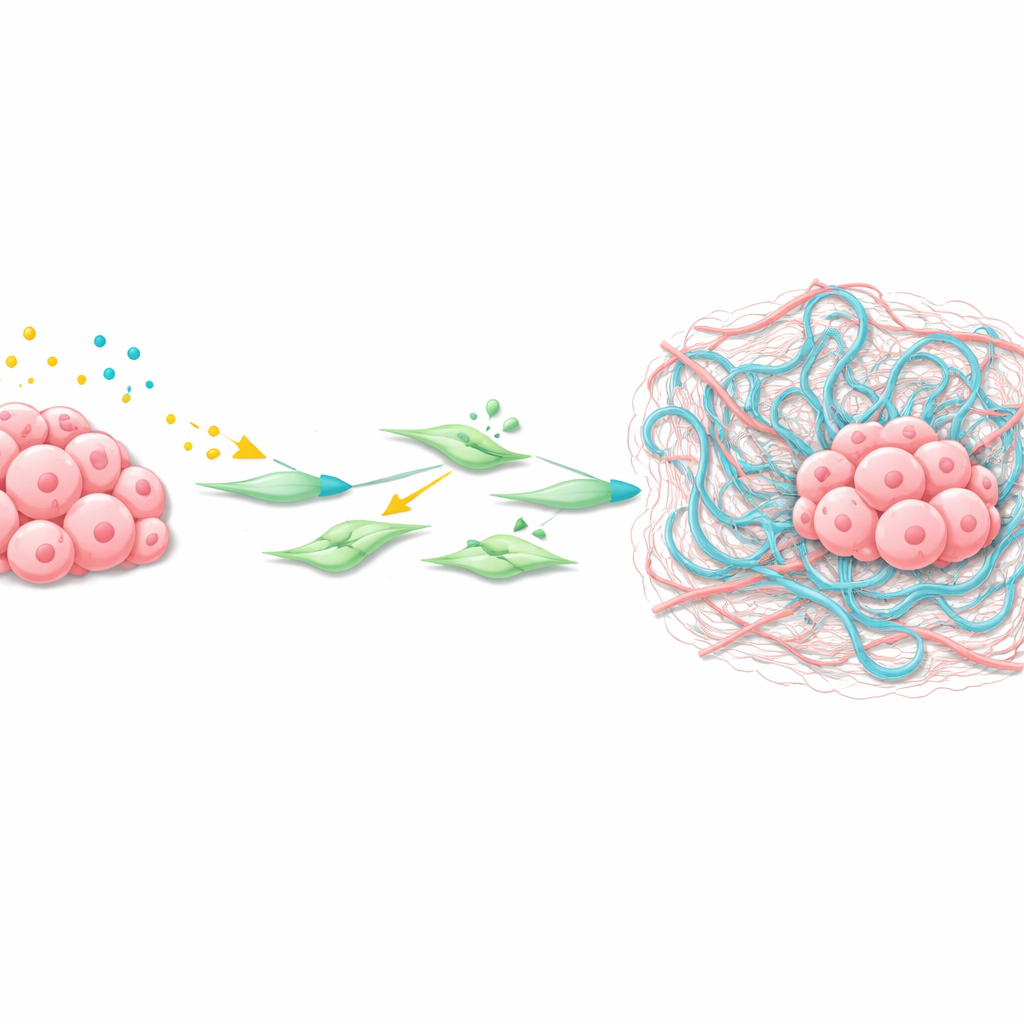
Comment la tumeur remodelle son voisinage
À l’aide de la transcriptomique spatiale — une technique qui cartographie l’activité génique à travers de fines sections de tissu — l’équipe s’est focalisée sur le microenvironnement des métastases hépatiques. Ils ont identifié un groupe de fibroblastes associés à la tumeur (CAF) entourant les tumeurs et présentant une forte activité des voies Wnt et TGFβ. Ces CAF exprimaient des niveaux élevés de Has2, une enzyme qui synthétise l’hyaluronane, un long polymère glucidique qui s’accumule sous forme d’un maillage visqueux dans les tissus. Des expériences sur des cellules stellaires hépatiques isolées et sur des CAF ont montré que les ligands Wnt et le TGFβ agissent de concert pour activer les gènes cibles de Wnt, activer les fibroblastes et augmenter fortement les niveaux de Has2, provoquant une forte contraction et un remodelage de la matrice environnante.
Une toile collante qui aide la colonisation tumorale
Les chercheurs ont ensuite démontré que l’hyaluronane elle‑même est un complice clé. Tant dans les métastases hépatiques de cancers gastriques murins qu’humains, l’hyaluronane était abondante autour des amas tumoraux dès les premiers stades. Lorsque des cellules cancéreuses WKTP ont été modifiées pour produire des hyaluronidases — des enzymes qui dégradent l’hyaluronane — elles ont continué de former des tumeurs au site d’injection mais ont généré beaucoup moins de métastases hépatiques. Cela suggère que la matrice riche en hyaluronane, collante, créée par les fibroblastes activés constitue une niche protectrice et nourricière qui aide les cellules de cancer gastrique disséminées à survivre, proliférer et s’organiser en véritables tumeurs métastatiques.
Implications pour les traitements futurs
Dans l’ensemble, l’étude révèle une chaîne d’événements : les tumeurs gastriques sécrètent des signaux Wnt ; ceux‑ci coopèrent avec le TGFβ pour activer les fibroblastes ; les fibroblastes produisent d’importantes quantités d’hyaluronane, bâtissant un microenvironnement hépatique fibreux et gélifié qui favorise la croissance métastatique. Pour les patients, cela suggère de nouvelles stratégies qui ne ciblent pas uniquement les cellules cancéreuses. Des thérapies bloquant la production ou la réception des ligands Wnt, interférant avec l’activation des fibroblastes par le TGFβ, ou empêchant l’accumulation d’hyaluronane pourraient rendre les organes distants moins hospitaliers aux cellules gastriques disséminées, transformant potentiellement une maladie rapidement létale en une pathologie plus contrôlable.
Citation: Furutani, Y., Oshima, H., Hong, C.P. et al. Ligand-dependent Wnt signaling promotes gastric cancer metastasis through hyaluronan expression in microenvironment. Nat Commun 17, 2777 (2026). https://doi.org/10.1038/s41467-026-69470-5
Mots-clés: cancer gastrique, métastase, signalisation Wnt, microenvironnement tumoral, hyaluronane