Clear Sky Science · ar
إشارات Wnt المعتمدة على الليجند تعزز انتقال سرطان المعدة عبر التعبير عن الهيالورونان في البيئة الميكروية
لماذا تهم هذه الدراسة
سرطان المعدة يعد من أكثر السرطانات فتكًا في العالم إلى حد كبير لأنه غالبًا ما ينتشر إلى أعضاء بعيدة مثل الكبد. تركز العديد من الأدوية على قتل الخلايا السرطانية نفسها، لكن هذه الدراسة تُظهر أن «التربة» المحيطة التي تنمو فيها الخلايا السرطانية — النسيج الداعم والمادة الشبيهة بالجِل حولها — قد تكون مهمة بنفس القدر. من خلال كشف كيفية إعادة أورام المعدة تشكيل بيئتها لتزدهر في الكبد، يشير هذا العمل إلى طرق جديدة لعرقلة الانبثاث بدلاً من الاكتفاء بتقليص الأورام الأولية.
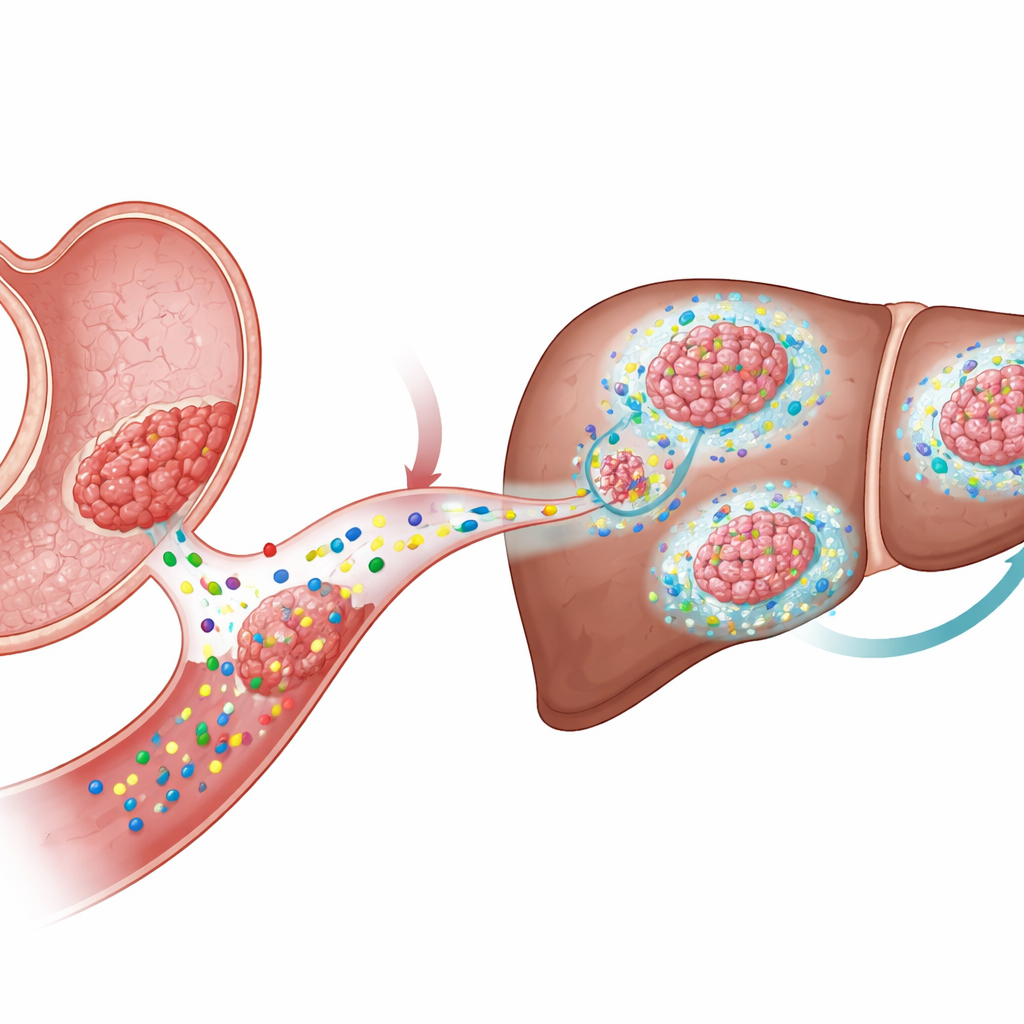
الإشارات التي تُحرّك نمو الورم
ركز الباحثون على عائلة من الإشارات الجزيئية تُسمى Wnt، التي تساعد في تنظيم الخلايا الجذعية في الأنسجة السليمة لكنها غالبًا ما تُستغل من قبل السرطانات. في سرطان القولون، يكون نشاط Wnt مدفوعًا عادةً بطفرات داخل الخلايا السرطانية نفسها. أما في سرطان المعدة فمثل هذه الطفرات أقل شيوعًا، ومع ذلك يبقى نشاط Wnt مرتفعًا. هذا يوحي بأن العديد من أورام المعدة قد تعتمد على الليجندات — جزيئات الإشارة المفرزة من الخلايا — بدلاً من مفاتيح جينية دائمة، مما يثير السؤال عن كيفية تأثير هذه الإشارات الخارجية على نمو الورم وانتشاره.
فئران مهندَسة تحاكي المرض البشري
لاستكشاف ذلك، أنشأ الفريق نماذج فئران متطورة تحمل تركيبات من ثلاث طفرات شائعة في سرطان المعدة (في الجينات Kras، Tgfbr2، وTrp53، المجموعة المسماة KTP). بعض الفئران أنتجت أيضًا كمية إضافية من الليجند Wnt1 مخصّصة في المعدة (WKTP). الفئران التي تحمل الطفرات المحركة للسرطان فقط طورت بطانة معدة سميكة وأنواعًا خلوية غير طبيعية، لكن إضافة Wnt1 دفع هذه التغيرات إلى الأمام، منتجة أورامًا واضحة التباين — ما بين ما قبل السرطاني والسرطاني. عندما نما العلماء أورامًا مصغرة (أورجانويدات) من هذه الفئران وزرعوها في حيوانات مستقبلِة، شكّلت كل من خلايا KTP وWKTP أورامًا كبيرة في الموضع الأصلي، مبيّنة أن مجموعة الطفرات الثلاث كانت كافية لتكوين ورم موضعي.
متى وأين يحدث الانتشار إلى الكبد
برز الفرق الرئيسي عندما درس الباحثون الانبثاث. حقنوا أورجانويدات KTP أو WKTP في الطحال، وهو طريق يرسل الخلايا مباشرةً إلى الكبد. فقط خلايا WKTP المنتجة لـWnt1 كونت أورامًا انتقالية كبيرة وتليفية في الكبد، على الرغم من أن كلا النوعين من الخلايا وصل في البداية إلى هناك بأعداد متشابهة. الأدوية التي تمنع إطلاق ليجندات Wnt قللت بشدة من الانبثاث الكبدي وجعلت الأورام المتبقية تبدو أكثر تمايزًا وأقل تكاثرًا. ومن المثير للاهتمام أن إجبار نشاط Wnt المستمر داخل خلايا KTP عن طريق تعطيل جين بوّاب (Apc) لم يُنتج الانبثاث بشكل موثوق. وهذا يشير إلى أن دور Wnt في انتشار المرض يعتمد على فعاليته في الخلايا المجاورة غير السرطانية، وليس فقط داخل خلايا الورم نفسها.
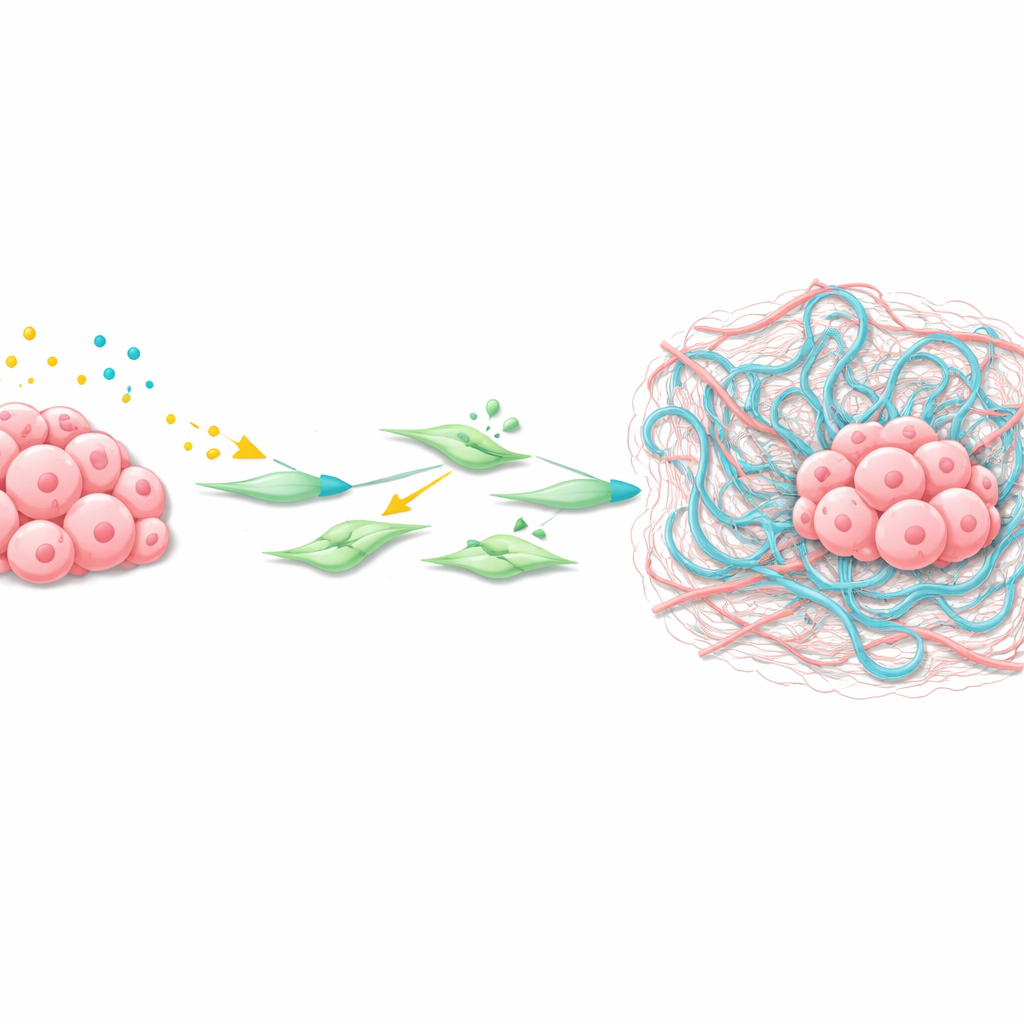
كيف يعيد الورم تشكيل جواره
باستخدام النسخ المكانية — تقنية ترسم نشاط الجينات عبر شرائح نسيجية رقيقة — ركز الفريق على بيئة الميكروفملة للانِبِثاث الكبدي. وجدوا مجموعة من الخلايا الليفية المرتبطة بالسرطان (CAFs) تحيط بالأورام مع نشاط قوي لإشارات Wnt وTGFβ. هذه الخلايا الليفية أنتجت مستويات عالية من Has2، إنزيم يصنع الهيالورونان، وهو بوليمر سكري طويل يتراكم كشبكة لزجة في الأنسجة. أظهرت تجارب بالخلايا النجمية الكبدية المعزولة وCAFs أن ليجندات Wnt وTGFβ تعملان معًا لتشغيل جينات الهدف للـWnt، وتفعيل الخلايا الليفية، وزيادة مستويات Has2 بشكل كبير، مما يسبب تقلصًا وإعادة تشكيل قوية للمصفوفة المحيطة.
شبكة لزجة تساعد السرطان على الاستقرار
بعد ذلك بيّن الباحثون أن الهيالورونان نفسه شريك أساسي. في كل من انبثاثات سرطان المعدة في الكبد لدى الفئران والبشر، كان الهيالورونان وفيرًا حول أعشاش الورم منذ المراحل المبكرة جدًا. عندما عدّلوا خلايا السرطان WKTP لتنتج هيالورونيدات — إنزيمات تكسر الهيالورونان — فقد شكّلت أورامًا في موقع الحقن لكنها أنتجت معدلات أقل بكثير من الانبثاثات في الكبد. هذا يشير إلى أن المصفوفة الغنية بالهيالورونان اللزجة التي تصنعها الخلايا الليفية النشيطة تشكل فجوة واقية ومغذية تساعد الخلايا السرطانية المهاجرة على النجاة، والتكاثر، والتنظيم إلى أورام انتقالية كاملة.
ما الذي يعنيه هذا للعلاجات المستقبلية
بشكل مجمل، تكشف الدراسة سلسلة من الأحداث: تفرز أورام المعدة إشارات Wnt؛ هذه تتعاون مع TGFβ لتنشيط الخلايا الليفية؛ تصنع الخلايا الليفية كميات كبيرة من الهيالورونان، مبنيةً بيئة ميكروية تليفية وجيلاتينية في الكبد تُفضّل نمو الانبثاث. للمرضى، يشير ذلك إلى استراتيجيات جديدة لا تستهدف الخلايا السرطانية وحدها. قد تجعل العلاجات التي تمنع إنتاج أو استقبال ليجندات Wnt، أو تتداخل مع تنشيط الخلايا الليفية المحفز بـTGFβ، أو تمنع تراكم الهيالورونان، الأعضاء البعيدة أقل ملاءمة لخلايا سرطان المعدة المهاجرة، مما قد يحول مرضًا قاتلًا بسرعة إلى حالة أكثر قابلية للسيطرة.
الاستشهاد: Furutani, Y., Oshima, H., Hong, C.P. et al. Ligand-dependent Wnt signaling promotes gastric cancer metastasis through hyaluronan expression in microenvironment. Nat Commun 17, 2777 (2026). https://doi.org/10.1038/s41467-026-69470-5
الكلمات المفتاحية: سرطان المعدة, الانبثاث, إشارة Wnt, البيئة الميكروية للورم, هيالورونان