Clear Sky Science · es
La señalización Wnt dependiente de ligando promueve la metástasis del cáncer gástrico mediante la expresión de hialuronano en el microambiente
Por qué importa esta investigación
El cáncer gástrico es uno de los más mortales del mundo, en gran parte porque con frecuencia se disemina a órganos distantes, como el hígado. Muchas drogas se centran en matar las propias células cancerosas, pero este estudio muestra que el “suelo” circundante en el que crecen las células tumorales —el tejido de sostén y la matriz gelatinosa a su alrededor— puede ser igual de importante. Al revelar cómo los tumores de estómago remodelan su entorno para prosperar en el hígado, este trabajo apunta a nuevas formas de bloquear la metástasis en lugar de limitarse a reducir el tumor primario.
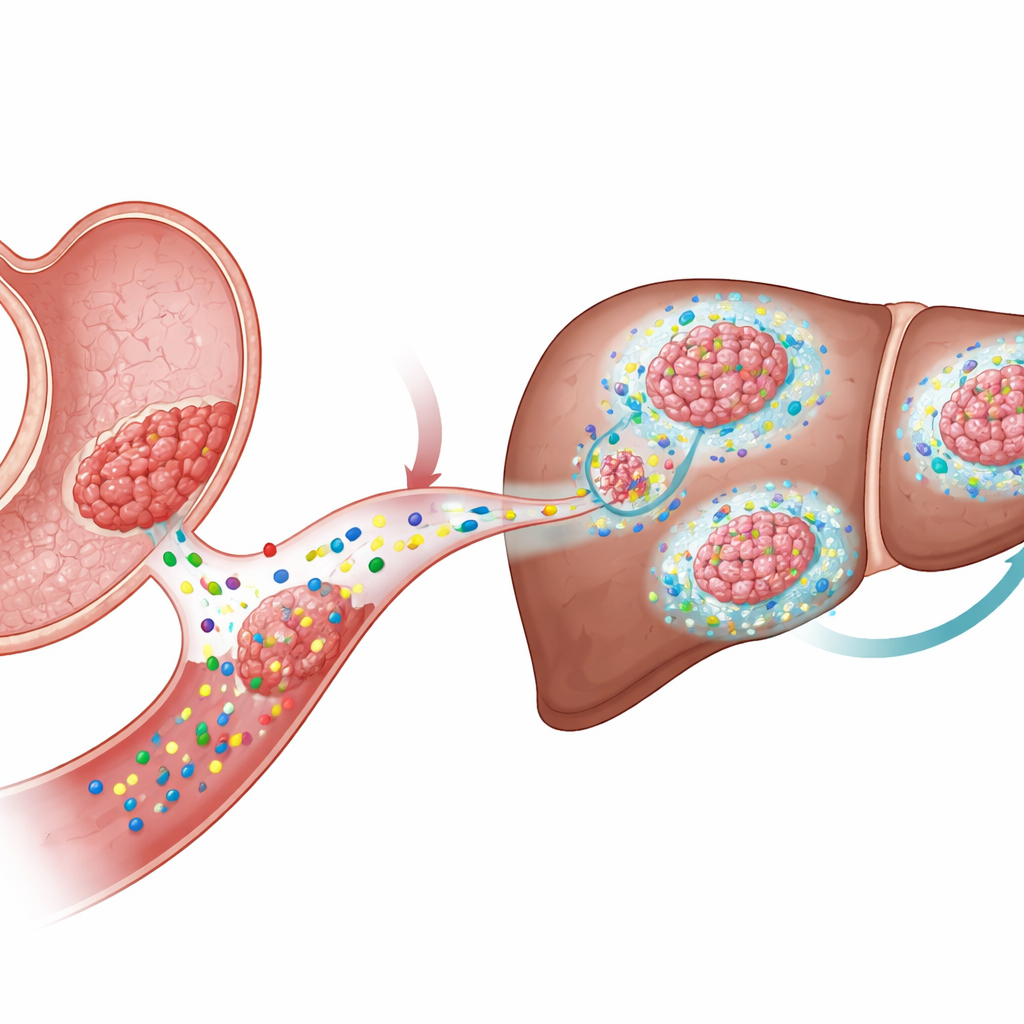
Señales que impulsan el crecimiento tumoral
Los investigadores se centraron en una familia de señales moleculares llamadas Wnt, que ayudan a regular las células madre en tejidos sanos pero que con frecuencia son secuestradas por los cánceres. En el cáncer de colon, la actividad Wnt suele estar impulsada por mutaciones dentro de las propias células cancerosas. Sin embargo, en el cáncer gástrico esas mutaciones son menos comunes, pese a que la actividad Wnt sigue siendo alta. Esto sugiere que muchos tumores gástricos pueden depender de ligandos Wnt —moléculas de señal secretadas por células— en lugar de interruptores genéticos permanentes, lo que plantea la pregunta de cómo estas señales externas influyen en el crecimiento y la diseminación tumoral.
Ratones diseñados que imitan la enfermedad humana
Para explorar esto, el equipo creó modelos murinos sofisticados que portaban combinaciones de tres mutaciones comunes en cáncer gástrico (en los genes Kras, Tgfbr2 y Trp53, agrupadas como KTP). Algunos ratones también producían Wnt1 adicional específicamente en el estómago (WKTP). Los animales con solo las mutaciones impulsoras del cáncer desarrollaron un engrosamiento del revestimiento gástrico y tipos celulares anormales, pero añadir Wnt1 potenció esos cambios, produciendo tumores claramente displásicos —de pre-cancerosos a cancerosos—. Cuando los científicos cultivaron mini-tumores (organoides) de estos ratones y los trasplantaron a animales receptores, tanto las células KTP como WKTP formaron tumores voluminosos en el sitio original, demostrando que el conjunto de tres mutaciones era suficiente para la formación tumoral local.
Cuándo y dónde ocurre la diseminación al hígado
La diferencia clave surgió al estudiar la metástasis. Inyectaron organoides KTP o WKTP en el bazo, una vía que envía células directamente al hígado. Solo las células WKTP productoras de Wnt1 formaron grandes tumores metastásicos fibrosos en el hígado, aunque ambos tipos de células llegaron inicialmente allí en números similares. Fármacos que bloquean la liberación de ligandos Wnt redujeron drásticamente las metástasis hepáticas y provocaron que los tumores restantes parecieran más diferenciados y menos proliferativos. Curiosamente, forzar una actividad Wnt constante dentro de las células KTP mediante la desactivación de un gen guardián (Apc) no produjo metástasis de forma fiable. Esto indicó que el papel de Wnt en la diseminación depende de su acción en las células no cancerosas circundantes, no solo dentro de las células tumorales.
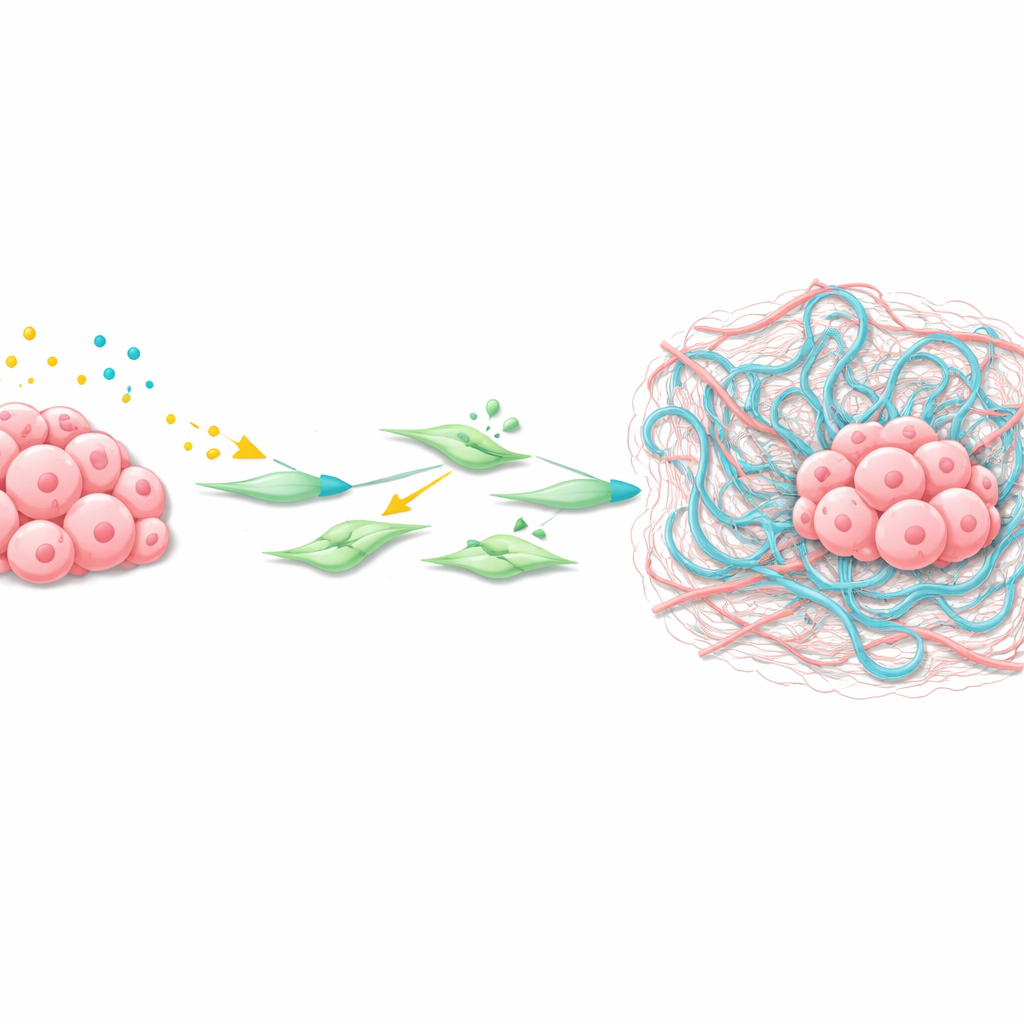
Cómo el tumor remodela su vecindario
Usando transcriptómica espacial —una técnica que mapea la actividad génica a lo largo de finas secciones de tejido—, el equipo analizó en detalle el microambiente de las metástasis hepáticas. Encontraron un cúmulo de fibroblastos asociados al cáncer (CAF) rodeando los tumores con una fuerte actividad de las vías Wnt y TGFβ. Estos CAF producían altos niveles de Has2, una enzima que sintetiza hialuronano, un polímero largo de azúcares que se acumula como una malla viscosa en los tejidos. Experimentos con células estrelladas hepáticas aisladas y CAF mostraron que los ligandos Wnt y TGFβ actúan conjuntamente para activar genes diana de Wnt, activar los fibroblastos y aumentar en gran medida los niveles de Has2, provocando una fuerte contracción y remodelación de la matriz circundante.
Una red pegajosa que ayuda al asentamiento del cáncer
Los investigadores demostraron después que el propio hialuronano es un cómplice clave. Tanto en metástasis hepáticas de cáncer gástrico en ratón como en humano, el hialuronano era abundante alrededor de los nidos tumorales desde etapas muy tempranas. Cuando las células cancerosas WKTP se modificaron para producir hialuronidasas —enzimas que degradan el hialuronano—, siguieron formando tumores en el sitio de inyección, pero produjeron muchas menos metástasis en el hígado. Esto sugiere que la matriz pegajosa rica en hialuronano creada por fibroblastos activados forma un nicho protector y nutritivo que ayuda a las células gástricas diseminadas a sobrevivir, proliferar y organizarse en tumores metastásicos completos.
Qué implica esto para futuros tratamientos
En conjunto, el estudio revela una cadena de eventos: los tumores gástricos secretan señales Wnt; estas cooperan con TGFβ para activar fibroblastos; los fibroblastos sintetizan grandes cantidades de hialuronano, construyendo un microambiente fibrótico y gelatinoso en el hígado que favorece el crecimiento metastásico. Para los pacientes, esto señala nuevas estrategias que no atacan únicamente a las células cancerosas. Terapias que bloqueen la producción o la recepción de ligandos Wnt, que interfieran con la activación de fibroblastos impulsada por TGFβ, o que prevengan la acumulación de hialuronano podrían hacer que los órganos distantes sean menos hospitalarios para las células de cáncer gástrico diseminadas, posiblemente transformando una enfermedad rápidamente letal en otra más manejable.
Cita: Furutani, Y., Oshima, H., Hong, C.P. et al. Ligand-dependent Wnt signaling promotes gastric cancer metastasis through hyaluronan expression in microenvironment. Nat Commun 17, 2777 (2026). https://doi.org/10.1038/s41467-026-69470-5
Palabras clave: cáncer gástrico, metástasis, señalización Wnt, microambiente tumoral, hialuronano