Clear Sky Science · pl
Sygnalizacja Wnt zależna od ligandów promuje przerzuty raka żołądka poprzez ekspresję hialuronanu w mikrośrodowisku
Dlaczego to badanie jest ważne
Rak żołądka jest jednym z najbardziej śmiertelnych nowotworów na świecie, w dużej mierze dlatego, że często rozprzestrzenia się do odległych narządów, takich jak wątroba. Wiele leków koncentruje się na zabijaniu samych komórek nowotworowych, lecz to badanie pokazuje, że otaczająca „gleba”, w której rosną komórki — wspierające tkanki i żelopodobna substancja wokół nich — może być równie istotna. Odkrywając, w jaki sposób guzy żołądka przekształcają swoje środowisko, by przetrwać w wątrobie, praca ta wskazuje nowe sposoby blokowania przerzutów zamiast jedynie zmniejszania guzów pierwotnych.
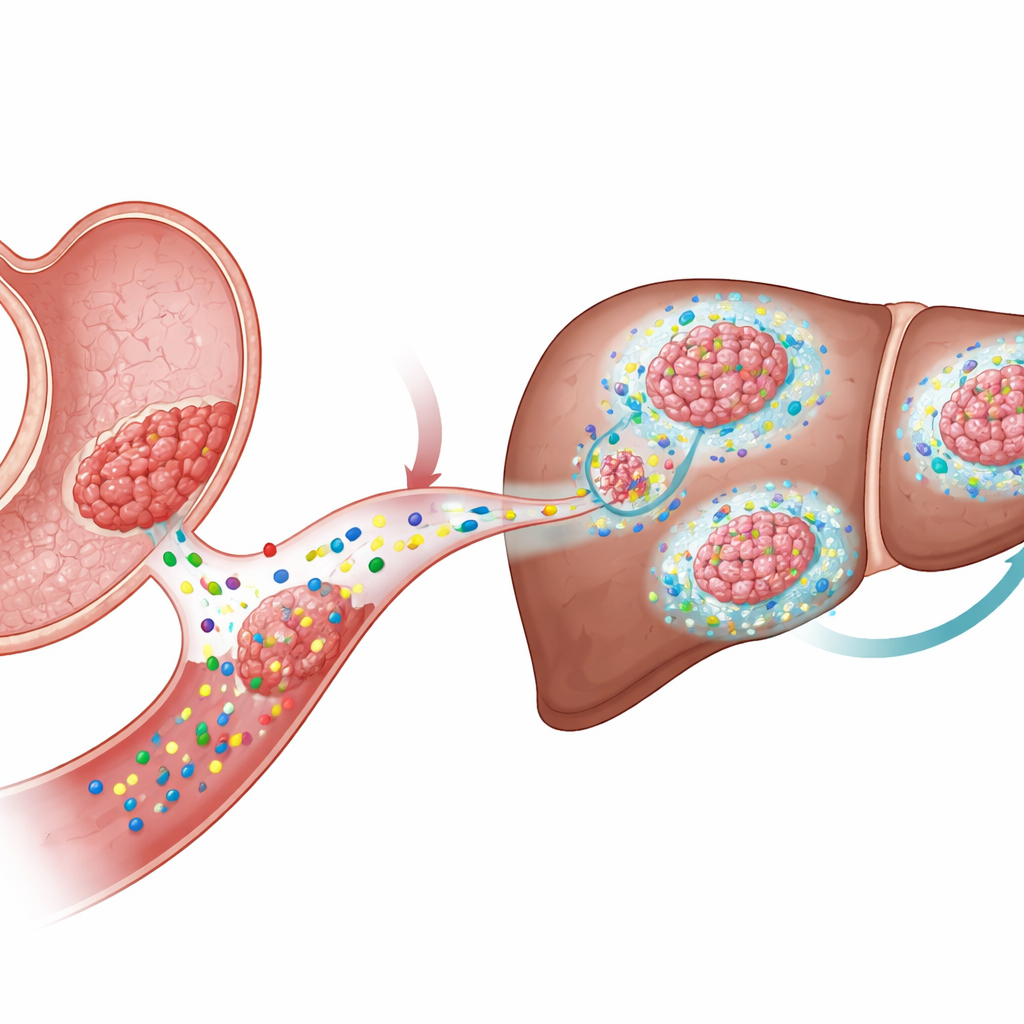
Sygnały napędzające wzrost guza
Naukowcy skupili się na rodzinie molekularnych sygnałów zwanych Wnt, które regulują komórki macierzyste w zdrowych tkankach, ale są często wykorzystywane przez nowotwory. W raku jelita grubego aktywność Wnt zwykle wynika z mutacji wewnątrz komórek nowotworowych. W raku żołądka takie mutacje są jednak rzadsze, a mimo to aktywność Wnt jest wysoka. Sugerowało to, że wiele guzów żołądka może polegać na ligandach Wnt — cząsteczkach sygnałowych wydzielanych przez komórki — zamiast na trwałych przełącznikach genetycznych, co rodzi pytanie, jak zewnętrzne sygnały wpływają na wzrost i rozprzestrzenianie się guza.
Zmodyfikowane myszy naśladujące chorobę u ludzi
Aby to zbadać, zespół stworzył zaawansowane modele myszy z kombinacjami trzech powszechnych mutacji raka żołądka (w genach Kras, Tgfbr2 i Trp53, zgrupowanych jako KTP). Niektóre myszy dodatkowo produkowały nadmiar liganda Wnt1 specyficznie w żołądku (WKTP). Myszy posiadające tylko mutacje napędzające nowotwór rozwinęły pogrubione wyściółki żołądka i nieprawidłowe typy komórek, ale dodanie Wnt1 wzmocniło te zmiany, prowadząc do wyraźnie dysplastycznych — od przednowotworowych po nowotworowe — guzów. Gdy naukowcy hodowali mini-guzki (organoidy) z tych myszy i przeszczepiali je do biorców, zarówno komórki KTP, jak i WKTP tworzyły znaczne guzy w miejscu pierwotnym, co pokazało, że zestaw trzech mutacji wystarcza do powstania lokalnego guza.
Kiedy i gdzie dochodzi do rozprzestrzeniania się do wątroby
Kluczowa różnica ujawniła się przy badaniu przerzutów. Naukowcy wstrzykiwali organoidy KTP lub WKTP do śledziony — trasą, która wysyła komórki bezpośrednio do wątroby. Tylko komórki produkujące Wnt1 (WKTP) tworzyły duże, włókniste guzy przerzutowe w wątrobie, mimo że oba typy komórek początkowo docierały tam w podobnej liczbie. Leki blokujące uwalnianie ligandów Wnt znacząco zmniejszały liczbę przerzutów w wątrobie i powodowały, że pozostałe guzy wyglądały na bardziej zróżnicowane i mniej proliferujące. Co ciekawe, wymuszenie stałej aktywności Wnt wewnątrz komórek KTP przez unieruchomienie stróża-gena (Apc) nie powodowało niezawodnie przerzutów. Wskazywało to, że rola Wnt w rozprzestrzenianiu choroby zależy od jego działania w otaczających, nie-nowotworowych komórkach, a nie tylko wewnątrz samych komórek guza.
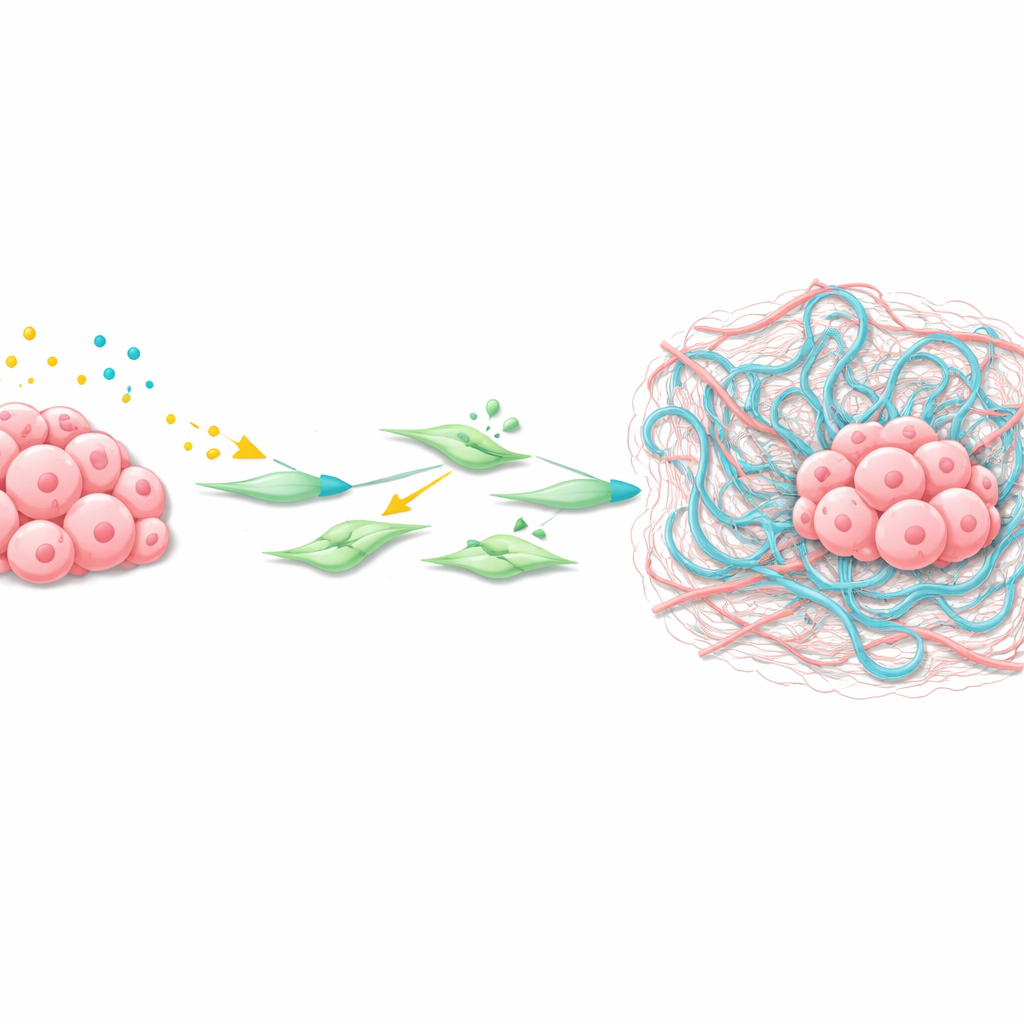
Jak guz przekształca swoje otoczenie
Wykorzystując transkryptomikę przestrzenną — technikę mapowania aktywności genów w cienkich przekrojach tkanek — zespół przyjrzał się mikrośrodowisku przerzutów w wątrobie. Odkryli skupisko fibroblastów związanych z rakiem (CAF) otaczających guzy z wyraźnie aktywną sygnalizacją Wnt i TGFβ. Te CAFy wytwarzały wysokie poziomy Has2, enzymu syntetyzującego hialuronan, długi polimer cukrowy, który kumuluje się jako lepka sieć w tkankach. Eksperymenty z izolowanymi komórkami gwiaździstymi wątroby i CAF wykazały, że ligandy Wnt i TGFβ działają razem, aby włączyć geny docelowe Wnt, aktywować fibroblasty i znacznie zwiększyć poziomy Has2, powodując silne skurcze i przebudowę otaczającej macierzy.
Lepka sieć, która pomaga rakowi osiedlić się
Następnie badacze wykazali, że sam hialuronan jest kluczowym wspólnikiem. Zarówno w mysich, jak i ludzkich przerzutach raka żołądka do wątroby, hialuronan był obfity wokół gniazd guza już na bardzo wczesnych etapach. Gdy komórki WKTP zostały zmodyfikowane tak, by produkować hialuronidazy — enzymy rozkładające hialuronan — nadal tworzyły guzy w miejscu wstrzyknięcia, ale w wątrobie wytwarzały znacznie mniej przerzutów. Sugeruje to, że lepka, bogata w hialuronan macierz tworzona przez aktywowane fibroblasty stanowi ochronną, wspierającą niszę, która pomaga rozproszonym komórkom raka żołądka przetrwać, proliferować i organizować się w pełne guzy przerzutowe.
Co to oznacza dla przyszłych terapii
Podsumowując, badanie ujawnia łańcuch zdarzeń: guzy żołądka wydzielają sygnały Wnt; te współdziałają z TGFβ, aby aktywować fibroblasty; fibroblasty produkują duże ilości hialuronanu, budując włókniste, żelopodobne mikrośrodowisko w wątrobie sprzyjające wzrostowi przerzutów. Dla pacjentów wskazuje to nowe strategie, które nie celują wyłącznie w komórki nowotworowe. Terapie blokujące produkcję lub odbiór ligandów Wnt, zakłócające aktywację fibroblastów przez TGFβ lub zapobiegające gromadzeniu się hialuronanu mogą uczynić odległe narządy mniej gościnnymi dla przemieszczających się komórek raka żołądka, potencjalnie przekształcając szybko śmiertelną chorobę w bardziej kontrolowalną.
Cytowanie: Furutani, Y., Oshima, H., Hong, C.P. et al. Ligand-dependent Wnt signaling promotes gastric cancer metastasis through hyaluronan expression in microenvironment. Nat Commun 17, 2777 (2026). https://doi.org/10.1038/s41467-026-69470-5
Słowa kluczowe: rak żołądka, przerzuty, sygnalizacja Wnt, mikrośrodowisko guza, hialuronan